Clear Sky Science · pt
Candesartana cilexetil desestabiliza a membrana de Staphylococcus aureus resistente à meticilina e potencializa a atividade da gentamicina e do polimixina B
Transformando um remédio para pressão arterial em aliado contra germes
Staphylococcus aureus resistente à meticilina (MRSA) é um microrganismo persistente em hospitais e na comunidade que resiste a muitos dos nossos melhores antibióticos. Este estudo faz uma pergunta inesperada: um fármaco comum para pressão arterial, a candesartana cilexetil, pode ser reposicionado para enfraquecer o MRSA e tornar os antibióticos padrão mais eficazes? Ao examinar células de MRSA por múltiplas abordagens — química, genética, imagens e modelos animais — os pesquisadores mostram como esse comprimido pode furar as defesas bacterianas e reviver drogas antigas.
Por que o Staph resistente a drogas é tão difícil de tratar
O MRSA causa centenas de milhares de infecções graves e milhares de mortes todos os anos. Uma razão pela qual é tão difícil de tratar é que a membrana externa e a parede celular da bactéria funcionam como um escudo sofisticado. As moléculas gordurosas nesse escudo podem ser reorganizadas para se tornarem mais duras, menos permeáveis e mais resistentes aos antibióticos convencionais. Algumas células de MRSA também entram em estados de crescimento lento chamados “persisters” ou se escondem em biofilmes pegajosos, onde toleram drogas que normalmente matariam bactérias ativas. Essas características tornam crucial encontrar novas formas de atacar a superfície bacteriana em vez de projetar outro antibiótico tradicional do zero.
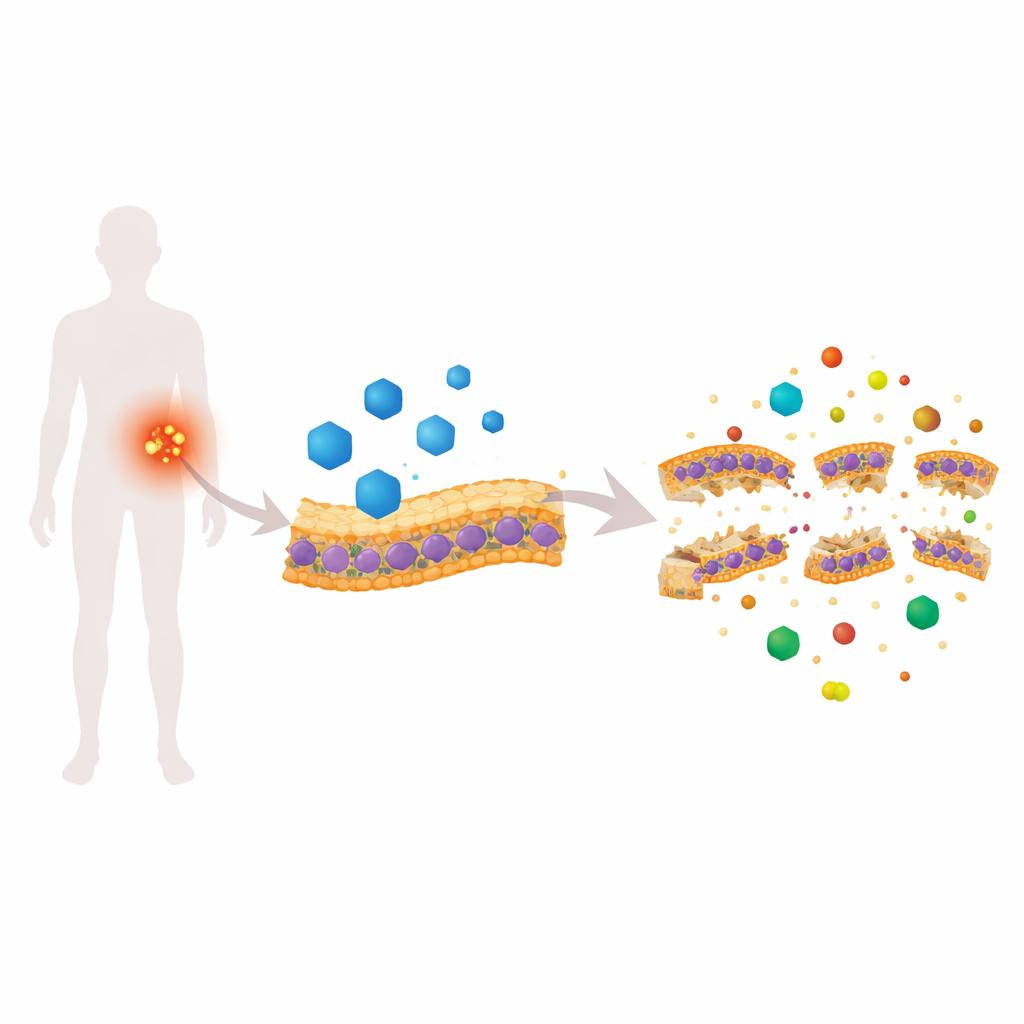
Um remédio cardíaco que ataca a “pele” bacteriana
A candesartana cilexetil (CC) é aprovada para tratar hipertensão, mas em uma triagem com vermes mostrou, de forma inesperada, forte atividade contra MRSA. Em testes de laboratório, a CC matou MRSA em divisão ativa e também as células mais resistentes em fase estacionária, além de reduzir a formação e a viabilidade de biofilmes. Experimentos detalhados com corantes fluorescentes revelaram que a CC torna a membrana do MRSA rapidamente permeável, colapsa o gradiente elétrico através dela e torna o interior da célula extraordinariamente alcalino. Imagens de alta resolução — microscopia eletrônica de varredura, microscopia de força atômica, microscopia eletrônica de transmissão e crio-tomografia 3D — mostraram superfícies com bolhas, afinamento da membrana e lacunas visíveis, todos sinais de que a “pele” bacteriana está fisicamente comprometida.
Reprogramando a química e a camada lipídica do microrganismo
Para entender o que a CC faz internamente, a equipe combinou sequenciamento de RNA, perfilagem de metabólitos e análise lipídica. Eles descobriram que genes e pequenas moléculas envolvidos na construção da parede celular, na síntese de lipídios de membrana e na geração de energia foram amplamente reduzidos após a exposição à CC, mesmo em doses muito baixas para matar diretamente. Vários fosfolipídios-chave que ajudam a manter a membrana intacta diminuíram em abundância. Uma mudança marcante envolveu um grupo particular de ácidos graxos longos de 20 carbonos (chamados C20:0). Quando os pesquisadores usaram outro composto, a cerulenina, para depletar esses ácidos graxos, o MRSA tornou-se menos sensível à CC. A reposição dos ácidos graxos C20:0 restaurou grande parte da eficácia do fármaco, e ensaios de ligação separados mostraram interação direta da CC com lipídios ligados a C20:0 e componentes de superfície relacionados. Medições da “fluidez” da membrana indicaram que a CC, na verdade, torna a membrana do MRSA mais rígida, travando os lipídios em um estado menos móvel que acaba minando sua função.
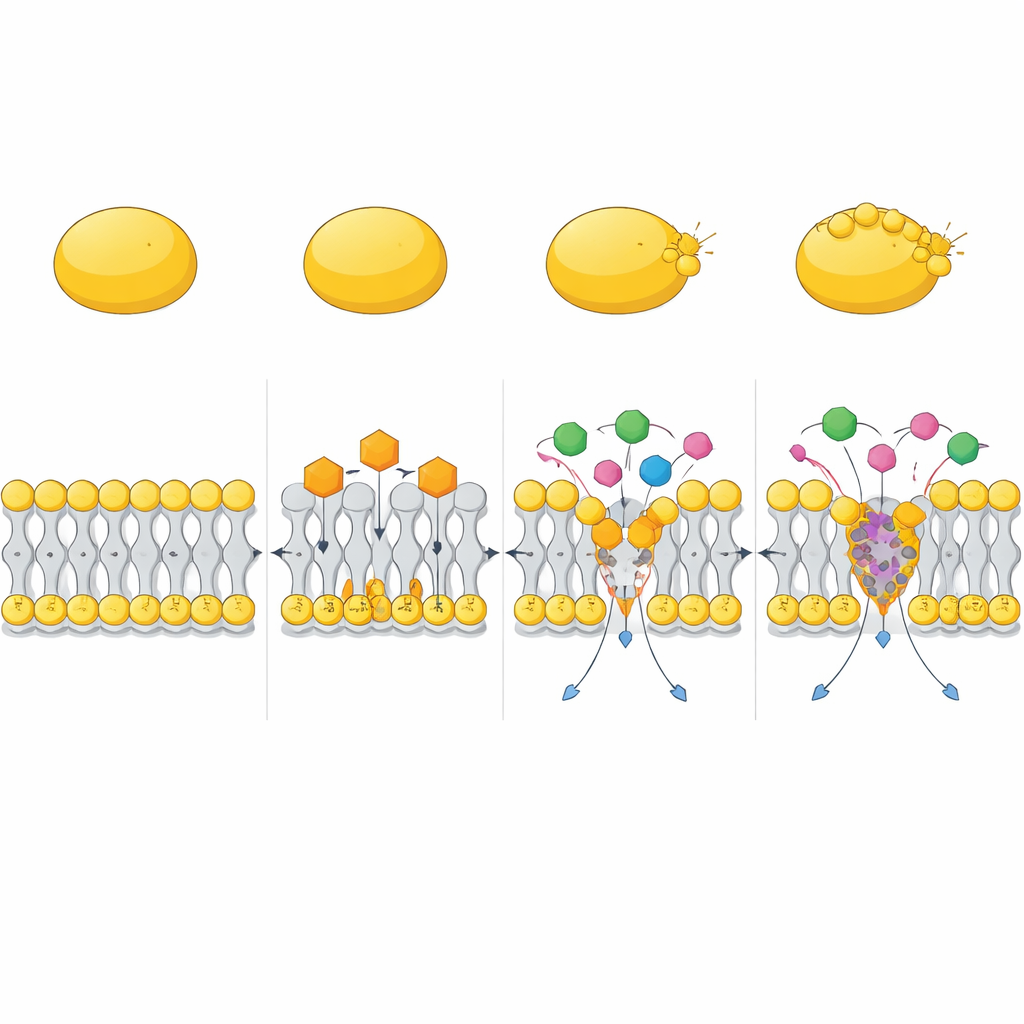
Em parceria com antibióticos existentes
O estudo também testou como a CC se comporta em conjunto com drogas já usadas. Em experimentos do tipo checkerboard e de redução de viabilidade ao longo do tempo, a CC aumentou dramaticamente a atividade de aminoglicosídeos como a gentamicina, assim como do polimixina B. Essas combinações eliminaram rapidamente tanto o MRSA em crescimento ativo quanto as células persister difíceis de matar, ao passo que os fármacos isolados frequentemente deixavam sobreviventes. Simulações computacionais sugeriram uma razão: a CC pode formar complexos compactos com o polimixina B que se inserem na membrana e a deformam mais fortemente do que cada molécula isolada, criando distorções profundas e amplas na camada lipídica. Isso ajuda outros antibióticos a atravessarem a barreira da membrana e alcançarem seus alvos com mais eficiência.
Do prato de Petri aos animais vivos
De forma encorajadora, os efeitos antibacterianos e potencializadores da CC extrapolaram o tubo de ensaio. Em pequenos vermes e em larvas de traça-da-cera infectadas com MRSA, a CC melhorou a sobrevivência. Em um modelo de infecção no músculo da coxa de camundongos com uma cepa virulenta de MRSA, a CC sozinha reduziu a contagem bacteriana, e sua combinação com gentamicina diminuiu a carga bacteriana em cerca de mil vezes em comparação com controles não tratados. Medições no sangue mostraram que níveis de droga semelhantes aos eficazes em laboratório puderam ser alcançados em camundongos sem danos óbvios ao fígado, rins ou coração ao longo do experimento.
O que isso pode significar para tratamentos futuros
Em termos simples, este trabalho revela que um medicamento para pressão arterial usado há muito tempo pode também funcionar como uma arma que mira a membrana contra o MRSA. Ao se ligar a blocos gordurosos específicos do envelope bacteriano, rigidificar a membrana e abrir buracos nela, a candesartana cilexetil tanto mata o MRSA diretamente quanto abre caminho para que antibióticos antigos voltem a ser eficazes. Embora sejam necessários mais estudos de segurança e de dosagem — especialmente porque este medicamento também age nos vasos sanguíneos humanos — os achados sugerem um atalho promissor: em vez de inventar antibióticos inteiramente novos, poderíamos reaproveitar drogas existentes para enfraquecer defesas bacterianas e restaurar o poder de tratamentos que já temos.
Citação: Tharmalingam, N., Kovacs, R.W., Scarpa de Mello, S. et al. Candesartan cilexetil disrupts methicillin-resistant Staphylococcus aureus membrane and potentiates gentamicin and polymyxin B activity. Nat Commun 17, 4012 (2026). https://doi.org/10.1038/s41467-026-70173-0
Palavras-chave: MRSA, resistência a antibióticos, reaproveitamento de fármacos, membrana bacteriana, candesartana cilexetil