Clear Sky Science · it
Il candesartan cilexetile compromette la membrana di Staphylococcus aureus resistente alla meticillina e potenzia l’attività di gentamicina e polimixina B
Trasformare una pillola per la pressione in un alleato contro i germi
Staphylococcus aureus resistente alla meticillina (MRSA) è un patogeno ostico, sia in ambiente ospedaliero sia nella comunità, che resiste a molti dei nostri migliori antibiotici. Questo studio pone una domanda sorprendente: un comune farmaco per la pressione arteriosa, il candesartan cilexetile, può essere riproposto per indebolire MRSA e rendere più efficaci gli antibiotici standard? Analizzando le cellule di MRSA da più angolazioni—chimica, genetica, immagini e modelli animali—i ricercatori mostrano come questa molecola possa compromettere le difese batteriche e ridare efficacia a farmaci più vecchi.
Perché lo Staph resistente è così difficile da trattare
MRSA causa centinaia di migliaia di infezioni gravi e migliaia di decessi ogni anno. Una ragione della sua difficoltà di trattamento è che la membrana esterna e la parete cellulare del batterio funzionano come uno scudo sofisticato. Le molecole lipidiche in questo rivestimento possono riorganizzarsi per diventare più dure, meno permeabili e più resistenti agli antibiotici tradizionali. Alcune cellule di MRSA entrano anche in stati di crescita lenta detti “persister” o si nascondono in biofilm appiccicosi, dove tollerano farmaci che normalmente ucciderebbero batteri attivi. Queste caratteristiche rendono cruciale trovare nuovi modi per attaccare la superficie batterica, piuttosto che progettare un altro antibiotico tradizionale da zero.
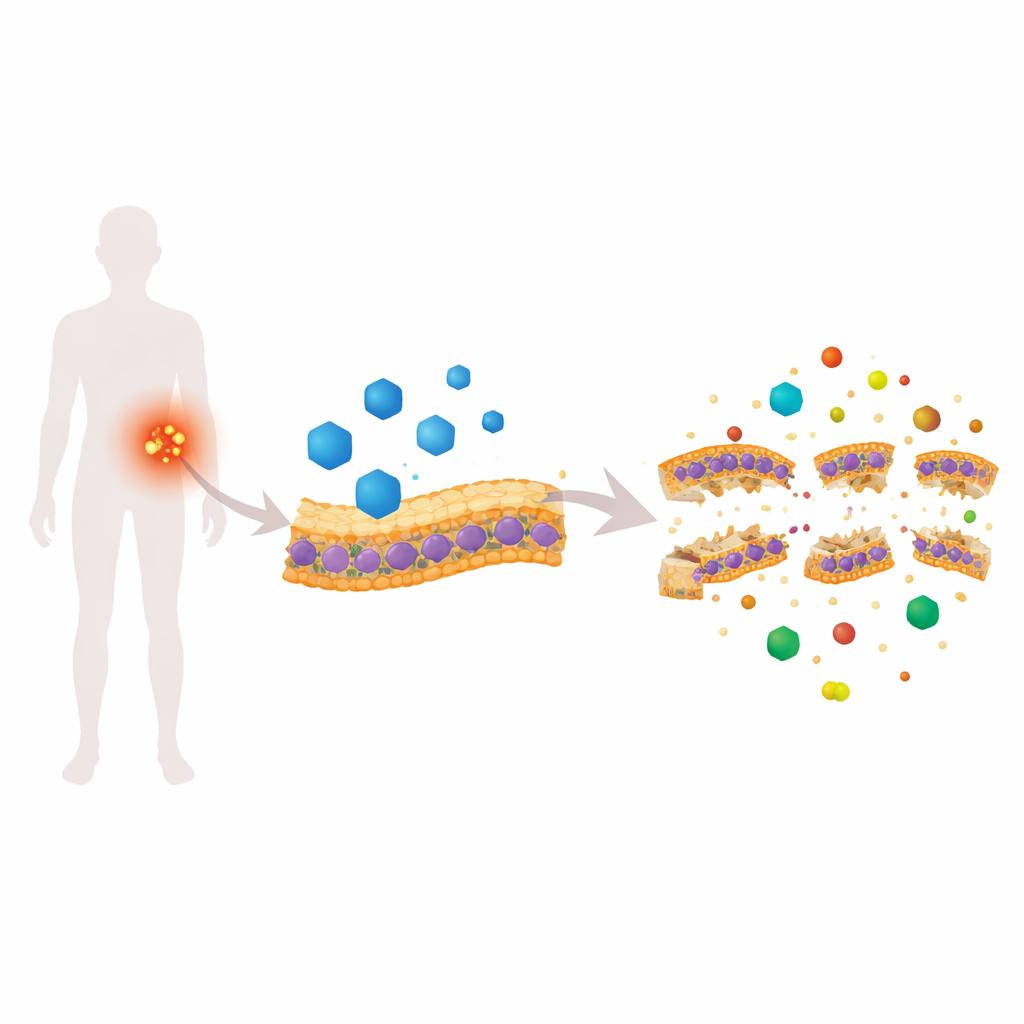
Un farmaco cardiaco che attacca la “pelle” batterica
Il candesartan cilexetile (CC) è approvato per il trattamento dell’ipertensione, ma in uno screening su vermi si è mostrato inaspettatamente attivo contro MRSA. Nei test di laboratorio, CC ha ucciso sia MRSA in fase di divisione attiva sia le più ostinate cellule in fase stazionaria, riducendo anche la formazione e la vitalità dei biofilm. Esperimenti dettagliati con coloranti fluorescenti hanno rivelato che CC rende rapidamente la membrana di MRSA permeabile, fa collassare il gradiente elettrico attraverso di essa e causa un aumento dell’alcalinità interna della cellula. Immagini ad alta risoluzione—microscopia elettronica a scansione, microscopia a forza atomica, microscopia elettronica a trasmissione e crio-tomografia 3D—mostrano superfici sfibrate, assottigliamento della membrana e gap visibili, tutti segni che la “pelle” batterica è fisicamente compromessa.
Rimodellare la chimica e il rivestimento lipidico del batterio
Per capire cosa faccia CC a livello molecolare, il team ha combinato sequenziamento dell’RNA, profilazione dei metaboliti e analisi dei lipidi. Hanno riscontrato che geni e piccole molecole coinvolti nella costruzione della parete cellulare, nella sintesi dei lipidi di membrana e nella produzione di energia risultavano generalmente downregolati dopo l’esposizione a CC, anche a dosi troppo basse per uccidere immediatamente. Diverse fosfolipidi chiave che contribuiscono a mantenere la membrana integra sono diminuiti in abbondanza. Un cambiamento notevole ha riguardato un gruppo specifico di acidi grassi lunghi a 20 atomi di carbonio (detti C20:0). Quando i ricercatori hanno usato un altro composto, la cerulenina, per depletare questi acidi grassi, MRSA è diventato meno sensibile a CC. L’aggiunta di acidi grassi C20:0 ha ripristinato gran parte dell’effetto del farmaco, e saggi di legame separati hanno mostrato un’interazione diretta di CC con lipidi legati a C20:0 e componenti superficiali correlati. Misure della “fluidità” della membrana hanno indicato che CC in realtà irrigidisce la membrana di MRSA, bloccando i lipidi in uno stato più rigido che alla fine ne compromette la funzione.
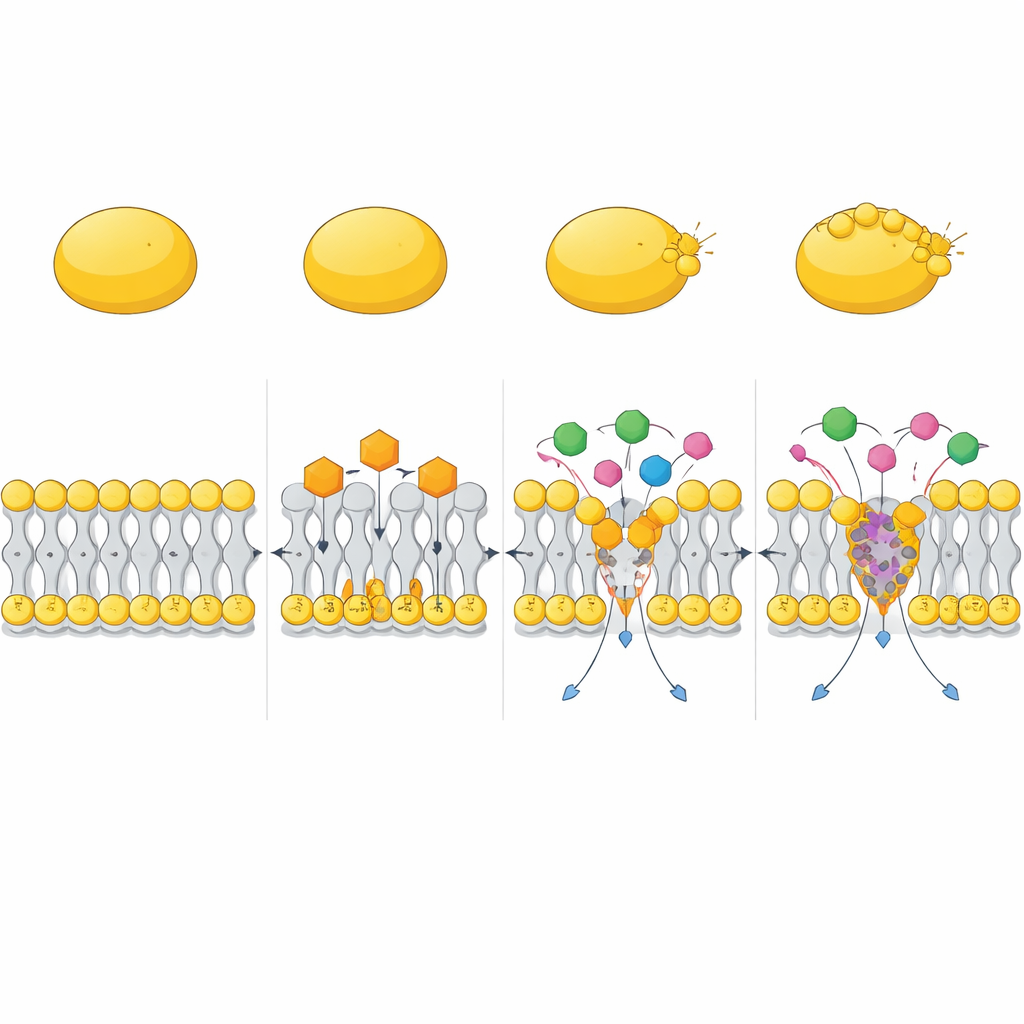
Collaborare con gli antibiotici esistenti
Lo studio ha inoltre testato il comportamento di CC in combinazione con farmaci già in uso. In esperimenti a scacchiera e di kill-curve, CC ha notevolmente potenziato l’attività di antibiotici aminoglicosidici come la gentamicina, così come della polimixina B. Queste combinazioni hanno rapidamente eliminato sia MRSA in crescita attiva sia le cellule persister difficili da uccidere, mentre i singoli farmaci spesso lasciavano sopravvissuti. Simulazioni al computer hanno suggerito una possibile ragione: CC può formare complessi compatti con la polimixina B che si inseriscono nella membrana e la deformano più intensamente di quanto faccia ciascuna molecola da sola, creando deformazioni profonde e diffuse nello strato lipidico. Questo facilita il passaggio degli altri antibiotici attraverso la barriera di membrana e il raggiungimento più efficace dei loro bersagli.
Dal piatto di Petri agli animali vivi
In modo incoraggiante, gli effetti antibatterici e potenzianti di CC si sono estesi oltre la provetta. In piccoli vermi e larve della falena della cera infettati con MRSA, CC ha migliorato la sopravvivenza. In un modello murino di infezione della coscia con un ceppo virulento di MRSA, CC da solo ha ridotto il numero di batteri, e la sua combinazione con gentamicina ha ridotto il carico batterico di circa mille volte rispetto ai controlli non trattati. Le misurazioni ematiche hanno mostrato che livelli di farmaco simili a quelli efficaci in laboratorio potevano essere raggiunti nei topi senza danni evidenti a fegato, rene o cuore nel corso dell’esperimento.
Cosa potrebbe significare per i trattamenti futuri
In termini semplici, questo lavoro rivela che un farmaco antipertensivo di lunga data può fungere anche da arma mirata alla membrana contro MRSA. Legandosi a specifici mattoni lipidici della parete batterica, irrigidendo la membrana e perforandola, il candesartan cilexetile sia uccide MRSA direttamente sia apre la strada per far funzionare di nuovo vecchi antibiotici. Pur richiedendo ulteriori studi su sicurezza e dosaggio—specialmente perché il farmaco agisce anche sui vasi sanguigni umani—i risultati suggeriscono una scorciatoia promettente: invece di inventare nuovi antibiotici ex novo, potremmo riorientare farmaci esistenti per indebolire le difese batteriche e restaurare l’efficacia di trattamenti già disponibili.
Citazione: Tharmalingam, N., Kovacs, R.W., Scarpa de Mello, S. et al. Candesartan cilexetil disrupts methicillin-resistant Staphylococcus aureus membrane and potentiates gentamicin and polymyxin B activity. Nat Commun 17, 4012 (2026). https://doi.org/10.1038/s41467-026-70173-0
Parole chiave: MRSA, resistenza agli antibiotici, riutilizzo di farmaci, membrana batterica, candesartan cilexetile