Clear Sky Science · pl
Candesartan cilexetil uszkadza błonę methycylinoopornego Staphylococcus aureus i wzmacnia działanie gentamycyny oraz polimyksyny B
Przekształcenie leku na ciśnienie w sojusznika przeciwko zarazkom
Methycylinooporny Staphylococcus aureus (MRSA) to uciążliwy szczep szpitalny i środowiskowy, który opiera się wielu naszym najlepszym antybiotykom. W tym badaniu zadano zaskakujące pytanie: czy powszechny lek na ciśnienie, candesartan cilexetil, można ponownie wykorzystać, aby osłabić MRSA i sprawić, że standardowe antybiotyki będą działać lepiej? Analizując komórki MRSA z wielu perspektyw — chemii, genetyki, obrazowania i modeli zwierzęcych — badacze pokazują, jak ten lek może naruszyć obronę bakterii i przywrócić skuteczność starszych leków.
Dlaczego oporny gronkowiec jest tak trudny do leczenia
MRSA powoduje setki tysięcy poważnych zakażeń i tysiące zgonów rocznie. Jednym z powodów trudności leczenia jest to, że zewnętrzna błona i ściana komórkowa bakterii działają jak inteligentna tarcza. Tłuszczowe cząsteczki w tej osłonie mogą zostać przegrupowane, stając się twardsze, mniej przepuszczalne i bardziej odporne na standardowe antybiotyki. Niektóre komórki MRSA wchodzą też w wolno rosnące stany „przetrwania” lub ukrywają się w lepkich biofilmach, gdzie tolerują leki, które zwykle zabijają aktywne bakterie. Te cechy sprawiają, że kluczowe jest znalezienie nowych sposobów ataku na powierzchnię bakterii, zamiast projektowania kolejnego tradycyjnego antybiotyku od podstaw.
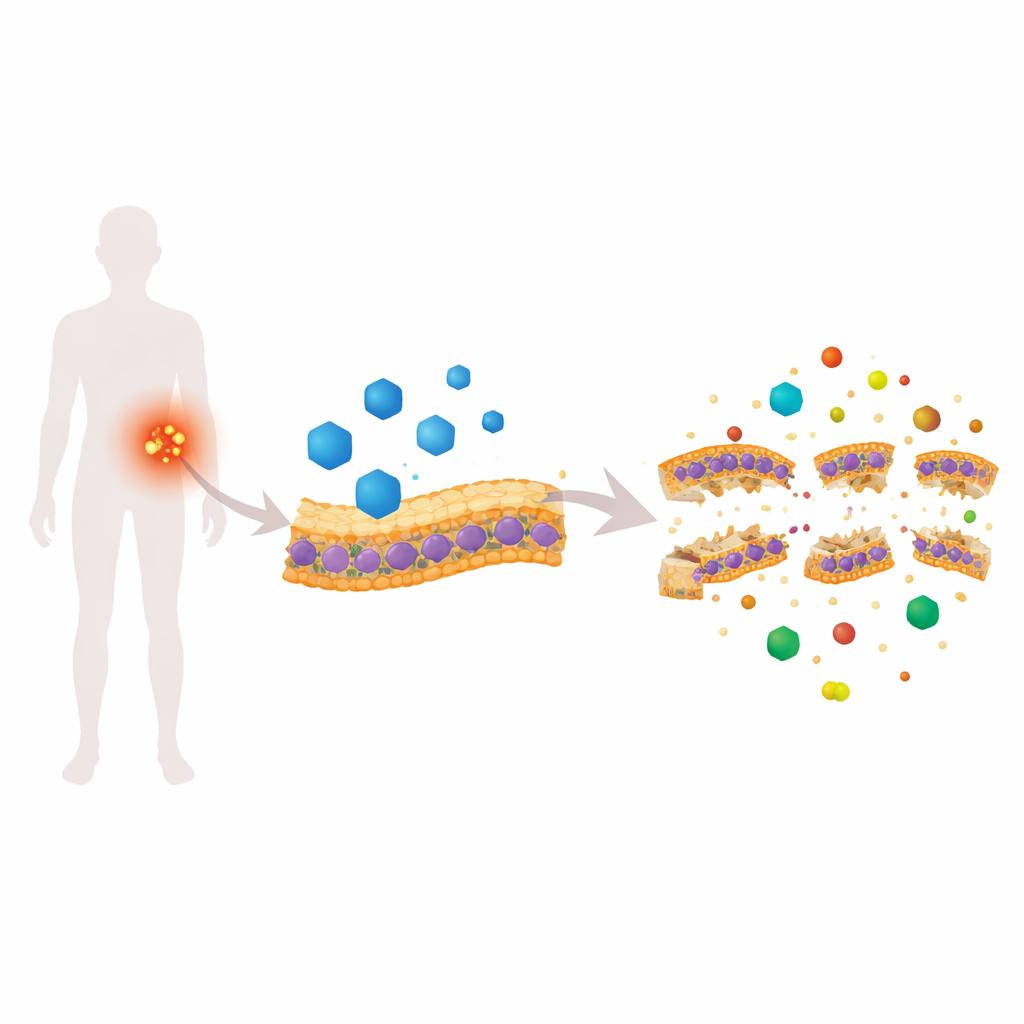
Lek sercowo-naczyniowy, który atakuje bakteryjną „skórę”
Candesartan cilexetil (CC) jest zatwierdzony do leczenia nadciśnienia, ale w przesiewowym badaniu z użyciem nicieni niespodziewanie wykazał silną aktywność przeciw MRSA. W testach laboratoryjnych CC zabijał aktywnie dzielące się komórki MRSA oraz bardziej oporne komórki w fazie stacjonarnej, a także zmniejszał tworzenie i żywotność biofilmów. Szczegółowe eksperymenty z użyciem barwników fluorescencyjnych wykazały, że CC szybko zwiększa przepuszczalność błony MRSA, zaburza gradient elektryczny przez nią oraz powoduje alkalizację wnętrza komórki. Obrazowanie wysokiej rozdzielczości — mikroskopia skaningowa elektronowa, mikroskopia sił atomowych, transmisyjna mikroskopia elektronowa i trójwymiarowa kriotomografia — ujawniło pęcherzycowe powierzchnie, przerzedzenie błony i widoczne szczeliny, czyli oznaki fizycznego naruszenia „skóry” bakterii.
Przeprogramowanie biochemii i tłuszczowej osłony bakterii
Aby zrozumieć, co robi CC „pod maską”, zespół połączył sekwencjonowanie RNA, profilowanie metabolitów i analizę lipidów. Odkryto, że geny i małe cząsteczki zaangażowane w budowę ściany komórkowej, syntezę lipidów błonowych i produkcję energii były szeroko osłabiane po ekspozycji na CC, nawet przy dawkach za niskich, by bezpośrednio zabijać. Kilka kluczowych fosfolipidów, które pomagają utrzymać integralność błony, zmniejszyło swoją obfitość. Uderzającą zmianą objęła szczególna grupa długich, 20-węglowych kwasów tłuszczowych (oznaczanych C20:0). Gdy badacze użyli innego związku, ceruleninu, by wyczerpać te kwasy tłuszczowe, MRSA stał się mniej wrażliwy na CC. Dodanie z powrotem kwasów C20:0 przywróciło dużą część działania leku, a odrębne testy wiązania wykazały bezpośrednią interakcję CC z lipidami związanymi z C20:0 i powiązanymi składnikami powierzchni. Pomiary „płynności” błony wskazały, że CC faktycznie usztywnia błonę MRSA, blokując lipidy w bardziej sztywnym stanie, co ostatecznie podważa jej funkcję.
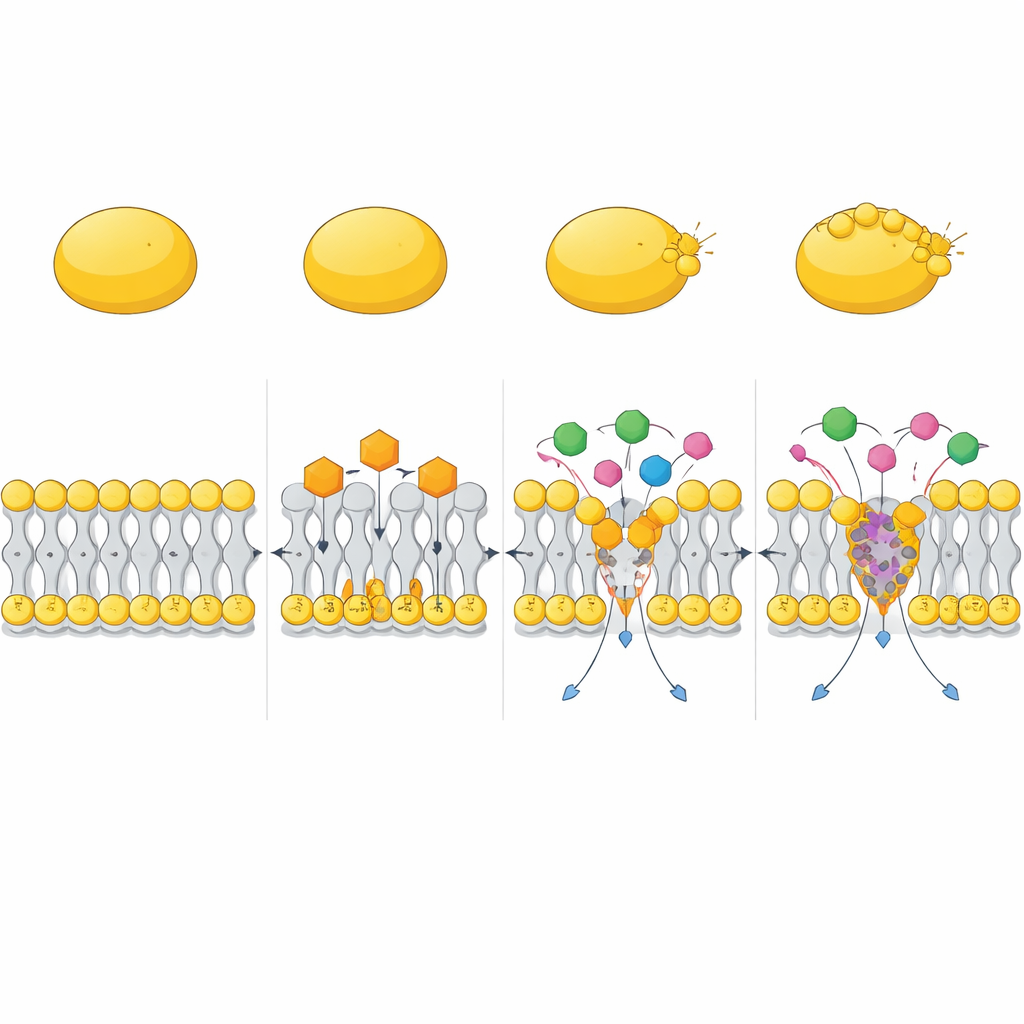
Współpraca z istniejącymi antybiotykami
Badanie sprawdziło też, jak CC zachowuje się w połączeniu z istniejącymi lekami. W eksperymentach typu checkerboard i time-kill CC znacząco zwiększał aktywność aminoglikozydowych antybiotyków, takich jak gentamycyna, oraz polimyksyny B. Te kombinacje szybko eliminowały zarówno aktywnie rosnący MRSA, jak i trudne do zabicia komórki przetrwalnikowe, podczas gdy pojedyncze leki często pozostawiały ocalałych. Symulacje komputerowe zasugerowały jedną z przyczyn: CC może tworzyć zwarte kompleksy z polimyksyną B, które wnikają w błonę i deformują ją silniej niż każda z tych cząsteczek osobno, tworząc głębokie, rozległe odkształcenia w warstwie lipidowej. To ułatwia innym antybiotykom przekraczanie bariery błonowej i szybsze docieranie do celów wewnątrz komórki.
Od płytki Petriego do żywych organizmów
Co zachęcające, antybakteryjne i wspomagające efekty CC rozszerzały się poza probówkę. U drobnych nicieni i larw ćmy woskowej zakażonych MRSA, CC poprawiał przeżywalność. W modelu zakażenia uda myszy z użyciem wirulentnego szczepu MRSA CC samodzielnie zmniejszał liczbę bakterii, a jego kombinacja z gentamycyną obniżyła obciążenie bakteryjne w przybliżeniu o tysiąc razy w porównaniu z grupami kontrolnymi. Pomiary we krwi wykazały, że stężenia leków zbliżone do tych skutecznych w laboratorium można osiągnąć u myszy bez wyraźnych uszkodzeń wątroby, nerek czy serca w czasie eksperymentu.
Co to może znaczyć dla przyszłych terapii
Mówiąc prosto, praca ta pokazuje, że długo stosowany lek na nadciśnienie może służyć także jako narzędzie celujące w błonę przeciw MRSA. Dzięki wiązaniu się z określonymi tłuszczowymi elementami budulcowymi otoczki bakteryjnej, usztywnianiu błony i tworzeniu w niej dziur, candesartan cilexetil zarówno bezpośrednio zabija MRSA, jak i otwiera drogę, by starsze antybiotyki znów były skuteczne. Chociaż potrzebne są dalsze badania nad bezpieczeństwem i dawkowaniem — zwłaszcza że lek ten działa także na naczynia krwionośne u ludzi — wyniki sugerują obiecującą drogę: zamiast wymyślać zupełnie nowe antybiotyki, możemy przerobić istniejące leki, by osłabić bakteryjne mechanizmy obronne i przywrócić siłę terapii, które już mamy.
Cytowanie: Tharmalingam, N., Kovacs, R.W., Scarpa de Mello, S. et al. Candesartan cilexetil disrupts methicillin-resistant Staphylococcus aureus membrane and potentiates gentamicin and polymyxin B activity. Nat Commun 17, 4012 (2026). https://doi.org/10.1038/s41467-026-70173-0
Słowa kluczowe: MRSA, oporność na antybiotyki, ponowne zastosowanie leków, błona bakteryjna, candesartan cilexetil