Clear Sky Science · es
Candesartán cilexetilo altera la membrana de Staphylococcus aureus resistente a meticilina y potencia la actividad de la gentamicina y la polimixina B
Convertir una pastilla para la presión arterial en un aliado contra microbios
Staphylococcus aureus resistente a meticilina (MRSA) es un patógeno persistente en hospitales y comunidades que elude muchos de nuestros mejores antibióticos. Este estudio plantea una pregunta sorprendente: ¿puede un fármaco común para la hipertensión, el candesartán cilexetilo, reutilizarse para debilitar al MRSA y mejorar la eficacia de los antibióticos estándar? Al investigar las células de MRSA desde múltiples ángulos —química, genética, imagen y modelos animales— los investigadores muestran cómo esta pastilla puede perforar las defensas bacterianas y resucitar fármacos antiguos.
Por qué el Staph resistente es tan difícil de tratar
El MRSA causa cientos de miles de infecciones graves y miles de muertes cada año. Una razón por la que es tan difícil de tratar es que la membrana externa y la pared celular de la bacteria actúan como un escudo inteligente. Las moléculas grasas en este escudo pueden reorganizarse para volverse más duras, menos permeables y más resistentes a los antibióticos habituales. Algunas células de MRSA también entran en estados de crecimiento lento («persisters») o se esconden en bionfilms pegajosos, donde toleran medicamentos que normalmente matarían bacterias activas. Estas características hacen crucial encontrar nuevas formas de atacar la superficie bacteriana en lugar de diseñar otro antibiótico tradicional desde cero.
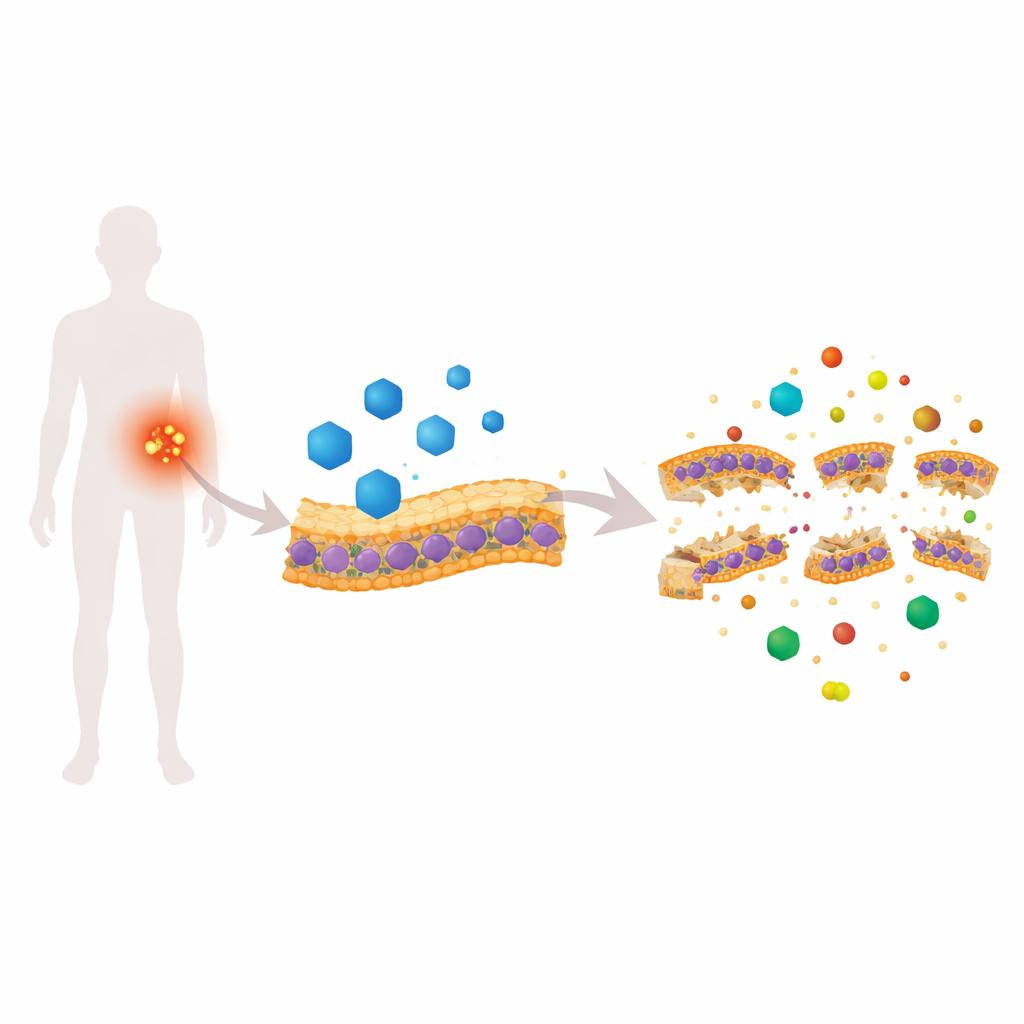
Un medicamento cardiaco que ataca la “piel” bacteriana
El candesartán cilexetilo (CC) está aprobado para tratar la hipertensión, pero en una cribado con gusanos mostró inesperadamente una fuerte actividad contra MRSA. En pruebas de laboratorio, CC mató MRSA en división activa y también las células en fase estacionaria más obstinadas, además de reducir la formación y viabilidad de biofilms. Experimentos detallados con colorantes fluorescentes revelaron que CC vuelve rápidamente la membrana de MRSA permeable, colapsa el gradiente eléctrico a través de ella y provoca que el interior celular se vuelva inusualmente alcalino. Imágenes de alta resolución —microscopía electrónica de barrido, microscopía de fuerza atómica, microscopía electrónica de transmisión y crio-tomografía 3D— mostraron superficies ampolladas, adelgazamiento de la membrana y huecos visibles, todos signos de que la “piel” bacteriana está físicamente comprometida.
Reprogramando la química y la capa grasa del microbio
Para entender qué hace CC en detalle, el equipo combinó secuenciación de ARN, perfilado de metabolitos y análisis lipídico. Encontraron que genes y pequeños metabolitos implicados en la construcción de la pared celular, la síntesis de lípidos de membrana y la generación de energía estaban ampliamente reprimidos tras la exposición a CC, incluso a dosis demasiado bajas para matar por completo. Varios fosfolípidos clave que ayudan a mantener la integridad de la membrana disminuyeron en abundancia. Un cambio notable afectó a un grupo particular de ácidos grasos largos de 20 carbonos (denominados C20:0). Cuando los investigadores usaron otro compuesto, cerulenina, para agotar estos ácidos grasos, el MRSA se volvió menos sensible a CC. Añadir de nuevo ácidos grasos C20:0 restauró gran parte del efecto del fármaco, y ensayos de unión por separado mostraron que CC interactúa directamente con lípidos enlazados a C20:0 y componentes superficiales relacionados. Mediciones de la “fluidez” de la membrana indicaron que CC en realidad endurece la membrana de MRSA, bloqueando los lípidos en un estado más rígido que finalmente socava su función.
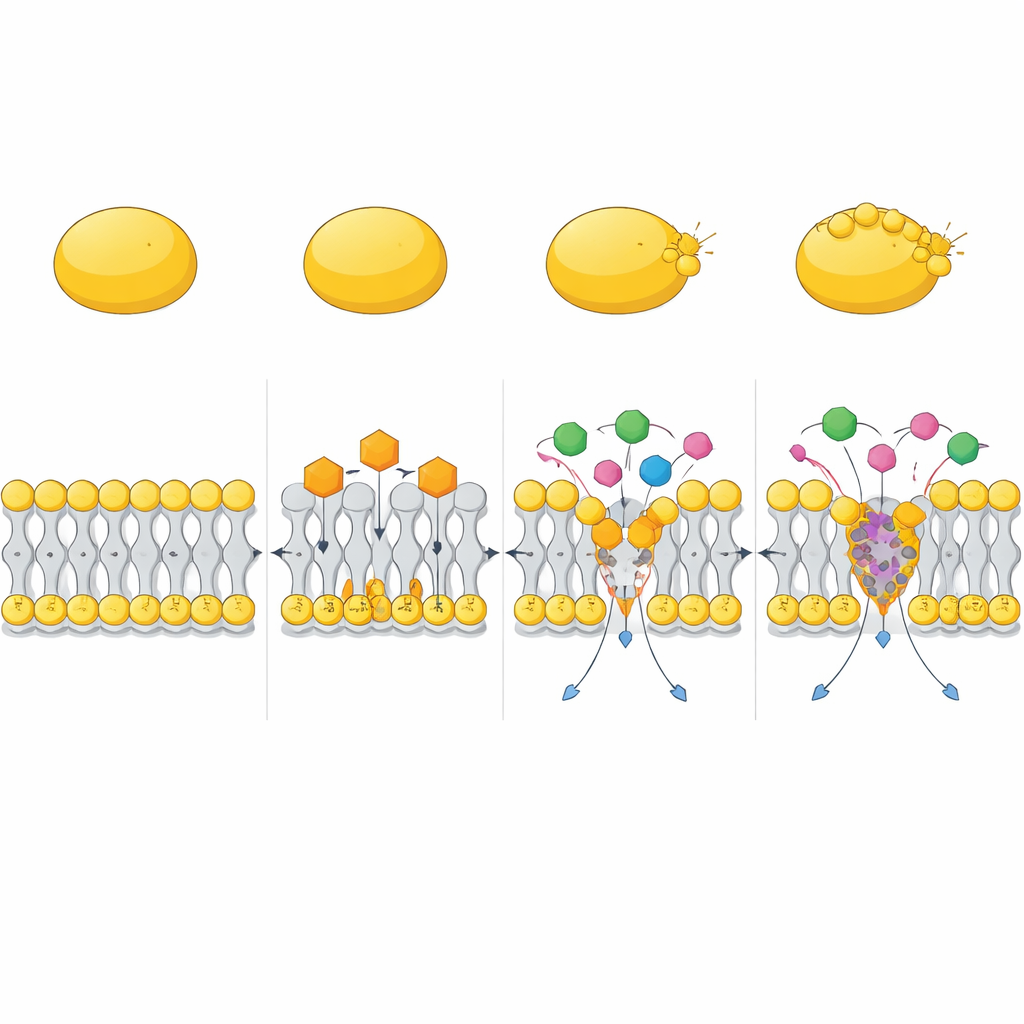
Unidos a antibióticos existentes
El estudio también evaluó cómo se comporta CC junto con fármacos ya disponibles. En experimentos de tablero de ajedrez y de reducción temporal de viabilidad, CC potenció de manera dramática la actividad de antibióticos aminoglucósidos como la gentamicina, así como de la polimixina B. Estas combinaciones eliminaron rápidamente tanto MRSA en crecimiento activo como células persister difíciles de matar, mientras que los fármacos por separado a menudo dejaban supervivientes. Simulaciones por ordenador sugirieron una razón: CC puede formar complejos compactos con la polimixina B que se insertan en la membrana y la deforman con mayor potencia que cualquiera de las moléculas por sí sola, creando deformaciones profundas y de gran alcance en la capa lipídica. Esto ayuda a que otros antibióticos atraviesen la barrera de la membrana y alcancen sus dianas con mayor eficiencia.
Del plato de Petri a animales vivos
De forma alentadora, los efectos antibacterianos y potenciadores de CC se extendieron más allá del tubo de ensayo. En pequeños gusanos y larvas de la polilla de cera infectadas con MRSA, CC mejoró la supervivencia. En un modelo murino de infección en el muslo con una cepa virulenta de MRSA, CC por sí solo redujo los recuentos bacterianos, y su combinación con gentamicina disminuyó la carga bacteriana aproximadamente mil veces en comparación con controles no tratados. Mediciones en sangre mostraron que se podían alcanzar en ratones niveles del fármaco similares a los efectivos en el laboratorio sin daños evidentes en hígado, riñón o corazón durante el curso del experimento.
Qué podría significar esto para futuros tratamientos
En términos sencillos, este trabajo revela que un fármaco para la presión arterial usado desde hace tiempo puede funcionar también como un arma dirigida a la membrana contra MRSA. Al unirse a bloques grasos específicos del envoltorio bacteriano, endurecer la membrana y perforarla, el candesartán cilexetilo tanto mata al MRSA directamente como abre la puerta para que antibióticos antiguos vuelvan a ser eficaces. Si bien se necesitan más estudios de seguridad y dosificación —especialmente porque este medicamento también actúa sobre los vasos sanguíneos humanos— los hallazgos sugieren un atajo prometedor: en lugar de inventar antibióticos completamente nuevos, podríamos reconvertir fármacos existentes para debilitar las defensas bacterianas y restaurar la potencia de los tratamientos que ya tenemos.
Cita: Tharmalingam, N., Kovacs, R.W., Scarpa de Mello, S. et al. Candesartan cilexetil disrupts methicillin-resistant Staphylococcus aureus membrane and potentiates gentamicin and polymyxin B activity. Nat Commun 17, 4012 (2026). https://doi.org/10.1038/s41467-026-70173-0
Palabras clave: MRSA, resistencia a antibióticos, reutilización de fármacos, membrana bacteriana, candesartán cilexetilo