Clear Sky Science · zh
通过不对称β‑H消除反应构建杂原子桥联的[3.2.1]环辛烷骨架的手性合成
这些小环分子为何重要
许多重要药物,尤其是作用于大脑的药物,均以一种紧凑的环状结构为核心,这种结构称为托品(tropane)。这些分子“骨架”帮助药物锁定参与阿尔茨海默病和抑郁症等疾病的靶点。然而,要以单一、优选的镜像形式(手性纯净体)来合成基于托品的候选分子,历来既缓慢又成本高、技术要求也高。本研究提出了一种更直接、更高效的策略,可由廉价起始物构建这些复杂骨架,从而加快新疗法的发现进程。
把简单起始块变成丰富的药物家族
研究人员以托品酮(一种价格低廉且已含有许多天然托品生物碱基本环布局的化合物)为出发。由该简单起始物制备出高度通用的构建单元——N‑芳磺酰肼(N-arylsulfonylhydrazones)。随后将其与各种芳基溴化物偶联——这些分子携带不同的芳香“装饰”——从而拼装出一系列N‑桥联的[3.2.1]环辛烷及相关骨架。关键进展在于该转化以显著偏好一种镜像形式进行,从而获得在药物设计中特别有价值的手性托品。
引导分子流向的定制催化剂
该方法的核心是一个量身定制的钯催化剂,与名为Ming‑Phos的手性配体配对。反应经过一个短暂且高度活泼的卡宾中间体阶段,随后发生一个微妙的步骤:从相邻碳原子上移去一个氢原子——即β‑H消除。在该体系中,有两个不同位点可能发生此消除,理论上会导致四条不同的途径。因此催化剂不仅必须控制分子哪一面参与反应(手性选择性),还要决定移去的是哪个氢。通过精心设计Ming‑Phos配体——调节其取代基并定位关键基团以便与反应伙伴形成氢键——作者创造了一个催化“口袋”,将分子引导到单一路径,从而以高产率和优异的对映纯度产出目标产物。
从反应范围到真实药物靶点
在优化条件下,该方法对芳基溴的官能团兼容性很强,既可接受电子给体与电子受体取代环、体积较大的取代基,也适用于吡啶等杂环。当桥头氮被氧替换时,方法同样适用于生成氧代托品(oxa‑tropane)类似物。研究团队还展示了这些产物并非仅为实验室趣味:他们将该反应用于构建针对阿尔茨海默病的药物高级中间体,以及能结合单胺转运蛋白(参与情绪与认知的关键蛋白)的配体。与以往需采用苛刻条件、有毒气体或繁琐手性拆分的路线相比,新策略用更少步骤、更温和的条件,并以更佳的手性控制,合成出这些靶分子。
窥探新反应的机理
为理解该过程的运作机理,作者进行了详尽的机理学研究。通过改变芳基溴反应伙伴的电子性质并测量对反应速率的影响,他们表明与芳基溴形成键的初始步骤不太可能是缓慢且决定性的步骤。同位素标记实验进一步提示β‑H消除本身并非限速步骤。相反,数据指向由磺酰肼衍生的钯‑卡宾中间体的形成为瓶颈。额外测试排除了涉及自由基的途径,并支持这样一幅图景:Ming‑Phos配体与反应伙伴之间的氢键有助于组织过渡态,从而精确控制移去哪一个β‑氢以及形成哪种镜像产物。
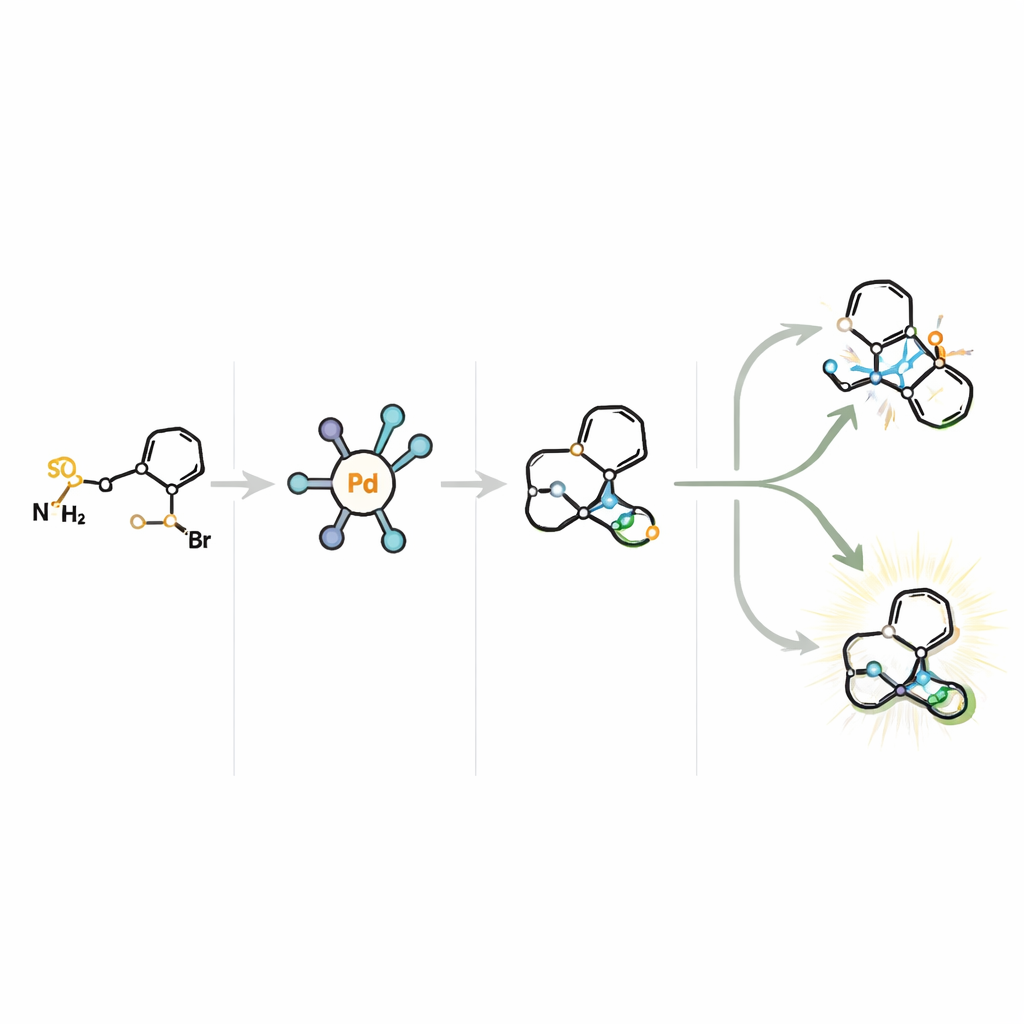
通向脑部药物及更多应用的新路线
总体而言,这项工作表明,精心设计的催化剂可以驯服一个历来难以控制的步骤,并将其转化为构建复杂分子骨架的强有力工具。通过实现从廉价原料高效、可放大且高度选择性地获得手性托品与氧代托品骨架,该方法简化了潜在阿尔茨海默药物、单胺转运体配体及其他生物活性分子的合成。对非专业读者而言,核心信息是化学家现在拥有一种更精确、更经济的方式来构建这一关键药物骨架类别,这可能加速针对脑部疾病乃至某些癌症的新疗法开发。
引用: Fang, C., Ai, J., Wang, Q. et al. Asymmetric synthesis of Heteroatom-bridged [3.2.1]Octane scaffolds via enantioselective β-H elimination reaction. Nat Commun 17, 3315 (2026). https://doi.org/10.1038/s41467-026-69960-6
关键词: 托品骨架, 不对称催化, 钯化学, 药物发现, β‑氢消除