Clear Sky Science · es
Síntesis asimétrica de andamios [3.2.1]octano puenteados por heteroátomos mediante reacción enantioselectiva de eliminación β‑H
Por qué importan estas diminutas moléculas en forma de anillo
Muchos medicamentos importantes, especialmente los que actúan en el cerebro, se construyen alrededor de una estructura compacta en forma de anillo denominada tropano. Estos “esqueletos” moleculares facilitan que los fármacos se fijen a dianas implicadas en enfermedades como el Alzheimer y la depresión. Sin embargo, obtener candidatos farmacológicos basados en tropanos en una sola forma preferida de imagen especular ha sido lento, caro y técnicamente exigente. Este estudio presenta una vía más directa y eficiente para construir estos complejos entramados a partir de un material de partida barato, lo que abre la puerta a un descubrimiento más rápido de nuevos tratamientos.
Convertir un bloque de partida sencillo en una amplia familia de fármacos
Los investigadores parten de tropinona, un compuesto económico que ya contiene el diseño básico de anillos presente en muchos alcaloides naturales tropánicos. A partir de este bloque se transforma en unidades de construcción muy versátiles denominadas N‑arilsulfonilhidrazonas. Éstas se acoplan luego con una amplia gama de bromuros arílicos—moléculas que llevan distintas “decoraciones” aromáticas—para ensamblar una familia extensa de andamios N‑puenteados [3.2.1]octano y análogos relacionados. El avance clave es que esta transformación ocurre favoreciendo de forma marcada una de las formas especulares sobre la otra, proporcionando acceso a tropanos quirales que son particularmente valiosos en el diseño de fármacos.
Un catalizador diseñado que dirige el tráfico molecular
En el corazón del método está un catalizador de paladio hecho a medida, asociado a un ligando quiral llamado Ming‑Phos. La reacción progresa a través de una etapa de carbene de vida corta y altamente reactiva seguida por un paso sutil en el que se extrae un átomo de hidrógeno de un carbono vecino—conocido como eliminación β‑H. En este sistema, dos sitios distintos pueden sufrir esta eliminación, lo que en principio conduciría a cuatro rutas diferentes. Por tanto, el catalizador debe controlar no solo cuál cara de la molécula reacciona (su quiralidad) sino también qué hidrógeno se elimina. Al diseñar cuidadosamente el ligando Ming‑Phos—ajustando sus sustituyentes y posicionando grupos clave para que puedan formar un enlace de hidrógeno con la pareja reactiva—los autores crean una “bolsita” catalítica que guía la molécula por una única ruta favorecida, entregando productos con altos rendimientos y excelente pureza enantiomérica.
Del alcance de la reacción a dianas medicinales reales
Bajo condiciones optimizadas, el método tolera una amplia variedad de grupos funcionales en los bromuros arílicos, incluidos anillos ricos y pobres en electrones, sustituyentes voluminosos y heterociclos como las piridinas. También funciona cuando el nitrógeno en la cabeza del puente se sustituye por oxígeno, dando análogos oxa‑tropánicos. El equipo demuestra que estos productos no son meras curiosidades de laboratorio: adaptan la reacción para construir intermedios avanzados para fármacos dirigidos al tratamiento del Alzheimer y para ligandos que se unen a transportadores de monoaminas, proteínas clave implicadas en el estado de ánimo y la cognición. En comparación con rutas anteriores que requerían condiciones duras, gases tóxicos o resoluciones quirales laboriosas, la nueva estrategia obtiene estas dianas en menos pasos, en condiciones más suaves y con mucho mejor control de la quiralidad molecular.
Mirando bajo el capó de la nueva reacción
Para entender cómo funciona el proceso, los autores realizan estudios mecanísticos detallados. Variando la naturaleza electrónica de los bromuros arílicos y midiendo cómo esto afecta a las velocidades de reacción, muestran que el paso inicial de formación del enlace con el bromuro arílico probablemente no sea el paso lento y determinante. Experimentos de marcado isotópico sugieren además que la eliminación β‑H en sí no es la etapa limitante de la velocidad. En cambio, los datos apuntan a la formación del intermedio paladio‑carbene, derivado de la sulfonilhidrazona, como el cuello de botella. Pruebas adicionales descartan una vía que involucre radicales libres y apoyan una imagen en la que la formación de enlaces de hidrógeno entre el ligando Ming‑Phos y la pareja reactiva ayuda a organizar el estado de transición, conduciendo a un control preciso sobre qué hidrógeno β se elimina y qué producto enantiomérico se forma.
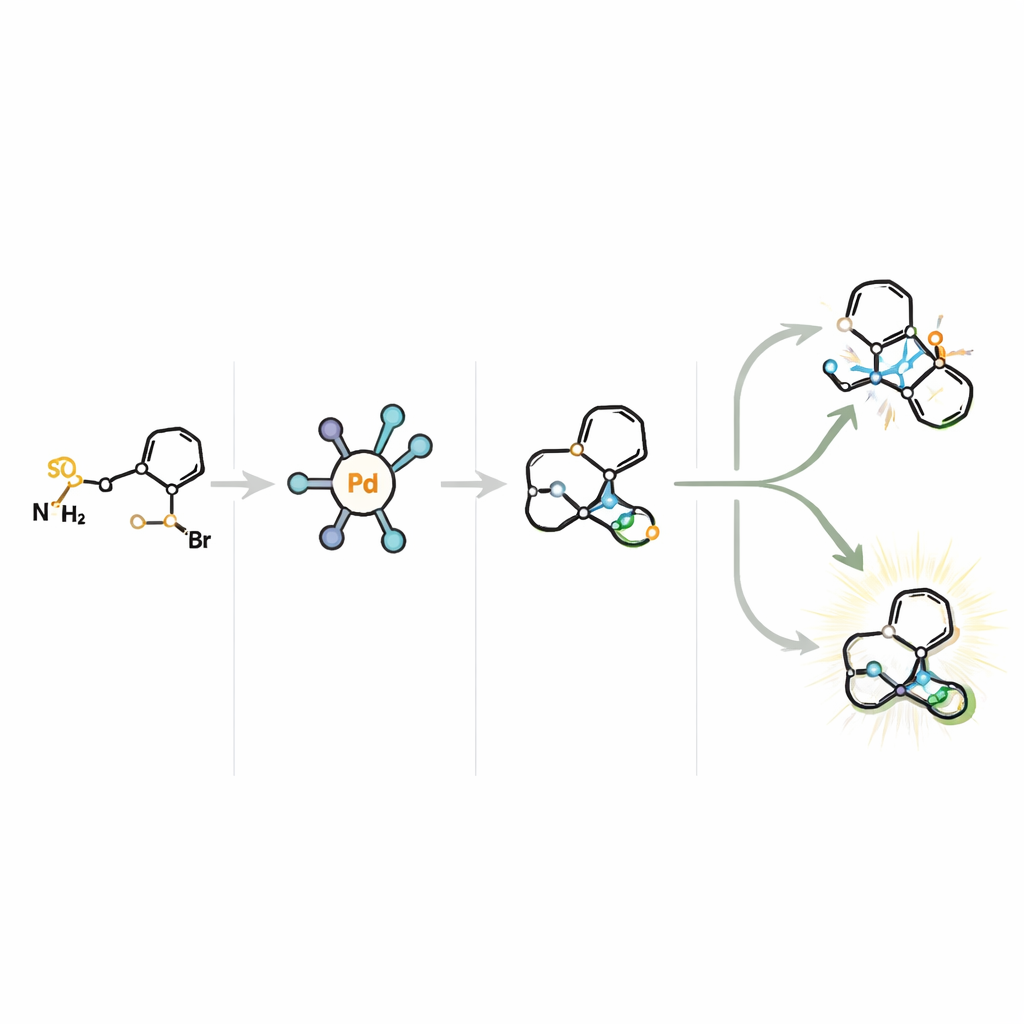
Nuevas rutas hacia fármacos cerebrales y más allá
En conjunto, este trabajo muestra que un catalizador cuidadosamente diseñado puede domesticar un paso notoriamente difícil de controlar y convertirlo en una herramienta poderosa para construir entramados moleculares intrincados. Al permitir un acceso eficiente, escalable y altamente selectivo a andamios tropánicos y oxa‑tropánicos quirales a partir de una materia prima económica, el método agiliza la síntesis de posibles fármacos contra el Alzheimer, ligandos de transportadores de monoaminas y otras moléculas bioactivas. Para los no especialistas, el mensaje clave es que los químicos disponen ahora de una manera más precisa y económica de construir una clase crucial de esqueletos farmacológicos, lo que podría acelerar el desarrollo de nuevos tratamientos para trastornos cerebrales y, posiblemente, el cáncer.
Cita: Fang, C., Ai, J., Wang, Q. et al. Asymmetric synthesis of Heteroatom-bridged [3.2.1]Octane scaffolds via enantioselective β-H elimination reaction. Nat Commun 17, 3315 (2026). https://doi.org/10.1038/s41467-026-69960-6
Palabras clave: andamios tropánicos, catálisis enantioselectiva, química del paladio, descubrimiento de fármacos, eliminación de hidrógeno beta