Clear Sky Science · he
סינתזה אסימטרית של שלדיים [3.2.1]אוקטאן מחוברים על ידי הטרואטום באמצעות תגובת β‑H אלימינציה אננטיוסלקטיבית
מדוע מולקולות מעגליות זעירות אלה חשובות
תרופות רבות חשובות, ובמיוחד אלו הפועלות על המוח, מבוססות על מבנה קומפקטי בצורת טבעת המכונה טראופאן. ה"שלדים" המולקולריים האלה מסייעים לתרופות להיקשר למטרות המעורבות במחלות כגון אלצהיימר ודיכאון. עם זאת, הכנת מועמדי תרופות מבוססי טראופאן בצורתם האנטרי־מועדפת נשארה איטית, יקרה ומאתגרת טכנית. מחקר זה מציג דרך ישירה ויעילה יותר לבנות את המסגרות המורכבות הללו מחומר מוצא זול, ובכך פותח דלת לגילוי מהיר יותר של טיפולים חדשים.
הפיכת קוביית בניין פשוטה למשפחה עשירה של תרופות
החוקרים מתחילים מטורפינון, תרכובת זולה שכבר כוללת את פריסת הטבעת הבסיסית הנמצאת ברבים מאלקלואידים הטראופאן הטבעיים. מתוך בלוק בניין פשוט זה הם ממירים אותו ליחידות בנייה רב‑שימושיות הנקראות N‑arylsulfonylhydrazones. אלה משולבות לאחר מכן עם טווח רחב של אריל ברומידים — מולקולות הנושאות "קישוטים" ארומטיים שונים — כדי להרכיב משפחה רחבה של שלדיים N‑מחוברים [3.2.1]אוקטאן ושלדיים קרובים. ההתקדמות המרכזית היא שהטרנספורמציה מתרחשת באופן שמעדיף בחוזקה צורת מראה אחת על פני השנייה, ומאפשרת גישה לטראופאנים כירליים בעלי ערך רב בעיצוב תרופות.
קטליזטור בעיצוב מיוחד שמנווט תנועה מולקולרית
בלב השיטה עומד קטליזטור פלדיום מעוצב יחד עם ליגנד כירלי שנקרא Ming‑Phos. התגובה מתקדמת דרך שלב קרבני קצר‑חיי וריאקטיבי למדי ואחריו שלב עדין שבו מוסר אטום מימן מפחמן סמוך — תהליך הידוע כאלימינציית β‑H. במערכת זו שני אתרים מובחנים יכולים לעבור אלימינציה זו, מה שמוביל עקרונית לארבעה מסלולים שונים. הקטליזטור חייב לכן לשלוט לא רק באיזו פאה של המולקולה מגיבה (הידית שלה) אלא גם איזה מימן מוסר. על ידי עיצוב מדוקדק של ליגנד Ming‑Phos — כוונון הסובסיטואנטים שלו ומיקום קבוצות מפתח כך שיוכלו ליצור קשר מימן עם השותף המגיב — המחברים יוצרים "כיס" קטליטי שמנחה את המולקולה לאורך מסלול מועדף בודד, ומניב תוצרים בתשואה גבוהה ובטוהר אננטיומרי מצוין.
ממאגר התגובה למטרות תרופתיות ממשיות
בתנאים מותאמים, השיטה סובלת טווח רחב של קבוצות פונקציונליות על האריל ברומידים, כולל טבעות עשירות ועניות באלקטרונים, סובסיטואנטים מסיביים והטרו‑טבעות כגון פירידינים. היא עובדת גם כאשר החנקן בגרעין הגשר מוחלף בחמצן, ומייצרת אנלוגים אוקסה‑טראופאן. הצוות מדגים שהתוצרים הללו אינם סתם סקרניזמים מעבדתיים: הם מתאימים את התגובה לבניית מתווכים מתקדמים לתרופות שמיועדות לטיפול במחלת אלצהיימר ולליגנדים שמקשרים למוביליות מונואמינים, חלבונים מפתח המעורבים במצב הרוח ובקוגניציה. בהשוואה לנתיבים ישנים שדרשו תנאים קשים, גזים רעילים או הפרדות כירליות מתישות, האסטרטגיה החדשה מספקת את המטרות הללו במספר שלבים מופחת, בתנאים מתונים יותר ובבקרה טובה יותר על הידיות המולקולריות.
הצצה לתוך מנגנון התגובה החדש
כדי להבין כיצד התהליך פועל, המחברים מבצעים מחקרים מכניסטיים מפורטים. על‑ידי שינוי האופי האלקטרוני של שותפי האריל ברומיד ומדידת ההשפעה על קצבי התגובה, הם מראים שהצעד הראשוני של יצירת הקשר עם האריל ברומיד ככל הנראה אינו הצעד האיטי והקובע. ניסויי תיוג איזוטופי מרמזים עוד שהאלימינציית β‑H עצמה אינה הצעד הקובע בקצב. במקום זאת, הנתונים מצביעים על יצירת הביניים פלדיום‑קרבין, הנגזר מהסולפואיל-הידרהזון, כמחסום. מבחנים נוספים שוללים מסלול הכולל רדיקלים חופשיים ותומכים בתמונה שבה קישור מימן בין ליגנד Ming‑Phos לשותף המגיב מסייע לארגן את מצב המעבר, מה שמוביל לשליטה מדויקת באיזה מימן‑β מוסר ואיזה תוצר מראה‑יד נוצר.
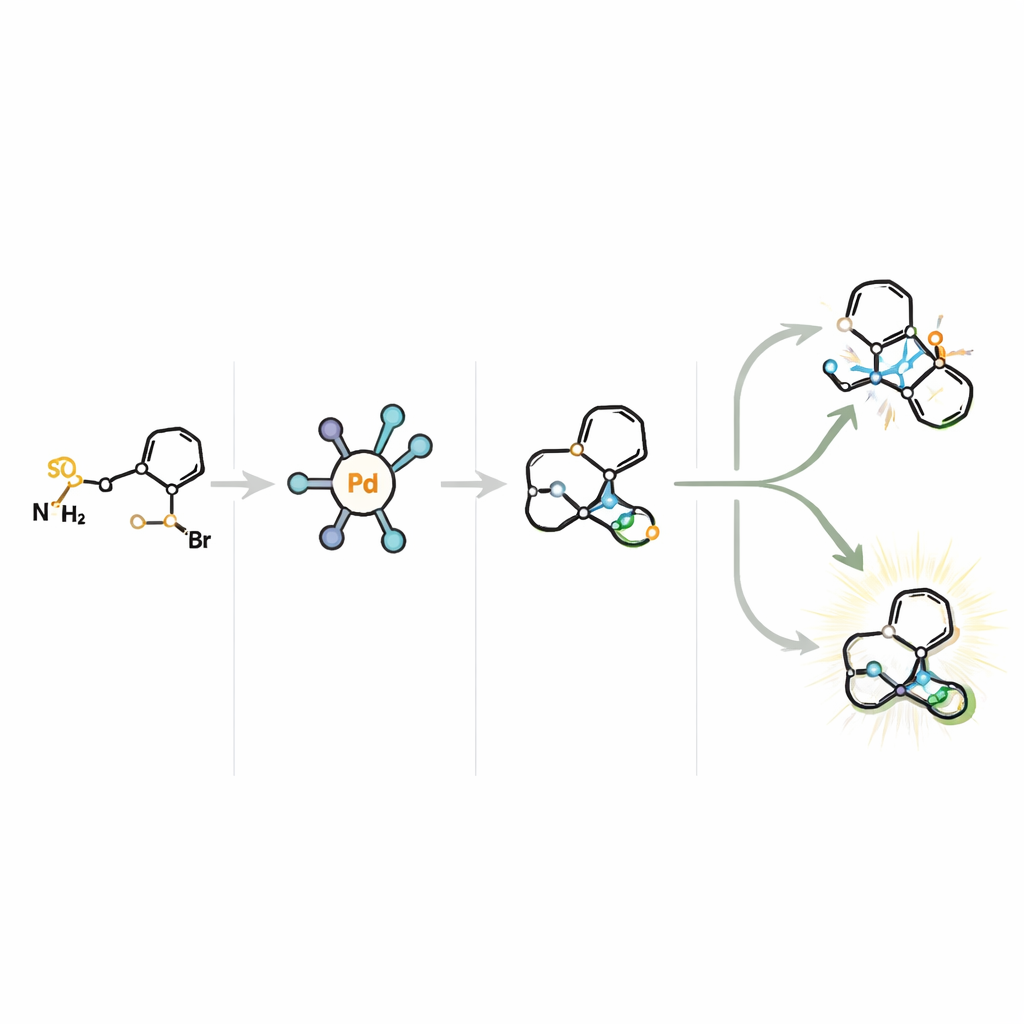
דרכים חדשות לתרופות מוח ומעבר להן
בסך הכל, עבודה זו מראה שקטליזטור המעוצב בקפידה יכול לאלף צעד שקשה בדרך כלל לשלוט בו ולהפוך אותו לכלי חזק לבניית מסגרות מולקולריות מסובכות. על ידי אספקת גישה יעילה, מדרגית ובחירתית מאוד לשלדי טראופאן וכאלו אוקסה‑טראופאן כירליים מחומר גלם זול, השיטה מפשטת את הסינתזה של תרופות פוטנציאליות לאלצהיימר, ליגנדים של מובילי מונואמינים ומולקולות ביואקטיביות אחרות. עבור קוראים שאינם מומחים, המסר המרכזי הוא שכימאים יש כיום דרך מדויקת וחסכונית יותר לבנות מעמד מכריע של גבישי תרופות, דבר שעשוי להאיץ את פיתוחם של טיפולים חדשים להפרעות מוחיות ולפוטנציאל גם לסרטן.
ציטוט: Fang, C., Ai, J., Wang, Q. et al. Asymmetric synthesis of Heteroatom-bridged [3.2.1]Octane scaffolds via enantioselective β-H elimination reaction. Nat Commun 17, 3315 (2026). https://doi.org/10.1038/s41467-026-69960-6
מילות מפתח: שלדיים טראופניים, קטליזה אננטיוסלקטיבית, כימיית פלדיום, גילוי תרופות, אלימינציית מימן‑בטא