Clear Sky Science · pt
Síntese assimétrica de esqueletos [3.2.1]octano bridged por heteroátomos via reação enantioseletiva de eliminação β-H
Por que essas pequenas moléculas em forma de anel importam
Muitos medicamentos importantes, especialmente os que atuam no cérebro, são construídos em torno de uma estrutura compacta em forma de anel chamada tropano. Esses “esqueletos” moleculares ajudam os fármacos a se ligarem a alvos envolvidos em doenças como Alzheimer e depressão. Ainda assim, produzir candidatos a fármacos baseados em tropano em uma única forma preferencial de imagem especular tem sido lento, caro e tecnicamente exigente. Este estudo apresenta uma forma mais direta e eficiente de construir esses frameworks complexos a partir de um material de partida barato, abrindo caminho para uma descoberta mais rápida de novos tratamentos.
Transformando um bloco de partida simples em uma família rica de fármacos
Os pesquisadores partem da tropinona, um composto econômico que já contém o arranjo básico de anel encontrado em muitos alcaloides naturais tropanos. A partir desse bloco de partida simples, eles o convertem em unidades de construção altamente versáteis chamadas N-arilsulfonilhidrazonas. Estas são então acopladas a uma ampla variedade de brometos arílicos — moléculas que carregam diferentes “decorações” aromáticas — para montar uma família extensa de esqueletos N-bridged [3.2.1]octano e estruturas relacionadas. O avanço chave é que essa transformação ocorre de forma a favorecer fortemente uma das imagens especulares em detrimento da outra, fornecendo acesso a tropanos quirais particularmente valiosos no desenho de fármacos.
Um catalisador sob medida que direciona o tráfego molecular
No cerne do método está um catalisador de paládio feito sob medida emparelhado com um ligante quiral chamado Ming-Phos. A reação prossegue através de um estágio carbeno de vida curta e altamente reativo, seguido por um passo sutil no qual um átomo de hidrogênio é removido de um átomo de carbono vizinho — conhecido como eliminação β‑H. Neste sistema, dois sítios distintos podem sofrer essa eliminação, levando em princípio a quatro caminhos diferentes. O catalisador deve, portanto, controlar não apenas qual face da molécula reage (sua quiralidade) mas também qual hidrogênio é removido. Ao moldar cuidadosamente o ligante Ming-Phos — ajustando seus substituintes e posicionando grupos-chave para que possam formar uma ligação de hidrogênio com o parceiro reativo — os autores criam um “bolsão” catalítico que guia a molécula ao longo de uma única rota favorecida, entregando produtos em alto rendimento e excelente pureza enantiomérica.
Do escopo da reação a alvos medicinais reais
Em condições otimizadas, o método tolera uma ampla gama de grupos funcionais nos brometos arílicos, incluindo anéis ricos e pobres em elétrons, substituintes volumosos e heterociclos como piridinas. Também funciona quando o nitrogênio da ponte é trocado por oxigênio, fornecendo análogos oxa-tropano. A equipe demonstra que esses produtos não são apenas curiosidades de laboratório: eles adaptam a reação para construir intermediários avançados para fármacos dirigidos ao tratamento da doença de Alzheimer e para ligantes que se ligam a transportadores de monoaminas, proteínas-chave envolvidas no humor e na cognição. Comparado com rotas antigas que exigiam condições severas, gases tóxicos ou resoluções quirais trabalhosas, a nova estratégia fornece esses alvos em menos etapas, sob condições mais brandas e com controle muito melhor da quiralidade molecular.
Investigando os detalhes da nova reação
Para entender como o processo funciona, os autores conduzem estudos mecanísticos detalhados. Variando a natureza eletrônica dos parceiros brometo arílico e medindo como isso afeta as velocidades de reação, eles mostram que a etapa inicial de formação de ligação com o brometo arílico provavelmente não é a etapa lenta e controladora. Experimentos de rotulagem isotópica sugerem ainda que a própria eliminação β‑H não é limitante de velocidade. Em vez disso, os dados apontam para a formação do intermediário paládio–carbeno, derivado da sulfonilhidrazona, como o gargalo. Testes adicionais descartam uma via envolvendo radicais livres e apoiam uma imagem em que a ligação de hidrogênio entre o ligante Ming-Phos e o parceiro reativo ajuda a organizar o estado de transição, levando a um controle preciso sobre qual hidrogênio β é removido e qual produto enantiomérico é formado.
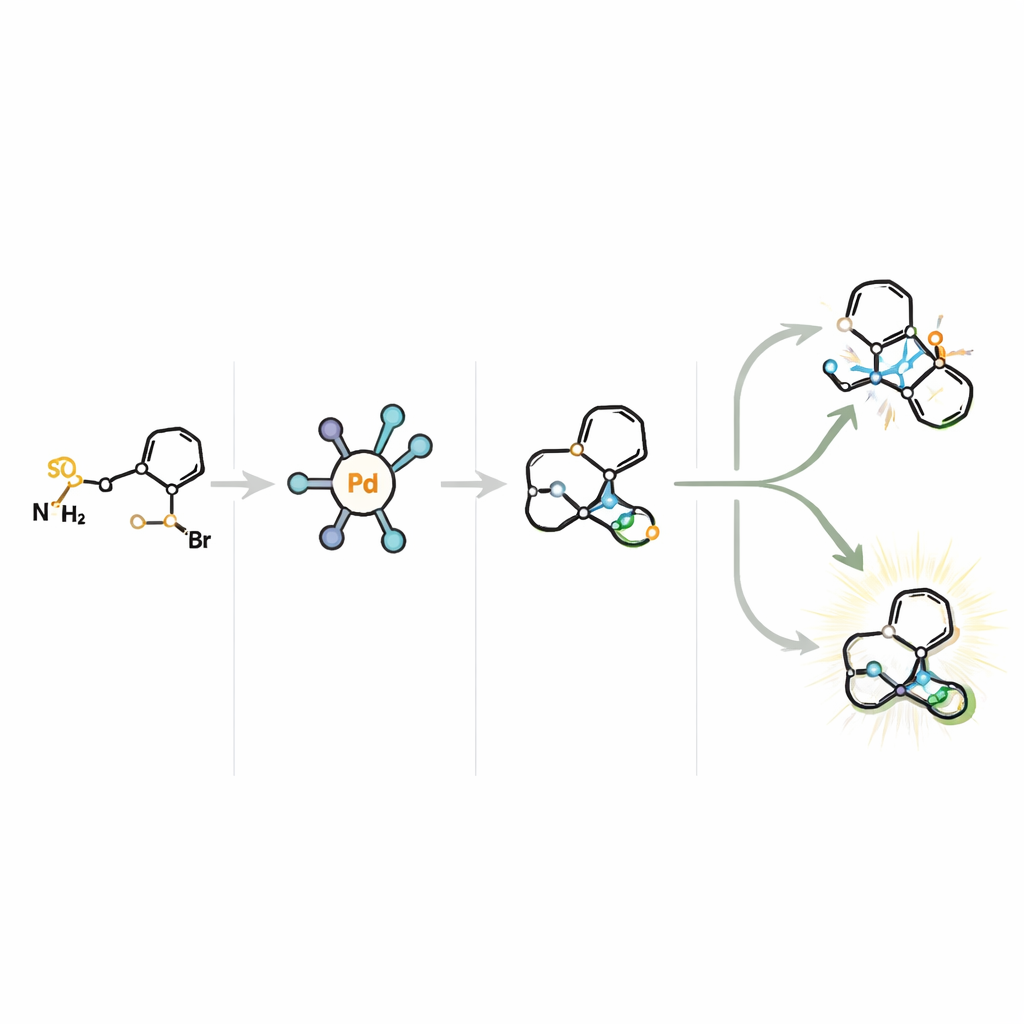
Novas rotas para fármacos cerebrais e além
No geral, este trabalho mostra que um catalisador cuidadosamente projetado pode domar um passo notoriamente difícil de controlar e transformá‑lo em uma ferramenta poderosa para construir frameworks moleculares intrincados. Ao possibilitar acesso eficiente, escalável e altamente seletivo a esqueletos tropano e oxa‑tropano quirais a partir de uma matéria-prima barata, o método simplifica a síntese de potenciais fármacos para Alzheimer, ligantes de transportadores de monoaminas e outras moléculas bioativas. Para o público não especializado, a mensagem principal é que os químicos agora dispõem de uma maneira mais precisa e econômica de construir uma classe crucial de estruturas básicas de fármacos, o que pode acelerar o desenvolvimento de novos tratamentos para transtornos cerebrais e possivelmente para câncer.
Citação: Fang, C., Ai, J., Wang, Q. et al. Asymmetric synthesis of Heteroatom-bridged [3.2.1]Octane scaffolds via enantioselective β-H elimination reaction. Nat Commun 17, 3315 (2026). https://doi.org/10.1038/s41467-026-69960-6
Palavras-chave: esqueletos tropanos, catálise enantioseletiva, química do paládio, descoberta de fármacos, eliminação de hidrogênio β