Clear Sky Science · ar
التخليق اللاتماثلي لهياكل [3.2.1] أوكتان مَجسّرة بذرات مختلفة عبر تفاعل إزالة الهيدروجين β الانتقائي لليمين واليسار
لماذا تهم هذه الجزيئات الصغيرة الحلقية
العديد من الأدوية المهمة، لا سيما تلك التي تؤثر على الدماغ، مبنية حول بنية مضغوطة حلقية تُدعى تروبان. تساعد هذه «الهياكل العظمية» الجزيئية الأدوية على الالتحام مع أهداف مرتبطة بأمراض مثل الزهايمر والاكتئاب. ومع ذلك، فإن تصنيع مرشحات دوائية مبنية على التروبان بالشكل المرآتي المفضل عادةً ما كان بطيئًا ومكلفًا ومتطلبًا تقنيًا. تعرض هذه الدراسة طريقة أكثر مباشرة وكفاءة لبناء هذه الأُطر المعقدة من مادة بداية رخيصة، ما يفتح الباب لاكتشاف أسرع لعلاجات جديدة.
تحويل بلوك بداية بسيط إلى عائلة غنية من الأدوية
يبدأ الباحثون بالتروبينون، مركب غير مكلف يحتوي بالفعل على التخطيط الحلقي الأساسي الموجود في العديد من قلويدات التروبان الطبيعية. من هذا البلوك البسيط يحولونه إلى وحدات بناء متعددة الاستخدام تعرف بـ N-arylsulfonylhydrazones. تُقترن هذه بعد ذلك بمجموعة واسعة من أريل بروميدات — جزيئات تحمل «زخارف» عطرية مختلفة — لتجميع عائلة واسعة من هياكل N-مُجَسَّرة [3.2.1] أوكتان والهياكل ذات الصلة. التقدم الرئيسي هو أن هذا التحول يحدث بطريقة تفضّل بقوة أحد الشكلين المرآيين على الآخر، ما يمنح إمكانية الوصول إلى تروبانات متمایزة إزواجياً ذات قيمة عالية في تصميم الأدوية.
محفز مُصمَّم يوجّه مسار الجزيئات
في قلب الطريقة يوجد محفز بالاديوم مُصمم خصيصًا مترافق مع لِجَند كيرالي يُسمى Ming-Phos. يتقدم التفاعل عبر مرحلة كاربين قصيرة العمر وعالية التفاعل تليها خطوة دقيقة يُزال فيها ذرة هيدروجين من ذرة كربون مجاورة — تُعرف بإزالة هيدروجين β. في هذا النظام يمكن أن يخضع موقعان مميزان لهذه الإزالة، ما يؤدي من حيث المبدأ إلى أربعة مسارات مختلفة. لذلك يجب على المحفز أن يتحكم ليس فقط في أي وجه من الجزيء يتفاعل (يديه) بل أيضًا في أي هيدروجين يُزال. من خلال تشكيل لِجَند Ming-Phos بعناية — وضبط بدائله ووضع مجموعات رئيسية بحيث تستطيع تكوين رابطة هيدروجينية مع الشريك المتفاعل — يخلق المؤلفون «جيبًا» للمحفز يوجّه الجزيء على طول مسار واحد مفضّل، موصلًا المنتجات بعائد مرتفع ونقاء إزواجي ممتاز.
من نطاق التفاعل إلى أهداف طبية حقيقية
تحت شروط محسّنة، تتحمّل الطريقة مجموعة واسعة من المجموعات الوظيفية على الأريل بروميدات، بما في ذلك الحلقات الغنية بالإلكترونات والفقيرة بها، والبدائل الضخمة، والحلقات غير المتجانسة مثل البيريدينات. كما تعمل عندما يُستبدل النيتروجين في رأس الجسر بالأكسجين، مما يعطي نظائر أوكسا‑تروبان. يبرهن الفريق أن هذه المنتجات ليست مجرد فضول مخبري: فقد عدّلوا التفاعل لبناء وسطيات متقدمة لأدوية موجهة لعلاج مرض الزهايمر ولكواشف ترتبط بناقلات المونوامين، وهي بروتينات رئيسية في المزاج والمعرفة. بالمقارنة مع الطرق الأقدم التي كانت تتطلب ظروفًا قاسية أو غازات سامة أو فصلًا إزواجيًا مرهقًا، توفر الاستراتيجية الجديدة هذه الأهداف في خطوات أقل، وبظروف ألطف، ومع تحكم أفضل بكثير في يمينية الجزيء.
نظرة تحت غطاء التفاعل الجديد
لفهم كيفية عمل العملية، أجرى المؤلفون دراسات آلية مفصّلة. من خلال تغيير الطبيعة الإلكترونية لشركاء الأريل بروميد وقياس كيفية تأثير ذلك على معدلات التفاعل، أظهروا أن خطوة تكوين الرابطة الأولية مع الأريل بروميد من غير المرجح أن تكون الخطوة البطيئة الضابطة. تقترح تجارب وسم النظائر كذلك أن إزالة هيدروجين β نفسها ليست المحدّدة للمعدل. بدلًا من ذلك، تشير البيانات إلى أن تشكيل متوسّط البالاديوم–كاربين، المشتق من السلفونيلهيدرازون، هو عنق الزجاجة. تستبعد اختبارات إضافية مسارًا يتضمن جذورًا حرة وتدعم صورة يكون فيها الترابط الهيدروجيني بين لِجَند Ming-Phos والشريك المتفاعل منظّمًا للحالة الانتقالية، مما يؤدي إلى تحكم دقيق في أي هيدروجين β يُزال وأي منتج مرايتي يتكوّن.
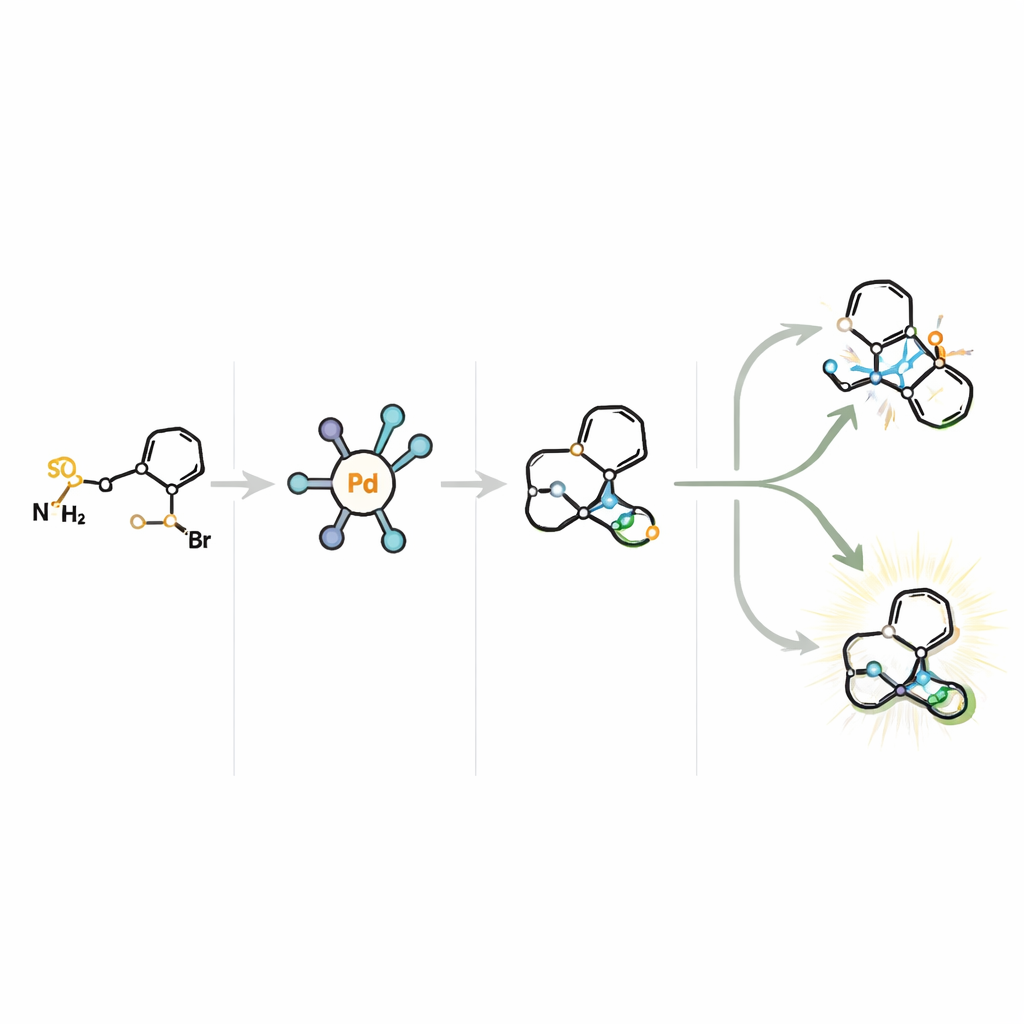
طرق جديدة لأدوية الدماغ وما بعدها
عمومًا، تُظهر هذه الدراسة أن محفزًا مُشكَّلًا بعناية يمكنه ترويض خطوة صعبة التحكم وتحويلها إلى أداة قوية لبناء أُطر جزيئية معقّدة. من خلال تمكين وصول فعال وقابل للتوسع وانتقائي جدًا إلى هياكل التروبان والأوكسا‑تروبان المتمایزة إزواجيًا من مادة خام رخيصة، تبسّط الطريقة تخليق وسطاء محتملين لأدوية الزهايمر، وموصلات ناقلات المونوامين، وغيرها من الجزيئات النشطة بيولوجيًا. للقراء غير المتخصصين، الرسالة الرئيسية هي أن الكيميائيين أصبح لديهم الآن وسيلة أكثر دقة واقتصادية لبناء فئة حاسمة من هياكل العمود الفقري الدوائي، ما قد يسرّع تطوير علاجات جديدة لاضطرابات الدماغ وربما للسرطان.
الاستشهاد: Fang, C., Ai, J., Wang, Q. et al. Asymmetric synthesis of Heteroatom-bridged [3.2.1]Octane scaffolds via enantioselective β-H elimination reaction. Nat Commun 17, 3315 (2026). https://doi.org/10.1038/s41467-026-69960-6
الكلمات المفتاحية: هياكل التروبان, التحفيز الانتقائي لليمين واليسار, كيمياء البالاديوم, اكتشاف الأدوية, إزالة هيدروجين بيتا