Clear Sky Science · de
Asymmetrische Synthese von heteroatom-überbrückten [3.2.1]Octan-Gerüsten mittels enantioselektiver β‑H‑Eliminationsreaktion
Warum diese winzigen ringförmigen Moleküle wichtig sind
Viele wichtige Medikamente, insbesondere solche, die im Gehirn wirken, basieren auf einer kompakten, ringförmigen Struktur, die als Tropan bezeichnet wird. Diese molekularen „Gerüste“ helfen Arzneistoffen, an Zielstrukturen zu binden, die an Erkrankungen wie Alzheimer und Depression beteiligt sind. Die Herstellung von tropanbasierten Wirkstoffkandidaten in einer einzigen, bevorzugten Spiegelbildform war jedoch bislang langsam, teuer und technisch anspruchsvoll. Diese Studie stellt einen direkteren und effizienteren Weg vor, diese komplexen Gerüste aus einem preiswerten Ausgangsstoff aufzubauen und ebnet damit den Weg für eine schnellere Entdeckung neuer Therapien.
Aus einem einfachen Baustein eine vielfältige Wirkstofffamilie formen
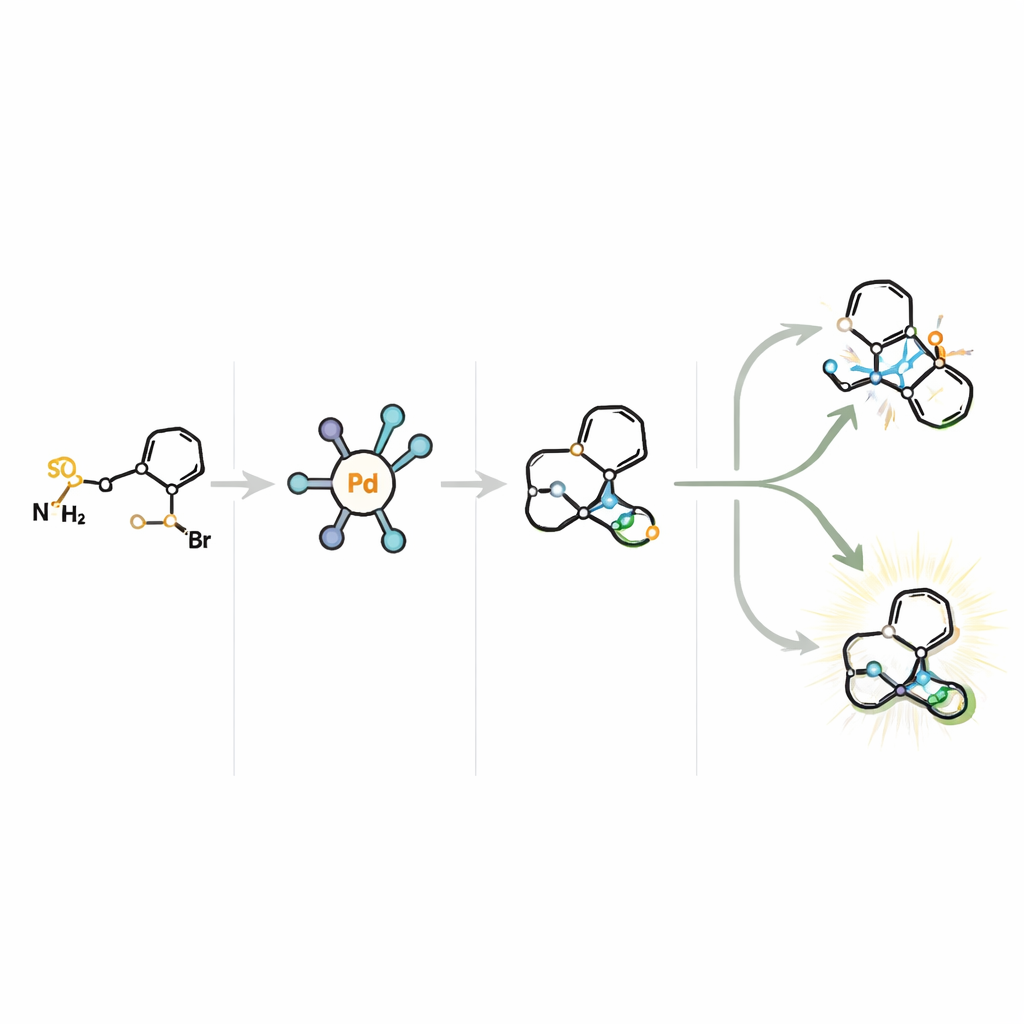
Die Forscher beginnen mit Tropinon, einer preiswerten Verbindung, die bereits das grundlegende Ringskelett enthält, wie es in vielen natürlichen Tropan-Alkaloiden vorkommt. Aus diesem einfachen Baustein wandeln sie es in hochgradig vielseitige Baueinheiten namens N‑aryl‑sulfonylhydrazone um. Diese werden dann mit einer großen Bandbreite von Aryl‑bromiden gekoppelt — Molekülen, die unterschiedliche aromatische „Dekorationen“ tragen — um eine breite Familie von N‑brückengebundenen [3.2.1]octan‑ und verwandten Gerüsten zusammenzusetzen. Der entscheidende Fortschritt besteht darin, dass diese Umwandlung so abläuft, dass eine Spiegelbildform stark bevorzugt wird, wodurch chirale Tropane zugänglich werden, die in der Wirkstoffentwicklung besonders wertvoll sind.
Ein maßgeschneiderter Katalysator, der den molekularen Verkehr lenkt
Kern der Methode ist ein speziell entwickelter Palladiumkatalysator in Kombination mit einem chiralen Liganden namens Ming‑Phos. Die Reaktion verläuft über eine kurzlebige, hochreaktive Carben‑Zwischenstufe, gefolgt von einem subtilen Schritt, in dem ein Wasserstoffatom von einem benachbarten Kohlenstoffatom entfernt wird — bekannt als β‑H‑Eliminierung. In diesem System können prinzipiell zwei unterschiedliche Positionen diese Eliminierung durchlaufen, was zu vier verschiedenen Wegen führen würde. Der Katalysator muss daher nicht nur steuern, welche Seite des Moleküls reagiert (seine Händigkeit), sondern auch, welcher Wasserstoff entfernt wird. Durch die sorgfältige Gestaltung des Ming‑Phos‑Liganden — das Abstimmen seiner Substituenten und das Positionieren von Schlüsselgruppen so, dass sie eine Wasserstoffbrücke zum reagierenden Partner bilden können — schaffen die Autoren eine Katalysator‑„Tasche“, die das Molekül entlang eines einzigen bevorzugten Pfades führt und Produkte in hohen Erträgen und ausgezeichneter enantiomerischer Reinheit liefert.
Vom Reaktionsumfang zu realen medizinischen Zielen
Unter optimierten Bedingungen toleriert die Methode eine breite Palette funktioneller Gruppen an den Aryl‑bromiden, einschließlich elektronreicher und elektronärmerer Ringe, sperriger Substituenten und Heterocyclen wie Pyridinen. Sie funktioniert auch, wenn das Brückenkopf‑Stickstoffatom durch Sauerstoff ersetzt wird und so Oxa‑Tropan‑Analoga liefert. Das Team zeigt, dass diese Produkte keine bloßen Laborneugierde sind: Sie passen die Reaktion an, um fortgeschrittene Zwischenprodukte für Arzneimittel gegen Alzheimer und für Liganden zu synthetisieren, die an Monoamintransporter binden — zentrale Proteine, die an Stimmung und Kognition beteiligt sind. Verglichen mit älteren Wegen, die harte Bedingungen, toxische Gase oder aufwändige chirale Auftrennungen erforderten, liefert die neue Strategie diese Zielverbindungen in weniger Schritten, unter milderen Bedingungen und mit deutlich besserer Kontrolle der molekularen Händigkeit.
Ein Blick unter die Motorhaube der neuen Reaktion
Um zu verstehen, wie der Prozess funktioniert, führen die Autoren detaillierte mechanistische Studien durch. Durch Variation des elektronischen Charakters der Aryl‑bromid‑Partner und Messung der Auswirkungen auf die Reaktionsraten zeigen sie, dass der initiale Bindungsbildungs‑Schritt mit dem Aryl‑bromid wahrscheinlich nicht der langsame, bestimmende Schritt ist. Isotopenmarkierungs‑Experimente deuten weiter darauf hin, dass die β‑H‑Eliminierung selbst nicht geschwindigkeitsbestimmend ist. Stattdessen deuten die Daten darauf hin, dass die Bildung des Palladium–Carben‑Intermediats, das aus dem Sulfonylhydrazon entsteht, der Engpass ist. Zusätzliche Tests schließen einen Weg über freie Radikale aus und unterstützen ein Bild, in dem Wasserstoffbrücken zwischen dem Ming‑Phos‑Liganden und dem reagierenden Partner helfen, den Übergangszustand zu organisieren und so eine präzise Kontrolle darüber ermöglichen, welcher β‑Wasserstoff entfernt und welches Spiegelbildprodukt gebildet wird.
Neue Wege zu Gehirnmedikamenten und darüber hinaus
Insgesamt zeigt diese Arbeit, dass ein sorgfältig gestalteter Katalysator einen berüchtigt schwer zu kontrollierenden Schritt zähmen und in ein leistungsfähiges Werkzeug zum Aufbau komplexer molekularer Gerüste verwandeln kann. Indem er einen effizienten, skalierbaren und hochselektiven Zugang zu chiralen Tropan‑ und Oxa‑Tropan‑Gerüsten aus einem preiswerten Rohstoff ermöglicht, vereinfacht die Methode die Synthese potenzieller Alzheimer‑Medikamente, Monoamintransporter‑Liganden und anderer bioaktiver Moleküle. Für Nicht‑Spezialisten lautet die Kernbotschaft: Chemiker verfügen nun über eine präzisere und wirtschaftlichere Möglichkeit, eine entscheidende Klasse von Arzneistoff‑Rückgraten zu konstruieren, was die Entwicklung neuer Behandlungen für Hirnerkrankungen und möglicherweise auch Krebs beschleunigen könnte.
Zitation: Fang, C., Ai, J., Wang, Q. et al. Asymmetric synthesis of Heteroatom-bridged [3.2.1]Octane scaffolds via enantioselective β-H elimination reaction. Nat Commun 17, 3315 (2026). https://doi.org/10.1038/s41467-026-69960-6
Schlüsselwörter: Tropan-Gerüste, enantioselektive Katalyse, Palladium-Chemie, Wirkstoffforschung, Beta-Wasserstoff‑Eliminierung