Clear Sky Science · it
Sintesi asimmetrica di impalcature eteroatomo-bridged [3.2.1]octano tramite reazione enantioselettiva di eliminazione β‑H
Perché queste piccole molecole ad anello contano
Molti farmaci importanti, in particolare quelli che agiscono sul cervello, si basano su una struttura compatta ad anello chiamata tropano. Questi “scheletri” molecolari aiutano i farmaci ad agganciarsi a bersagli coinvolti in malattie come l’Alzheimer e la depressione. Tuttavia, la preparazione di candidati farmaceutici a base di tropano in una singola forma speculare preferita è stata finora lenta, costosa e tecnicamente impegnativa. Questo studio introduce un modo più diretto ed efficiente per costruire questi complessi impalcature a partire da un materiale di partenza economico, aprendo la strada a una scoperta più rapida di nuovi trattamenti.
Trasformare un blocco di partenza semplice in una ricca famiglia di farmaci
I ricercatori partono dalla tropinone, un composto poco costoso che contiene già lo scheletro ad anello di base presente in molti alcaloidi naturali tropanici. Da questo blocco di partenza semplice lo convertono in unità di costruzione molto versatili chiamate N‑arylsulfonilidrazoni. Queste vengono quindi accoppiate con una vasta gamma di arilbromuri — molecole che portano diverse “decorazioni” aromatiche — per assemblare una famiglia ampia di impalcature N‑bridged [3.2.1]octano e strutture correlate. Il progresso chiave è che questa trasformazione avviene in modo fortemente preferenziale verso una delle due forme speculari, permettendo l’accesso a tropani chirali particolarmente preziosi nel design dei farmaci.
Un catalizzatore su misura che indirizza il traffico molecolare
Al cuore del metodo c’è un catalizzatore di palladio progettato su misura, abbinato a un ligando chirale chiamato Ming‑Phos. La reazione procede attraverso una fase di carbene breve e altamente reattiva seguita da un passaggio sottile in cui un atomo di idrogeno viene rimosso da un carbonio adiacente — noto come eliminazione β‑H. In questo sistema possono intervenire due siti distinti per questa eliminazione, dando in linea di principio quattro percorsi diversi. Il catalizzatore deve quindi controllare non solo quale faccia della molecola reagisce (la sua mano), ma anche quale idrogeno viene rimosso. Modellando con cura il ligando Ming‑Phos — tarando i suoi sostituenti e posizionando gruppi chiave in modo che possano formare un legame a idrogeno con il partner reagente — gli autori creano una «tasca» catalitica che guida la molecola lungo un unico percorso favorito, fornendo prodotti con ottimo rendimento e eccellente purezza enantiomerica.
Dall’ambito della reazione ai veri obiettivi medicinali
In condizioni ottimizzate, il metodo tollera un’ampia gamma di gruppi funzionali sugli arilbromuri, inclusi anelli ricchi o poveri di elettroni, sostituenti ingombranti e eterocicli come le piridine. Funziona inoltre quando l’azoto al ponte viene sostituito dall’ossigeno, ottenendo analoghi oxa‑tropanici. Il gruppo dimostra che questi prodotti non sono solo curiosità da laboratorio: adattano la reazione per costruire intermedi avanzati per farmaci mirati al trattamento dell’Alzheimer e per ligandi che legano i trasportatori delle monoamine, proteine chiave coinvolte nell’umore e nella cognizione. Rispetto a rotte più vecchie che richiedevano condizioni severe, gas tossici o risoluzioni chirali laboriose, la nuova strategia fornisce questi obiettivi in meno passaggi, in condizioni più miti e con un controllo molto migliore della stereochimica.
Uno sguardo sotto il cofano della nuova reazione
Per comprendere come funziona il processo, gli autori conducono studi meccanicistici dettagliati. Variando la natura elettronica dei partner arilbromuri e misurando come ciò influisce sulle velocità di reazione, mostrano che il passo iniziale di formazione del legame con l’arilbromuro difficilmente è il passaggio lento e controllante. Esperimenti di marcatura isotopica suggeriscono inoltre che l’eliminazione β‑H di per sé non è il passaggio limitante di velocità. I dati indicano invece che la formazione dell’intermedio palladio–carbene, derivato dal sulfonilidrazone, costituisce il collo di bottiglia. Ulteriori test escludono un percorso che coinvolga radicali liberi e supportano l’idea che il legame a idrogeno tra il ligando Ming‑Phos e il partner reagente aiuti a organizzare lo stato di transizione, portando a un controllo preciso su quale β‑idrogeno venga rimosso e quale prodotto enantiomerico si formi.
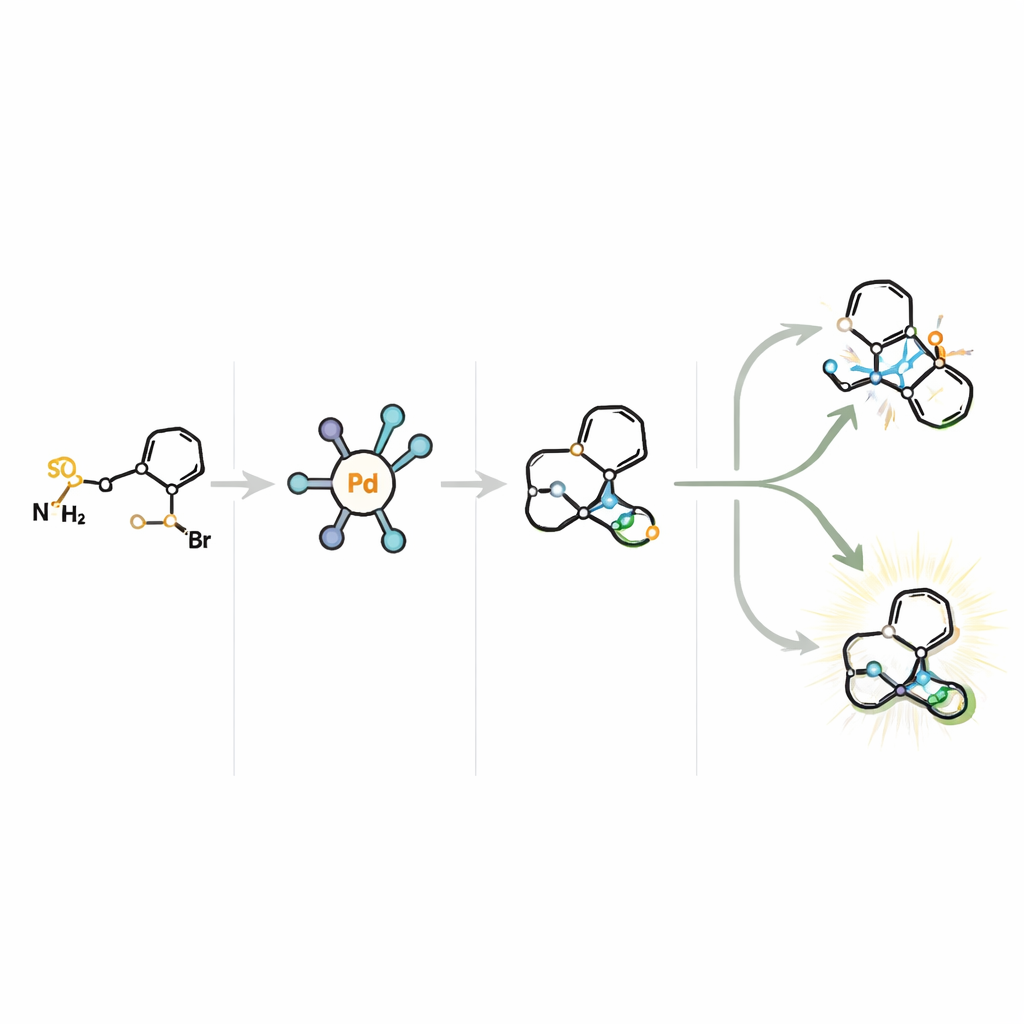
Nuove vie verso farmaci per il cervello e oltre
Complessivamente, questo lavoro dimostra che un catalizzatore accuratamente progettato può domare un passaggio notoriamente difficile da controllare e trasformarlo in uno strumento potente per costruire impalcature molecolari intricate. Consentendo un accesso efficiente, scalabile e altamente selettivo a impalcature tropaniche e oxa‑tropaniche chirali da una materia prima economica, il metodo snellisce la sintesi di potenziali farmaci per l’Alzheimer, ligandi dei trasportatori delle monoamine e altre molecole bioattive. Per i non esperti, il messaggio chiave è che i chimici dispongono ora di un modo più preciso ed economico per costruire una classe cruciale di scheletri farmaceutici, il che potrebbe accelerare lo sviluppo di nuovi trattamenti per disturbi cerebrali e, possibilmente, per il cancro.
Citazione: Fang, C., Ai, J., Wang, Q. et al. Asymmetric synthesis of Heteroatom-bridged [3.2.1]Octane scaffolds via enantioselective β-H elimination reaction. Nat Commun 17, 3315 (2026). https://doi.org/10.1038/s41467-026-69960-6
Parole chiave: impalcature tropaniche, catalisi enantioselettiva, chimica del palladio, scoperta di farmaci, eliminazione di idrogeno β