Clear Sky Science · fr
Synthèse asymétrique d’ossatures [3.2.1]octane bridgées par hétérroatome via une réaction énantiosélective d’élimination β‑H
Pourquoi ces petites molécules en forme d’anneau comptent
De nombreux médicaments importants, en particulier ceux qui agissent sur le cerveau, sont construits autour d’une structure compacte en anneau appelée tropane. Ces « squelettes » moléculaires permettent aux médicaments de se lier à des cibles impliquées dans des maladies comme la maladie d’Alzheimer et la dépression. Pourtant, obtenir des candidats‑médicaments à base de tropane dans une seule forme énantiomérique privilégiée a longtemps été lent, coûteux et techniquement exigeant. Cette étude présente une voie plus directe et plus efficace pour construire ces architectures complexes à partir d’un matériau de départ bon marché, ouvrant la porte à une découverte plus rapide de nouveaux traitements.
Transformer un bloc de départ simple en une riche famille de médicaments
Les chercheurs partent de la tropinone, un composé peu coûteux qui contient déjà l’agencement de base en anneau présent dans de nombreux alcaloïdes tropaniques naturels. À partir de ce bloc de départ simple, ils le transforment en unités de construction hautement polyvalentes appelées N‑arylsulfonylhydrazones. Celles‑ci sont ensuite couplées à une large gamme de bromures d’aryl — des molécules portant différentes « décorations » aromatiques — pour assembler une large famille d’ossatures N‑bridgées [3.2.1]octane et apparentées. L’avancée clé est que cette transformation favorise fortement une forme énantiomérique par rapport à l’autre, donnant accès à des tropanes chiraux particulièrement précieux en conception de médicaments.
Un catalyseur sur mesure qui oriente le trafic moléculaire
Au cœur de la méthode se trouve un catalyseur au palladium conçu sur mesure, associé à un ligand chiral appelé Ming‑Phos. La réaction passe par un état carbène très réactif et de courte durée, suivi d’une étape subtile où un atome d’hydrogène est retiré d’un atome de carbone voisin — connue sous le nom d’élimination β‑H. Dans ce système, deux sites distincts peuvent subir cette élimination, conduisant en principe à quatre voies différentes. Le catalyseur doit donc contrôler non seulement quelle face de la molécule réagit (son orientation), mais aussi quel hydrogène est enlevé. En façonnant soigneusement le ligand Ming‑Phos — en ajustant ses substituants et en positionnant des groupes clés afin qu’ils puissent former une liaison hydrogène avec le partenaire réactif — les auteurs créent une « poche » catalytique qui guide la molécule le long d’une seule voie privilégiée, fournissant les produits avec de hauts rendements et une excellente pureté énantiomérique.
De l’étendue de la réaction aux véritables cibles médicinales
Dans des conditions optimisées, la méthode tolère une large variété de groupes fonctionnels sur les bromures d’aryl, y compris des cycles électron‑donateurs et électron‑attracteurs, des substituants volumineux et des hétérocycles tels que les pyridines. Elle fonctionne également lorsque l’azote en tête de pont est remplacé par de l’oxygène, donnant des analogues oxa‑tropane. L’équipe montre que ces produits ne sont pas de simples curiosités de laboratoire : ils adaptent la réaction pour construire des intermédiaires avancés pour des médicaments destinés au traitement de la maladie d’Alzheimer et pour des ligands se liant aux transporteurs de monoamines, protéines clés impliquées dans l’humeur et la cognition. Par rapport aux voies plus anciennes nécessitant des conditions sévères, des gaz toxiques ou des résolutions chirales laborieuses, la nouvelle stratégie délivre ces cibles en moins d’étapes, dans des conditions plus douces et avec un contrôle bien supérieur de la chiralité moléculaire.
Regarder sous le capot de la nouvelle réaction
Pour comprendre le fonctionnement du procédé, les auteurs réalisent des études mécanistiques détaillées. En variant la nature électronique des partenaires bromure d’aryl et en mesurant l’effet sur les vitesses de réaction, ils montrent que l’étape initiale de formation de la liaison avec le bromure d’aryl est peu susceptible d’être l’étape lente et déterminante. Des expériences de marquage isotopique suggèrent en outre que l’élimination β‑H elle‑même n’est pas limitante en vitesse. Les données indiquent plutôt que la formation de l’intermédiaire palladium–carbene, dérivé de la sulfonylhydrazone, constitue le goulot d’étranglement. Des tests supplémentaires écartent une voie impliquant des radicaux libres et soutiennent un modèle dans lequel des liaisons hydrogène entre le ligand Ming‑Phos et le partenaire réactif aident à organiser l’état de transition, conduisant à un contrôle précis de l’hydrogène β retiré et de l’énantiomère formé.
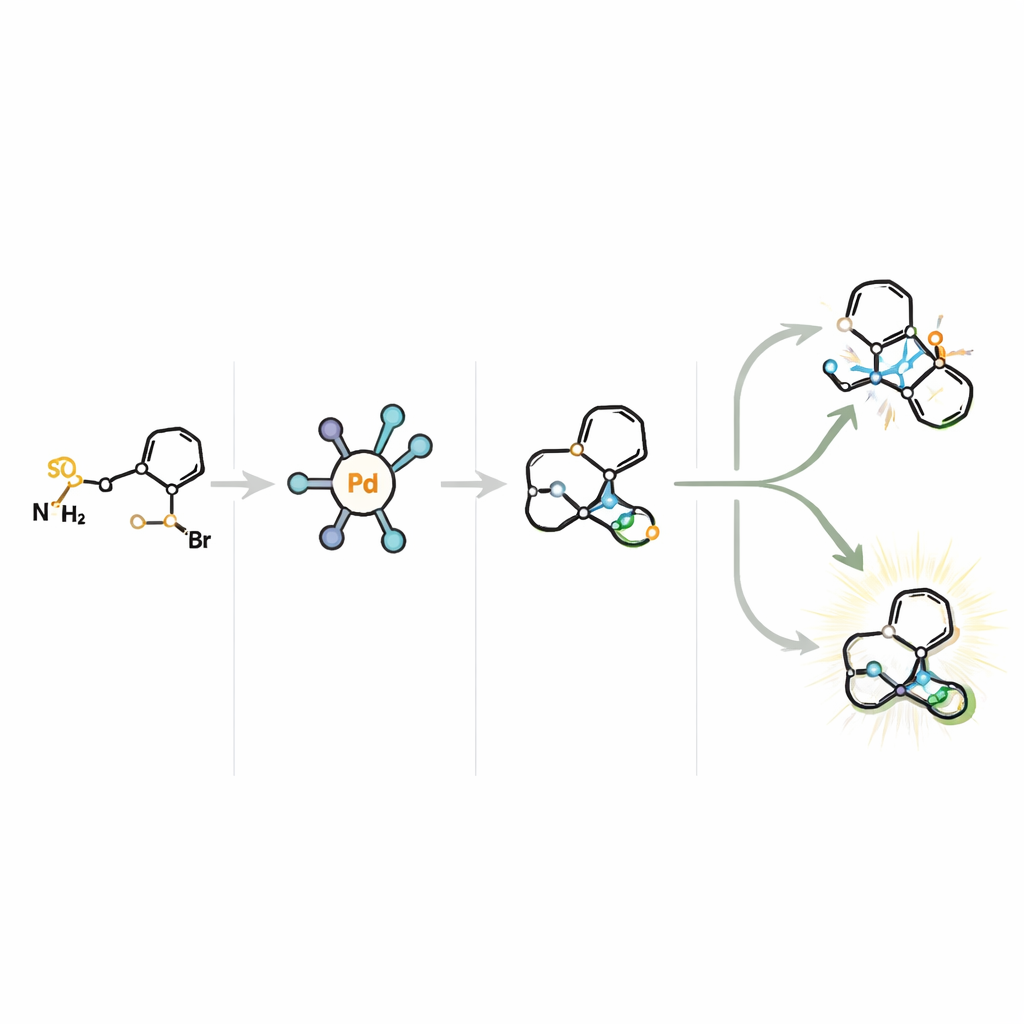
Nouvelles voies vers des médicaments cérébraux et au‑delà
Globalement, ce travail montre qu’un catalyseur soigneusement conçu peut maîtriser une étape notoirement difficile à contrôler et la transformer en un outil puissant pour construire des architectures moléculaires complexes. En permettant un accès efficace, évolutif et hautement sélectif aux ossatures tropane et oxa‑tropane chirales à partir d’un produit de base peu coûteux, la méthode simplifie la synthèse de candidats‑médicaments pour la maladie d’Alzheimer, de ligands pour transporteurs de monoamines et d’autres molécules bioactives. Pour les non‑spécialistes, le message clé est que les chimistes disposent désormais d’un moyen plus précis et économique de construire une classe cruciale d’échafaudages médicamenteux, ce qui pourrait accélérer le développement de nouveaux traitements pour les troubles cérébraux et possiblement le cancer.
Citation: Fang, C., Ai, J., Wang, Q. et al. Asymmetric synthesis of Heteroatom-bridged [3.2.1]Octane scaffolds via enantioselective β-H elimination reaction. Nat Commun 17, 3315 (2026). https://doi.org/10.1038/s41467-026-69960-6
Mots-clés: ossatures tropane, catalyse énantiosélective, chimie du palladium, découverte de médicaments, élimination du β‑hydrogène