Clear Sky Science · pl
Asymetryczna synteza heteroatomowo sprzężonych szkieletów [3.2.1]oktanowych poprzez enantioselektywną reakcję eliminacji β‑H
Dlaczego te małe, pierścieniowe cząsteczki są istotne
Wiele ważnych leków, szczególnie działających w mózgu, opiera się na zwartej, pierścieniowej strukturze zwanej tropanem. Te molekularne „szkieletu” pomagają lekom przyczepiać się do celów związanych z chorobami takimi jak choroba Alzheimera czy depresja. Mimo to wytwarzanie kandydatów leków opartych na tropanie w pojedynczej, preferowanej formie lustrzanej było dotąd powolne, kosztowne i technicznie trudne. W pracy tej przedstawiono bardziej bezpośredni i wydajny sposób budowania tych złożonych ram z taniego materiału wyjściowego, co otwiera drogę do szybszego odkrywania nowych terapii.
Przekształcenie prostego bloku wyjściowego w bogatą rodzinę związków
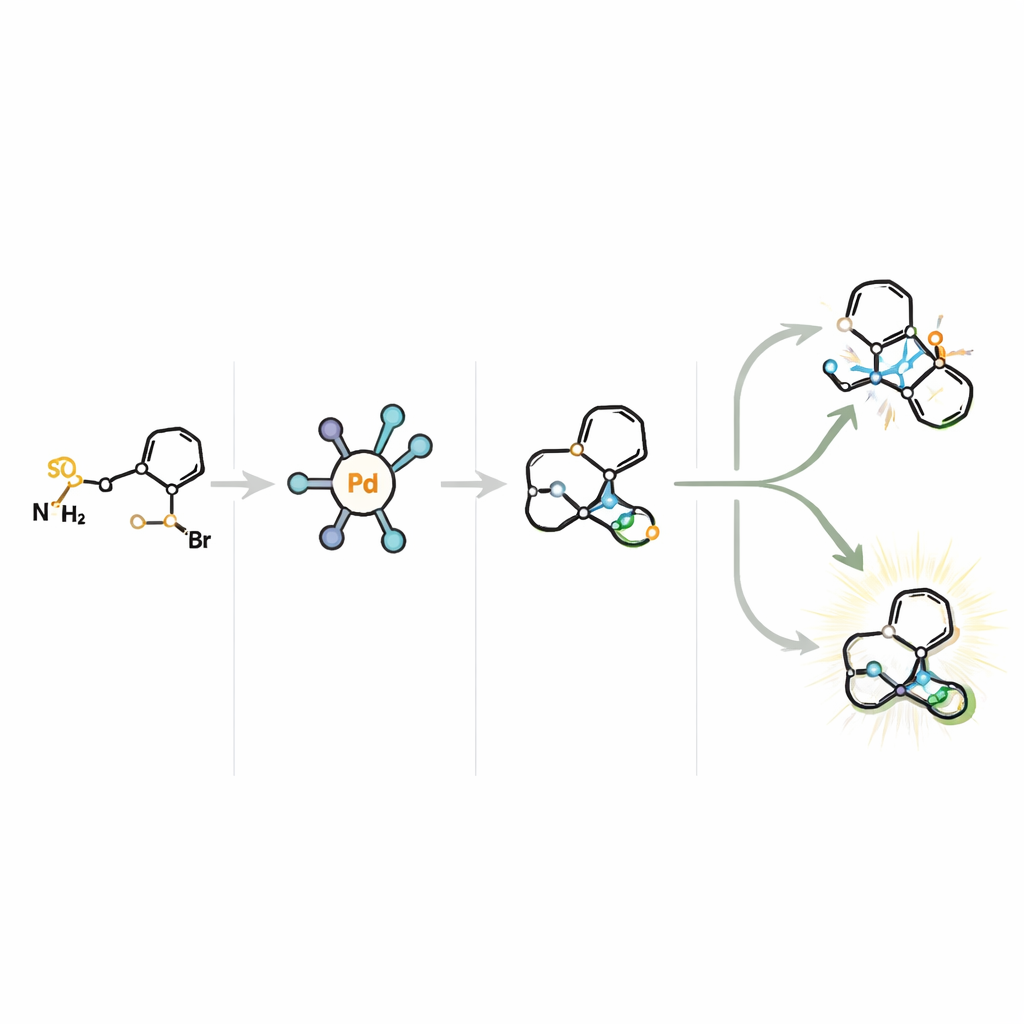
Naukowcy zaczynają od tropinonu, niedrogiego związku, który już zawiera podstawowy układ pierścieni występujący w wielu naturalnych alkaloidach tropanowych. Z tego prostego bloku wyjściowego przekształcają go w wysoce wszechstronne jednostki budulcowe zwane N‑arylosulfonylhydrazonami. Te związki są następnie sprzęgane z szerokim zestawem arylobromków — cząsteczek niosących różne aromatyczne „ozdoby” — aby złożyć rozległą rodzinę N‑mostkowanych szkieletów [3.2.1]oktanowych i pokrewnych. Kluczowym osiągnięciem jest to, że ta transformacja przebiega w sposób silnie faworyzujący jedną formę lustrzaną nad drugą, udostępniając chiralne tropany szczególnie cenne w projektowaniu leków.
Katalizator‑projektant, który kieruje ruchem molekularnym
W sercu metody leży specjalnie zaprojektowany katalizator palladowy w parze z chiralnym ligandem nazwanym Ming‑Phos. Reakcja przebiega przez krótkotrwały, wysoce reaktywny etap karbenowy, po którym następuje subtelny krok, w którym atom wodoru usuwany jest z sąsiedniego atomu węgla — znany jako eliminacja β‑H. W tym systemie dwie odrębne pozycje mogą podlegać tej eliminacji, co teoretycznie prowadzi do czterech różnych ścieżek. Katalizator musi więc kontrolować nie tylko którą stroną cząsteczka reaguje (jej „ręczność”), lecz także który wodór zostaje usunięty. Poprzez staranne ukształtowanie ligandu Ming‑Phos — dostrojenie podstawników i rozmieszczenie kluczowych grup tak, by mogły tworzyć wiązanie wodorowe z partnerem reakcyjnym — autorzy tworzą „kieszeń” katalizatora, która kieruje cząsteczkę jedną, uprzywilejowaną drogą, dostarczając produkty w wysokim wydatku i doskonałej czystości enancjomerycznej.
Od zakresu reakcji do rzeczywistych celów medycznych
W zoptymalizowanych warunkach metoda toleruje szerokie spektrum grup funkcyjnych na arylobromkach, w tym pierścienie bogate i ubogie elektronowo, rozbudowane podstawienia oraz heterocykle takie jak pirydyny. Działa także, gdy azot w węźle mostkowym zostanie zastąpiony tlenem, dając analogi oxa‑tropanowe. Zespół wykazuje, że te produkty to nie tylko ciekawostki laboratoryjne: adaptowali reakcję do syntezy zaawansowanych prekursorów leków ukierunkowanych na leczenie choroby Alzheimera oraz ligandów wiążących transportery monoaminowe, kluczowe białka zaangażowane w nastrój i procesy poznawcze. W porównaniu ze starszymi drogami, które wymagały surowych warunków, toksycznych gazów lub pracochłonnej rozdzielczości chiralnej, nowa strategia dostarcza te cele w mniejszej liczbie etapów, w łagodniejszych warunkach i z dużo lepszą kontrolą „ręczności” molekularnej.
Zajrzeć pod maskę nowej reakcji
Aby zrozumieć, jak przebiega proces, autorzy przeprowadzili szczegółowe badania mechanistyczne. Poprzez zmianę charakteru elektronowego partnerów arylobromkowych i mierzenie, jak wpływa to na szybkości reakcji, pokazują, że początkowy etap tworzenia wiązania z arylobromkiem prawdopodobnie nie jest wolnym, kontrolującym etapem. Eksperymenty z znakowaniem izotopowym dodatkowo sugerują, że sama eliminacja β‑H nie jest krokiem ograniczającym prędkość. Zamiast tego dane wskazują, że wąskim gardłem jest tworzenie się pośrednika pallad‑karbenowego pochodzącego z sulfonylhydrazonu. Dodatkowe testy wykluczają ścieżkę obejmującą wolne rodniki i wspierają obraz, w którym wiązania wodorowe między ligandem Ming‑Phos a partnerem reakcyjnym pomagają zorganizować stan przejściowy, prowadząc do precyzyjnej kontroli, który wodór β zostaje usunięty i jaki produkt lustrzany powstaje.
Nowe drogi do leków działających na mózg i nie tylko
Podsumowując, ta praca pokazuje, że starannie skonstruowany katalizator potrafi okiełznać krok tradycyjnie trudny do kontroli i przekształcić go w potężne narzędzie do budowy zawiłych ram molekularnych. Umożliwiając wydajny, skalowalny i wysoko selektywny dostęp do chirialnych szkieletów tropanowych i oxa‑tropanowych z taniego surowca, metoda upraszcza syntezę potencjalnych leków na chorobę Alzheimera, ligandów transporterów monoaminowych i innych bioaktywnych cząsteczek. Dla osób niebędących specjalistami kluczowym przesłaniem jest to, że chemicy mają teraz bardziej precyzyjny i ekonomiczny sposób konstruowania istotnej klasy szkieletów lekowych, co może przyspieszyć rozwój nowych terapii chorób mózgu, a być może także raka.
Cytowanie: Fang, C., Ai, J., Wang, Q. et al. Asymmetric synthesis of Heteroatom-bridged [3.2.1]Octane scaffolds via enantioselective β-H elimination reaction. Nat Commun 17, 3315 (2026). https://doi.org/10.1038/s41467-026-69960-6
Słowa kluczowe: szkielety tropanowe, enantioselektywna kataliza, chemia palladu, odkrywanie leków, eliminacja wodoru β