Clear Sky Science · ru
Асимметричный синтез гетероатом‑маятниковых каркасов [3.2.1]октана через энантиоселективную реакцию β‑H‑элиминации
Почему эти маленькие кольцевые молекулы важны
Многие важные лекарства, особенно действующие на мозг, построены вокруг компактной кольцевой структуры, называемой тропаном. Эти молекулярные «скелеты» помогают препаратам связываться с мишенями, вовлечёнными в заболевания, такие как болезнь Альцгеймера и депрессия. Тем не менее получение кандидатов на основе тропана в одной, предпочтительной зеркально‑несовмещённой форме было медленным, дорогим и технически сложным. В этом исследовании представлен более прямой и эффективный способ построения таких сложных каркасов из дешёвого исходного вещества, что открывает путь к более быстрой разработке новых терапий.
Преобразование простого строительного блока в богатое семейство соединений
Исследователи начинают с тропинона, недорогого соединения, которое уже содержит базовую кольцевую архитектуру, встречающуюся во многих натуральных тропановых алкалоидах. Из этого простого исходника они получают высокофункциональные строительные блоки — N‑арилсульфонилгидразоны. Эти соединения затем сопрягают с широким набором арилбромидов — молекул с разными ароматическими «декорациями» — чтобы собрать обширное семейство N‑мостиковых [3.2.1]октановых и родственных каркасов. Ключевое достижение в том, что это превращение происходит с сильным предпочтением одной зеркальной формы над другой, что даёт доступ к хиральным тропанам, особенно ценным в дизайне лекарств.
Дизайнерский катализатор, направляющий молекулярное движение
В основе метода лежит специально разработанный палладиевый катализатор в сочетании с хиральным лигандом под названием Ming‑Phos. Реакция проходит через короткоживущий, высокореактивный карбеновый этап, за которым следует тонкий шаг удаления атома водорода с соседнего атома углерода — известный как β‑H‑элиминация. В этой системе два различных участка могут подвергаться этой элиминации, что в принципе даёт четыре возможных пути. Катализатор должен контролировать не только с какой «грани» молекулы идёт реакция (ее «право‑/лево‑рукость»), но и какой именно водород удаляется. Тщательно формируя лиганд Ming‑Phos — подбирая заместители и позиционируя ключевые группы так, чтобы они могли образовывать водородную связь с реагирующим партнёром — авторы создают каталитический «карман», который направляет молекулу по одному предпочтительному пути, обеспечивая продукты в высоких выходах и с отличной энантиомерной чистотой.
От объёма реакций к реальным медицинским мишеням
При оптимальных условиях метод допускает широкий набор функциональных групп на арилбромидах, включая электронной‑богатые и электронной‑бедные кольца, громоздкие заместители и гетероциклы, такие как пиридины. Он также работает, когда азот в мостовом положении заменён кислородом, давая окса‑тропановые аналоги. Команда демонстрирует, что эти продукты — не просто лабораторные курьёзы: они адаптируют реакцию для получения продвинутых интермедиатов для препаратов против болезни Альцгеймера и для лигандов, связывающихся с моноаминными транспортёрами — ключевыми белками, вовлечёнными в настроение и когницию. По сравнению с более старыми путями, требовавшими жёстких условий, токсичных газов или трудоёмкой хиральной резолюции, новая стратегия даёт эти мишени за меньшее число стадий, в более мягких условиях и с гораздо лучшим контролем молекулярной правой/левой конфигурации.
Заглядывая в устройство новой реакции
Чтобы понять, как работает процесс, авторы проводят детальные механистические исследования. Варьируя электронные свойства партнёров‑арилбромидов и измеряя, как это влияет на скорости реакций, они показывают, что начальный шаг образования связи с арилбромидом вряд ли является медленным, контролирующим стадийным звеном. Эксперименты с изотопной меткой дополнительно указывают на то, что сама β‑H‑элиминация не является лимитирующей по скорости. Вместо этого данные указывают на образование палладий‑карбенового интермедиата, происходящего от сульфонилгидразона, как на узкое место. Дополнительные тесты исключают путь с участием свободных радикалов и поддерживают картину, в которой водородные связи между лигандом Ming‑Phos и реагирующим партнёром помогают организовать переходное состояние, обеспечивая точный контроль того, какой β‑водород удаляется и какой зеркальный продукт образуется.
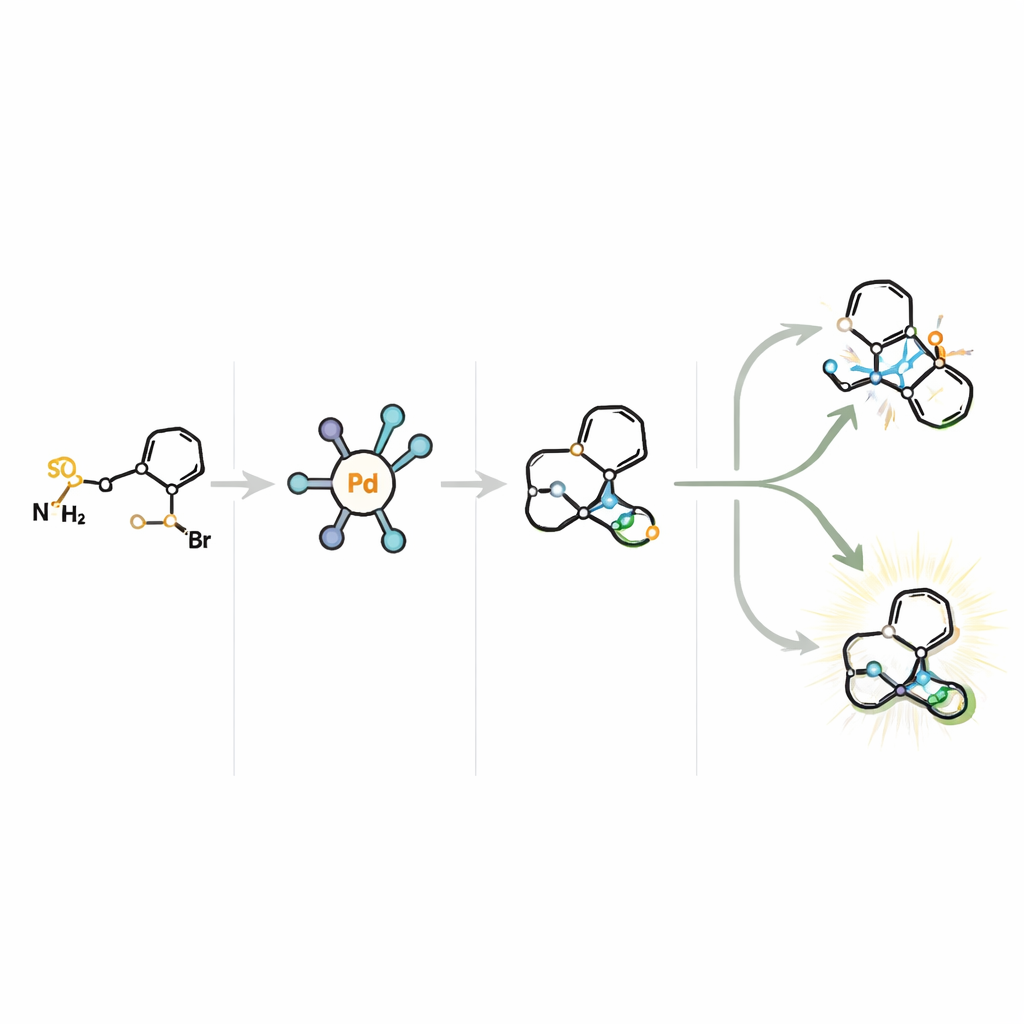
Новые пути к препаратам для мозга и не только
В целом эта работа показывает, что тщательно спроектированный катализатор способен укротить шаг, традиционно считавшийся трудноконтролируемым, и превратить его в мощный инструмент для построения сложных молекулярных каркасов. Обеспечивая эффективный, масштабируемый и высокоселективный доступ к хиральным тропановым и окса‑тропановым каркасам из дешёвого сырья, метод упрощает синтез потенциальных препаратов против болезни Альцгеймера, лигандов моноаминных транспортёров и других биологически активных молекул. Для неспециалистов ключевое сообщение в том, что у химиков теперь есть более точный и экономичный способ строить важный класс лекарственных «скелетов», что может ускорить разработку новых лечений для заболеваний мозга и, возможно, рака.
Цитирование: Fang, C., Ai, J., Wang, Q. et al. Asymmetric synthesis of Heteroatom-bridged [3.2.1]Octane scaffolds via enantioselective β-H elimination reaction. Nat Commun 17, 3315 (2026). https://doi.org/10.1038/s41467-026-69960-6
Ключевые слова: тропановые каркасы, энантиоселективный катализ, палладиевая химия, поиск лекарств, β‑удаление водорода