Clear Sky Science · sv
Asymmetrisk syntes av heteroatom‑bryggade [3.2.1]‑oktanskelett via enantioselektiv β‑H‑elimineringsreaktion
Varför dessa små ringformade molekyler spelar roll
Många viktiga läkemedel, särskilt de som verkar i hjärnan, är uppbyggda kring en kompakt, ringformad struktur kallad tropan. Dessa molekylära ”skelett” hjälper läkemedel att fästa vid mål som är inblandade i sjukdomar som Alzheimers och depression. Att framställa tropanbaserade läkemedelskandidater i en enda, föredragen spegelbildsform har dock varit långsamt, kostsamt och tekniskt krävande. Denna studie introducerar ett mer direkt och effektivt sätt att bygga dessa komplexa ramverk från ett billigt utgångsmaterial, vilket öppnar dörren för snabbare upptäckt av nya behandlingar.
Att förvandla ett enkelt utgångsblock till en rik familj av läkemedel
Forskarna börjar med tropinon, en billig förening som redan innehåller den grundläggande ringarkitekturen som finns i många naturliga tropanalkaloider. Från detta enkla utgångsblock omvandlar de det till mycket mångsidiga byggstenar kallade N‑arylsulfonylhydrazoner. Dessa kopplas sedan med ett brett spektrum av arylbromider — molekyler som bär olika aromatiska ”dekorationer” — för att sammanställa en omfattande familj av N‑bryggade [3.2.1]‑oktanskelett och relaterade skelett. Den avgörande framgången är att denna omvandling sker på ett sätt som starkt gynnar en spegelbildsform framför den andra, vilket ger tillgång till kirala tropaner som är särskilt värdefulla i läkemedelsdesign.
En skräddarsydd katalysator som styr molekyltrafiken
I centrum för metoden finns en specialutformad palladiumkatalysator i kombination med en kiral ligand kallad Ming‑Phos. Reaktionen går via ett kortlivat, mycket reaktivt karbensteg följt av ett subtilt moment där en väteatom avlägsnas från en intilliggande kolatom — känt som β‑H‑elimineringssteg. I detta system kan två olika platser genomgå denna eliminering, vilket i princip leder till fyra olika vägar. Katalysatorn måste därför kontrollera inte bara vilken sida av molekylen som reagerar (dess handighet) utan också vilket väte som tas bort. Genom att noggrant forma Ming‑Phos‑liganden — finjustera dess substituenter och placera nyckelgrupper så att de kan bilda en vätebindning till den reagerande partnern — skapar författarna ett katalysator"fack" som vägleder molekylen längs en enda, favoritväg och levererar produkter i hög utbyte och med utmärkt enantiomerisk renhet.
Från reaktionsomfång till verkliga medicinska mål
Under optimerade förhållanden tolererar metoden ett brett spektrum av funktionella grupper på arylbromiderna, inklusive elektronrika och elektronfattiga ringar, skrymmande substituenter och heterocykliska enheter såsom pyridiner. Den fungerar också när brygghuvudets kväve byts mot syre och ger då oxa‑tropananaloger. Teamet visar att dessa produkter inte bara är laboratoriekuriositeter: de anpassar reaktionen för att bygga avancerade intermediärer för läkemedel inriktade på behandling av Alzheimers sjukdom och för ligander som binder monoamintransportörer, nyckelproteiner involverade i stämning och kognition. Jämfört med äldre vägar som krävde hårda förhållanden, giftiga gaser eller omfattande kiral upplösning levererar den nya strategin dessa mål i färre steg, under mildare villkor och med mycket bättre kontroll över molekylens handighet.
Att titta under huven på den nya reaktionen
För att förstå hur processen fungerar genomför författarna detaljerade mekanistiska studier. Genom att variera den elektroniska karaktären hos arylbromidpartnerna och mäta hur detta påverkar reaktionshastigheterna visar de att det inledande bindningsbildande steget med arylbromiden sannolikt inte är det långsamma, styrande steget. Isotopmärkningsförsök tyder vidare på att β‑H‑elimineringen i sig inte är hastighetsbegränsande. Istället pekar data mot bildningen av palladium–karben‑intermediatet, härlett från sulfonylhydrazonen, som flaskhalsen. Ytterligare tester utesluter en väg som involverar fria radikaler och stöder en bild där vätebindning mellan Ming‑Phos‑liganden och den reagerande partnern hjälper till att organisera övergångstillståndet, vilket leder till exakt kontroll över vilket β‑väte som avlägsnas och vilken spegelbildsprodukt som bildas.
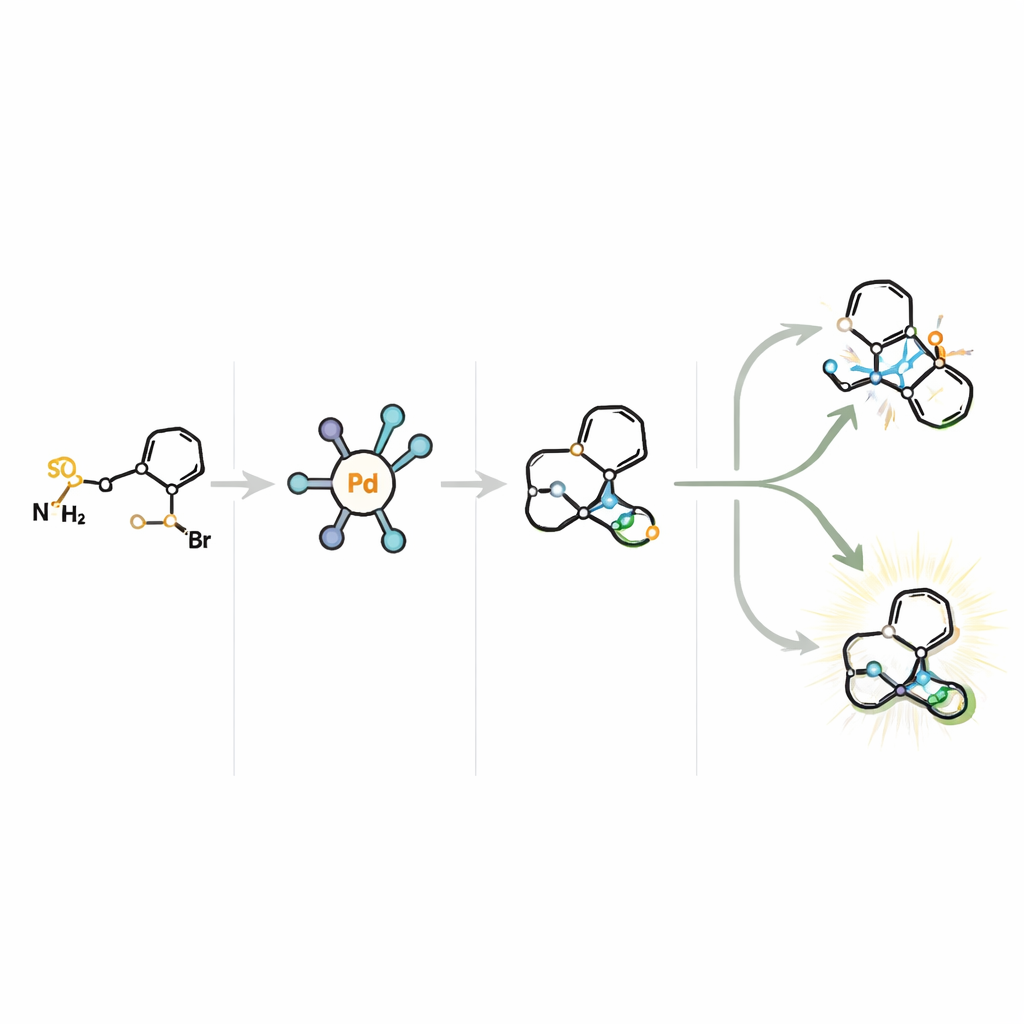
Nya vägar till hjärnläkemedel och mer därtill
Sammanfattningsvis visar detta arbete att en omsorgsfullt utformad katalysator kan tygla ett notorisk svårt‑styrt steg och göra det till ett kraftfullt verktyg för att bygga intrikata molekylära ramverk. Genom att möjliggöra effektiv, skalbar och mycket selektiv tillgång till kirala tropan‑ och oxa‑tropanskelett från ett billigt råmaterial förenklar metoden syntesen av potentiella Alzheimersläkemedel, ligander för monoamintransportörer och andra bioaktiva molekyler. För icke‑specialister är huvudbudskapet att kemister nu har ett mer precist och ekonomiskt sätt att konstruera en avgörande klass av läkemedelsryggräder, vilket kan påskynda utvecklingen av nya behandlingar för hjärnsjukdomar och möjligen även cancer.
Citering: Fang, C., Ai, J., Wang, Q. et al. Asymmetric synthesis of Heteroatom-bridged [3.2.1]Octane scaffolds via enantioselective β-H elimination reaction. Nat Commun 17, 3315 (2026). https://doi.org/10.1038/s41467-026-69960-6
Nyckelord: tropanskelett, enantioselektiv katalys, palladiumkemi, läkemedelsupptäckt, beta‑väteeliminering