Clear Sky Science · zh
通过平铺碱基编辑的等位基因读出实现核苷酸分辨率的调控元件绘制
为什么微小的DNA改变会影响癌症治疗
肿瘤科医生越来越依赖能够识别肿瘤细胞表面特定标记的免疫疗法来追踪并消灭癌细胞。白血病细胞上最著名的标记之一是CD19,这是强效CAR-T细胞疗法的靶点。然而,一些患者会复发,因为他们的癌细胞悄然丢失或降低了该标记,从而躲过治疗。这项研究展示了科学家如何能够放大观察控制CD19的DNA区段,精确识别那些在这些控制区内对保持CD19可见性至关重要的单个“字母”——以及仅仅几个字母的变化如何帮助癌细胞逃避免疫治疗。 
解读基因的控制开关
基因并非简单的开关;它们由称为增强子的附近DNA开关控制,这些开关微调细胞产生某种蛋白质的量。许多与疾病相关的DNA变化位于这些非编码控制区,而不是蛋白质编码基因本身。传统的遗传学研究可以标记可疑区域,但难以确定这些区域内究竟哪些DNA字母是关键,或这些字母如何影响细胞行为。对于像CD19 CAR-T这样的疗法,这一空白很重要:控制开关中微妙的改变可能使CD19下降到足以让癌细胞躲藏的程度,同时不破坏细胞的其他机能。
用分子“铅笔”逐字改写DNA
研究人员构建了一个从实验到计算的端到端框架,以空前精度绘制这些关键的DNA字母。他们聚焦于白血病细胞中位于CD19基因上游、长346个碱基的一个增强子。借助先进的CRISPR碱基编辑器——可以在不切断DNA的情况下改变单个DNA字母的分子“铅笔”——他们用一套密集的引导分子库遍历了该增强子。每个引导针对略有不同的位置,合力在数百万个细胞中引入各异的单字母变化以及同一短段内的小组合变化。
将DNA变体与总体蛋白水平关联
为了观察每个编辑后的DNA版本如何影响CD19,团队用一种荧光抗体染色细胞,该抗体在CD19水平高时发出更强的荧光。随后他们使用细胞分选机将细胞群体分为CD19高表达和CD19低表达两组。关键在于,他们没有仅仅统计哪些引导存在,而是直接测序了每组中被编辑的增强子区域。新的分析工具——CRISPR-Millipede和改编版的DESeq2软件——使得他们能够将每一个独特的编辑后DNA序列视作单独的变体,并通过统计方法推断出哪些精确的单字母改变使细胞趋向于降低或提高CD19表达。 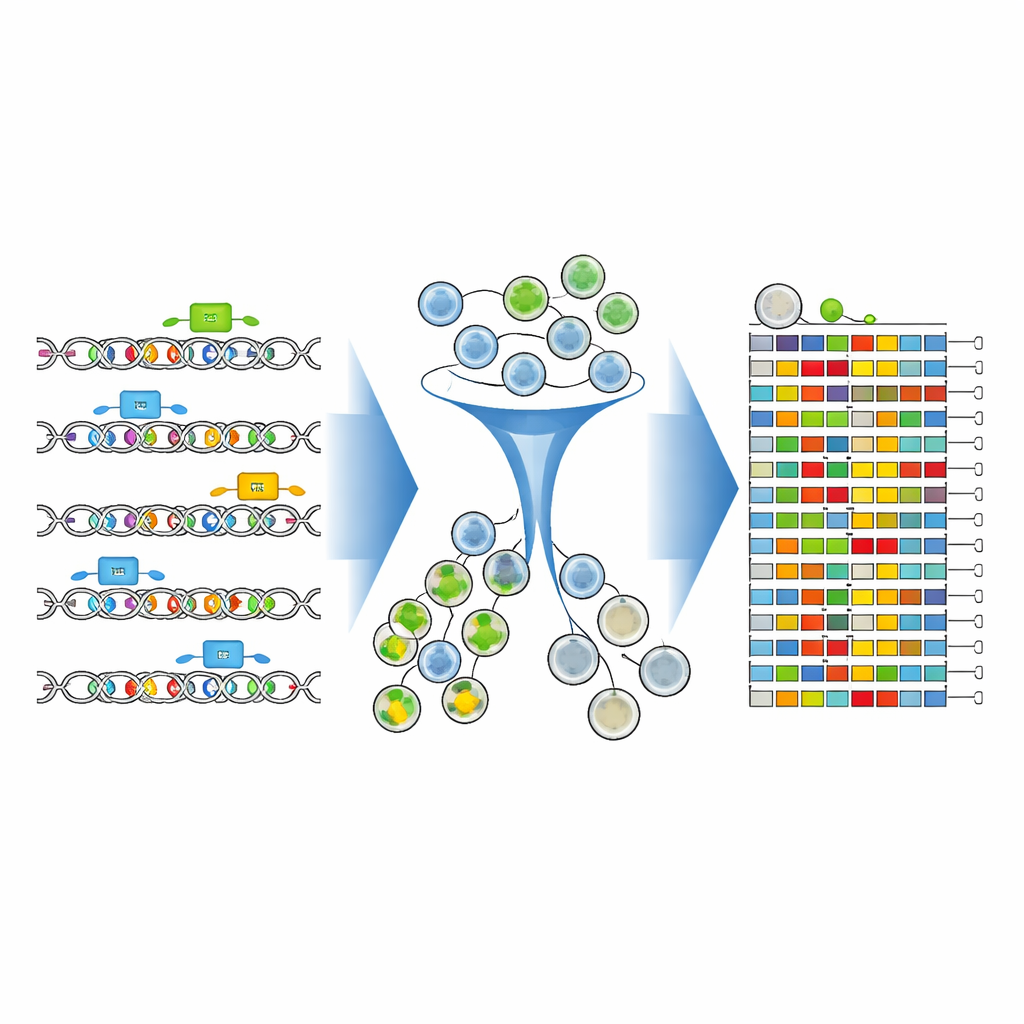
在增强子中找到关键的蛋白结合位点
借助逐核苷酸的图谱,研究人员将结果与已知的转录因子结合基序叠加——转录因子是结合DNA以上下调基因的蛋白质。他们发现影响最大的字母集中在MYB、PAX5和EBF1等因子识别的位点内,这些因子是B细胞的重要调控蛋白。通过有意重现这些特定的增强子突变以及敲除相应的转录因子,他们证实损坏这些结合位点会降低CD19水平。他们还表明,一些来自早期基于引导计数的方法的看似阳性结果其实是假阳性,由于庞大的编辑机械本身停留在DNA上而非真实的序列改变所致,并据此设计了可降解的编辑器以区分这些效应。
微小增强子变化如何削弱CAR-T疗法
最后,团队检验了这些微妙的调控调整是否真正影响癌症治疗。他们将带有或不带增强子突变的白血病细胞混合,并暴露于CD19 CAR-T细胞下。携带特定增强子改变的被编辑细胞在CAR-T攻击下持续优先生长,显示出CD19的适度降低——不是由于破坏CD19基因本身,而是通过改变其增强子——足以帮助癌细胞存活。这项工作表明了一种实用且可扩展的方法,用以在基因控制区的单字母水平绘制因果关系图谱,并证明非编码变异可以悄然左右前沿免疫疗法的成败。
引用: Becerra, B., Wittibschlager, S., Patel, Z.M. et al. Nucleotide-resolution mapping of regulatory elements via allelic readout of tiled base editing. Nat Commun 17, 3398 (2026). https://doi.org/10.1038/s41467-026-69918-8
关键词: CRISPR碱基编辑, 基因调控, CD19 CAR-T 耐药性, 非编码变异, 增强子绘图