Clear Sky Science · fr
Cartographie à résolution nucléotide des éléments régulateurs via le signal allélique de l’édition de bases en tuiles
Pourquoi de minuscules changements d’ADN peuvent compter pour le traitement du cancer
Les oncologues s’appuient de plus en plus sur des thérapies immunitaires sophistiquées qui traquent les cellules tumorales en reconnaissant des marqueurs spécifiques à leur surface. L’un des marqueurs les mieux connus des cellules leucémiques est le CD19, cible des puissantes thérapies CAR-T. Pourtant, certains patients rechutent parce que leurs cellules cancéreuses perdent ou atténuent discrètement ce marqueur, échappant ainsi au traitement. Cette étude montre comment les scientifiques peuvent maintenant zoomer sur des segments d’ADN qui contrôlent le CD19, en identifiant quelles « lettres » individuelles dans ces régions de contrôle sont essentielles pour maintenir CD19 visible — et comment des changements sur seulement quelques-unes de ces lettres peuvent permettre aux cellules cancéreuses d’échapper à la thérapie. 
Lire les interrupteurs de contrôle de nos gènes
Les gènes ne sont pas simplement allumés ou éteints : ils sont pilotés par des interrupteurs d’ADN proches, appelés enhancers, qui ajustent finement la quantité d’une protéine que la cellule produit. De nombreuses altérations associées à des maladies se trouvent dans ces régions de contrôle non codantes plutôt que dans les gènes codant des protéines. Les études génétiques classiques peuvent signaler des régions suspectes mais peinent à dire exactement quelles lettres d’ADN à l’intérieur sont critiques, ou comment elles modifient le comportement cellulaire. Pour des thérapies comme les CAR-T anti-CD19, cette lacune est importante : une modification subtile d’un interrupteur de contrôle peut diminuer le CD19 juste ce qu’il faut pour que les cellules cancéreuses se cachent, tout en laissant intact le reste de la machinerie cellulaire.
Utiliser des « stylos » moléculaires pour réécrire l’ADN lettre par lettre
Les chercheurs ont construit un cadre expérimental et computationnel complet pour cartographier ces lettres d’ADN cruciales avec une précision sans précédent. Ils se sont focalisés sur un enhancer de 346 lettres situé juste en amont du gène CD19 dans des cellules leucémiques. En utilisant des éditeurs de base CRISPR avancés — des « stylos » moléculaires capables de changer des lettres d’ADN individuelles sans couper l’ADN — ils ont balayé cet enhancer avec une bibliothèque dense de guides. Chaque guide ciblait un emplacement légèrement différent, ensemblant des millions de cellules de modifications d’une seule lettre et de petites combinaisons de changements au sein du même court segment d’ADN.
Lier les variants d’ADN aux niveaux protéiques en masse
Pour voir comment chaque version éditée de l’ADN affectait le CD19, l’équipe a marqué les cellules avec un anticorps fluorescent qui brille plus intensément lorsque les niveaux de CD19 sont élevés. Ils ont ensuite utilisé un trieur cellulaire pour séparer la population en groupes CD19-élevé et CD19-faible. Crucialement, au lieu de se contenter de compter quels guides étaient présents, ils ont séquencé directement la région enhancer éditée elle-même dans chaque groupe. De nouveaux outils d’analyse — CRISPR-Millipede et une version adaptée du logiciel DESeq2 — leur ont permis de considérer chaque séquence d’ADN éditée distincte comme son propre variant et d’inférer statistiquement quelles modifications d’une seule lettre faisaient basculer les cellules vers des niveaux plus faibles ou plus élevés de CD19. 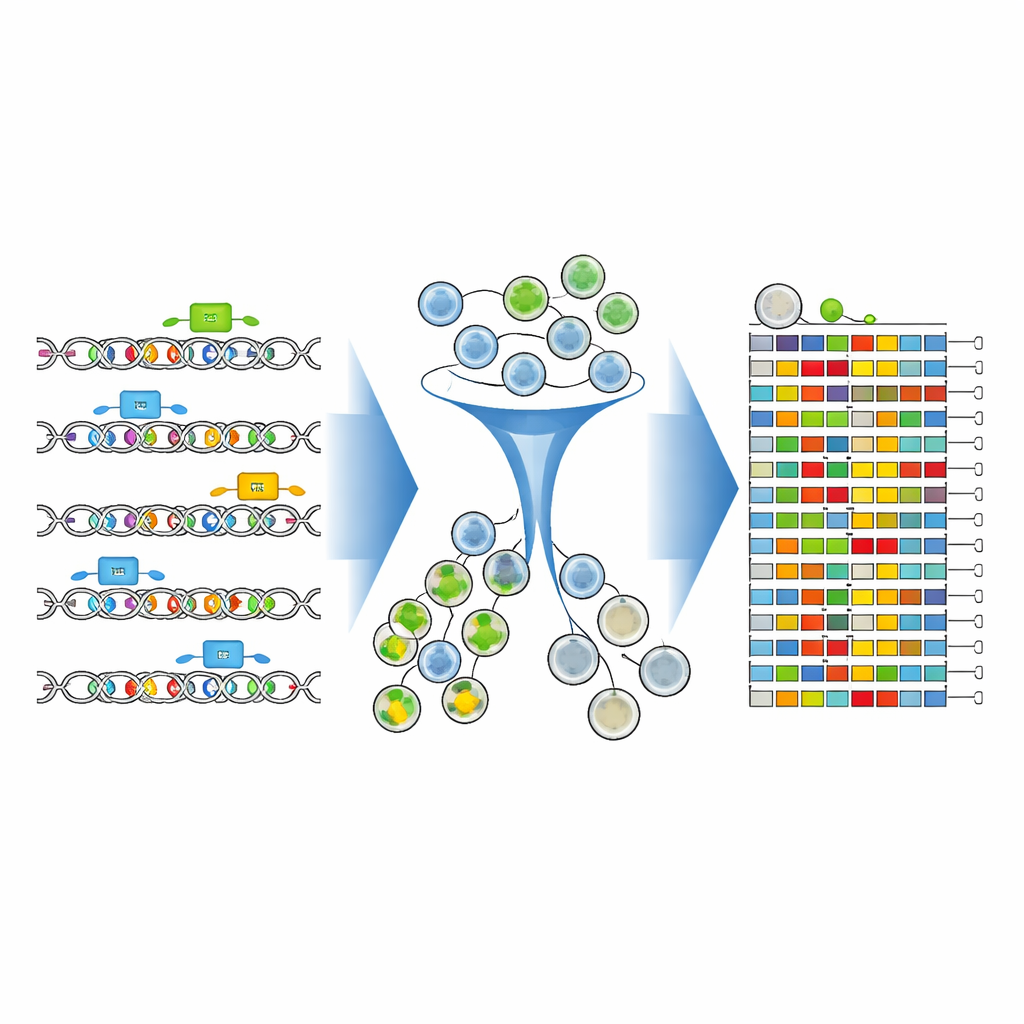
Identifier les sites d’ancrage protéiques clés dans l’enhancer
Avec cette carte nucléotide par nucléotide en main, les chercheurs ont superposé leurs résultats aux motifs de liaison connus pour les facteurs de transcription — des protéines qui se fixent à l’ADN pour activer ou réprimer les gènes. Ils ont constaté que les lettres les plus impactantes se regroupaient au sein de sites reconnus par des facteurs tels que MYB, PAX5 et EBF1, qui sont des régulateurs importants des cellules B. En recréant délibérément ces mutations spécifiques d’enhancer et en désactivant les facteurs de transcription correspondants, ils ont confirmé que l’altération de ces sites d’ancrage réduit les niveaux de CD19. Ils ont aussi montré que certains signaux obtenus par d’anciennes méthodes basées sur le comptage des guides étaient des faux positifs dus à la simple présence de la machinerie d’édition volumineuse sur l’ADN plutôt qu’à de véritables changements de séquence, et ils ont conçu un éditeur dégradable pour dissocier ces effets.
Comment de petites modifications d’enhancer peuvent compromettre la thérapie CAR-T
Enfin, l’équipe a évalué si ces ajustements régulateurs subtils influençaient réellement le traitement du cancer. Ils ont mélangé des cellules leucémiques porteuses ou non des mutations d’enhancer et les ont exposées à des cellules CAR-T anti-CD19. Les cellules éditées portant certaines modifications d’enhancer ont systématiquement surcroît par rapport à leurs homologues non éditées sous l’attaque CAR-T, révélant que des réductions modestes de CD19 — provoquées non pas par la rupture du gène CD19 mais par la modification de son enhancer — suffisaient à aider les cellules cancéreuses à survivre. Ce travail démontre une approche pratique et évolutive pour cartographier la relation de cause à effet au niveau d’une seule lettre dans les régions de contrôle génétique, et montre que des variants non codants peuvent silencieusement orienter le succès ou l’échec des immunothérapies de pointe.
Citation: Becerra, B., Wittibschlager, S., Patel, Z.M. et al. Nucleotide-resolution mapping of regulatory elements via allelic readout of tiled base editing. Nat Commun 17, 3398 (2026). https://doi.org/10.1038/s41467-026-69918-8
Mots-clés: Édition de base CRISPR, régulation génétique, résistance CAR-T anti-CD19, variants non codants, cartographie des enhancers