Clear Sky Science · ar
رسم خرائط للعناصر المنظمة بدقة النوكليوتيد عبر قراءة أليلية لتحرير القواعد المصفوف
لماذا قد تهم التغيرات الصغيرة في الحمض النووي لعلاج السرطان
يعتمد أطباء السرطان بشكل متزايد على علاجات مناعية ذكية تصطاد الخلايا الورمية عبر التعرف على علامات محددة على سطحها. إحدى أشهر هذه العلامات على خلايا اللوكيميا تُدعى CD19، وهو الهدف لعلاجات CAR-T القوية. ومع ذلك ينهار بعض المرضى لأن خلايا السرطان قد تفقد هذه العلامة أو تخففها بهدوء، فتفلت من العلاج. تُظهر هذه الدراسة كيف يمكن للعلماء الآن تكبير مناطق من الحمض النووي التي تتحكم في CD19، وتحديد أي «حروف» فردية في تلك المناطق التنظيمية مهمة للحفاظ على ظهور CD19 — وكيف أن تغييرات في بضعة حروف فقط قادرة على مساعدة خلايا السرطان على الهروب من العلاج. 
قراءة مفاتيح التحكم في جيناتنا
الجينات ليست مجرد تشغيل أو إيقاف؛ بل تتحكم بها مفاتيح DNA المجاورة المسماة المعززات التي تضبط بدقة كمية البروتين التي تنتجها الخلية. الكثير من التغيرات المرتبطة بالأمراض تقع في هذه المناطق التنظيمية غير المشفرة بدلاً من داخل الجينات المشفرة للبروتينات نفسها. الدراسات الجينية التقليدية قد تشير إلى مناطق مريبة لكنها تجد صعوبة في تحديد أي من حروف الحمض النووي داخلها حاسمة، أو كيف تؤثر على سلوك الخلية. بالنسبة للعلاجات مثل خلايا CAR-T المستهدفة CD19، هذه الفجوة مهمة: فقد يخفض تغيير طفيف في مفتاح تحكم مستوى CD19 بما يكفي لتختفي الخلايا السرطانية، بينما تظل باقي آليات الخلية سليمة.
استخدام «أقلام» جزيئية لإعادة كتابة الحمض النووي حرفاً تلو الآخر
بنى الباحثون إطاراً تجريبياً وحسابياً متكاملاً لرسم خريطة هذه الحروف الحرجة بدقة غير مسبوقة. ركزوا على معزز طوله 346 حرفاً يقع مباشرة قبل جين CD19 في خلايا اللوكيميا. باستخدام معدِّلات قواعد CRISPR المتقدمة — «أقلام» جزيئية يمكنها تغيير حرف واحد من الحمض النووي دون قطعه — مرّوا عبر هذا المعزز بمكتبة كثيفة من دلائل التوجيه. استهدف كل دليل موضعاً مختلفاً قليلاً، مجمّعين ملايين الخلايا مع تغييرات مفردة في الحروف ومجموعات صغيرة من التغييرات داخل نفس المقاطع القصيرة من الحمض النووي.
ربط متغيرات الحمض النووي بمستويات البروتين على نطاق واسع
لمعرفة كيف أثر كل طراز من الحمض النووي المعدل على CD19، صبغ الفريق الخلايا بأجسام مضادة فلورية تتوهج بشكل أقوى عندما تكون مستويات CD19 عالية. ثم استخدموا جهاز فرز الخلايا لتقسيم التجمع إلى مجموعات عالية CD19 ومنخفضة CD19. وبشكل حاسم، بدلاً من مجرد عد دلائل التوجيه الموجودة، قاموا بتسلسل منطقة المعزز المعدلة نفسها مباشرة في كل مجموعة. سمحت أدوات التحليل الجديدة — CRISPR-Millipede وإصدار معدل من برنامج DESeq2 — بمعاملة كل تسلسل حمض نووي معدل مميز كمتغير مستقل واستنتاج إحصائي أي التغيرات على مستوى الحرف الواحد دفعت الخلايا نحو مستويات CD19 أقل أو أعلى. 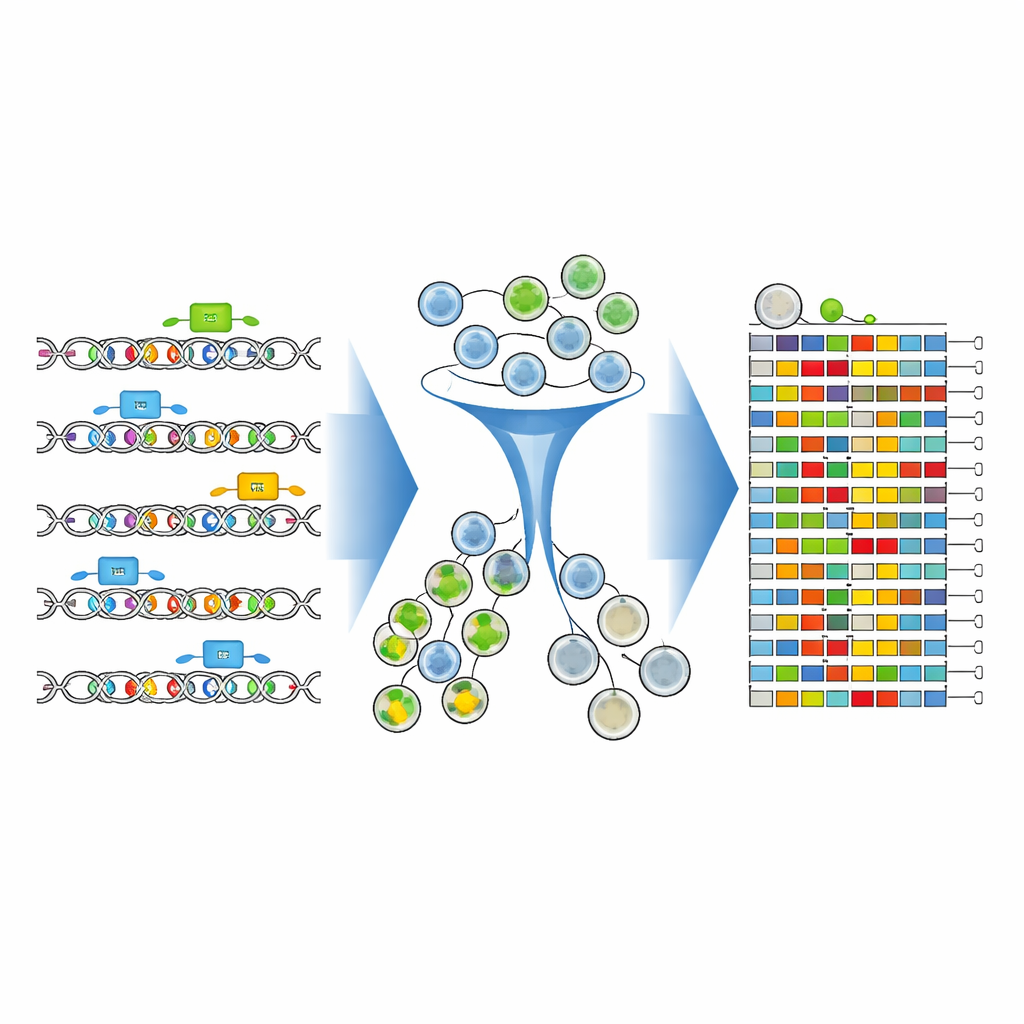
العثور على مواقع ارتكاز البروتينات الرئيسية في المعزز
بوجود خريطة حرفية تلو الأخرى، وضع الباحثون نتائجهم فوق نماذج مواقع ارتكاز عوامل النسخ المعروفة — البروتينات التي ترتبط بالحمض النووي لرفع أو خفض تعبير الجينات. وجدوا أن أكثر الحروف تأثيراً تركزت داخل مواقع يتعرف عليها عوامل مثل MYB وPAX5 وEBF1، وهي منظمات مهمة في خلايا B. بإعادة خلق هذه الطفرات في المعزز عمداً وبإيقاف عوامل النسخ المقابلة، أكدوا أن إتلاف هذه مواقع الارتكاز يخفض مستويات CD19. وأظهروا أيضاً أن بعض النتائج الظاهرة في طرق قديمة قائمة على عد الدلائل كانت نتائج إيجابية كاذبة ناتجة عن مجرد وجود آلية التحرير الضخمة على الحمض النووي بدلاً من تغييرات متسلسلة حقيقية، فصمموا محرراً قابلاً للتحلل لفصل هذه التأثيرات.
كيف يمكن لتغييرات طفيفة في المعزز أن تقوض علاج CAR-T
أخيراً، تساءل الفريق عما إذا كانت هذه التعديلات التنظيمية الدقيقة تؤثر فعلاً على العلاج السرطاني. مزجوا خلايا اللوكيميا المحررة والمعززة بدون الطفرات وتعرضوا لخلايا CD19 CAR-T. نمت الخلايا المعدلة التي تحمل تغييرات معزز محددة باستمرار على حساب نظيراتها غير المعدلة تحت هجوم CAR-T، كاشفة أن الانخفاضات المتواضعة في CD19 — الناجمة ليس عن تحطيم جين CD19 وإنما عن تعديل معززه — كانت كافية لمساعدة خلايا السرطان على البقاء. يبرهن هذا العمل على طريقة عملية وقابلة للتوسع لرسم علاقات السبب والنتيجة على مستوى الحرف الواحد في مناطق التحكم الجيني، ويظهر أن المتغايرات غير المشفرة يمكن أن توجه بصمت نجاح أو فشل العلاجات المناعية المتقدمة.
الاستشهاد: Becerra, B., Wittibschlager, S., Patel, Z.M. et al. Nucleotide-resolution mapping of regulatory elements via allelic readout of tiled base editing. Nat Commun 17, 3398 (2026). https://doi.org/10.1038/s41467-026-69918-8
الكلمات المفتاحية: تحرير قواعد CRISPR, تنظيم الجينات, مقاومة CD19 CAR-T, متغايرات غير مشفرة, تخطيط المعززات