Clear Sky Science · it
Mappatura a risoluzione nucleotidica degli elementi regolatori tramite lettura allelica dell’editing a base a mosaico
Perché piccole modifiche del DNA possono contare nel trattamento del cancro
I medici oncologi si affidano sempre più a terapie immunitarie intelligenti che cercano e distruggono le cellule tumorali riconoscendo specifiche “etichette” sulla loro superficie. Una delle etichette più note sulle cellule leucemiche è CD19, bersaglio di potenti terapie CAR-T. Tuttavia alcuni pazienti hanno ricadute perché le loro cellule tumorali perdono o attenuano silenziosamente questa etichetta, eludendo il trattamento. Questo studio mostra come oggi sia possibile ingrandire le regioni di DNA che controllano CD19, identificando quali singole “lettere” in quei controlli sono importanti per mantenere CD19 visibile — e come cambiamenti in poche di queste lettere possano permettere alle cellule tumorali di sfuggire alla terapia. 
Leggere gli interruttori di controllo dei nostri geni
I geni non sono semplicemente accesi o spenti; sono regolati da interruttori di DNA vicini chiamati enhancer che modulano con precisione la quantità di una proteina prodotta dalla cellula. Molte variazioni del DNA associate a malattie si trovano in queste regioni di controllo non codificanti piuttosto che nei geni che codificano proteine. Gli studi genetici tradizionali possono segnalare regioni sospette ma faticano a dire quali esatte lettere del DNA al loro interno sono critiche, o in che modo influenzano il comportamento cellulare. Per terapie come i CAR-T anti-CD19, questa lacuna è rilevante: una modifica sottile in un interruttore di controllo potrebbe abbassare CD19 quel tanto che basta perché le cellule tumorali si nascondano, senza compromettere il resto della macchina cellulare.
Usare “matite” molecolari per riscrivere il DNA lettera per lettera
I ricercatori hanno messo a punto un flusso sperimentale e computazionale completo per mappare queste lettere critiche del DNA con precisione senza precedenti. Si sono concentrati su un enhancer lungo 346 nucleotidi immediatamente a monte del gene CD19 nelle cellule leucemiche. Utilizzando avanzati editor basici CRISPR — delle “matite” molecolari che possono cambiare singole lettere del DNA senza tagliare il filamento — hanno eseguito una scansione fitta di guide su questo enhancer. Ogni guida mirava a una posizione leggermente diversa, distribuendo collettivamente milioni di cellule con distinte modifiche di una singola lettera e piccole combinazioni di modifiche all’interno dello stesso breve segmento di DNA.
Collegare varianti del DNA ai livelli proteici su larga scala
Per vedere come ogni versione modificata del DNA influenzava CD19, il team ha colorato le cellule con un anticorpo fluorescente che brilla più intensamente quando i livelli di CD19 sono alti. Hanno quindi usato un macchinario di separazione cellulare per dividere la popolazione in gruppi CD19-alto e CD19-basso. Crucialmente, invece di contare solo quali guide erano presenti, hanno sequenziato direttamente la regione enhancer modificata in ciascun gruppo. Nuovi strumenti di analisi — CRISPR-Millipede e una versione adattata del software DESeq2 — hanno permesso di trattare ogni sequenza di DNA modificata distinta come una sua variante e inferire statisticamente quali esatte modifiche di una lettera spostavano le cellule verso livelli più bassi o più alti di CD19. 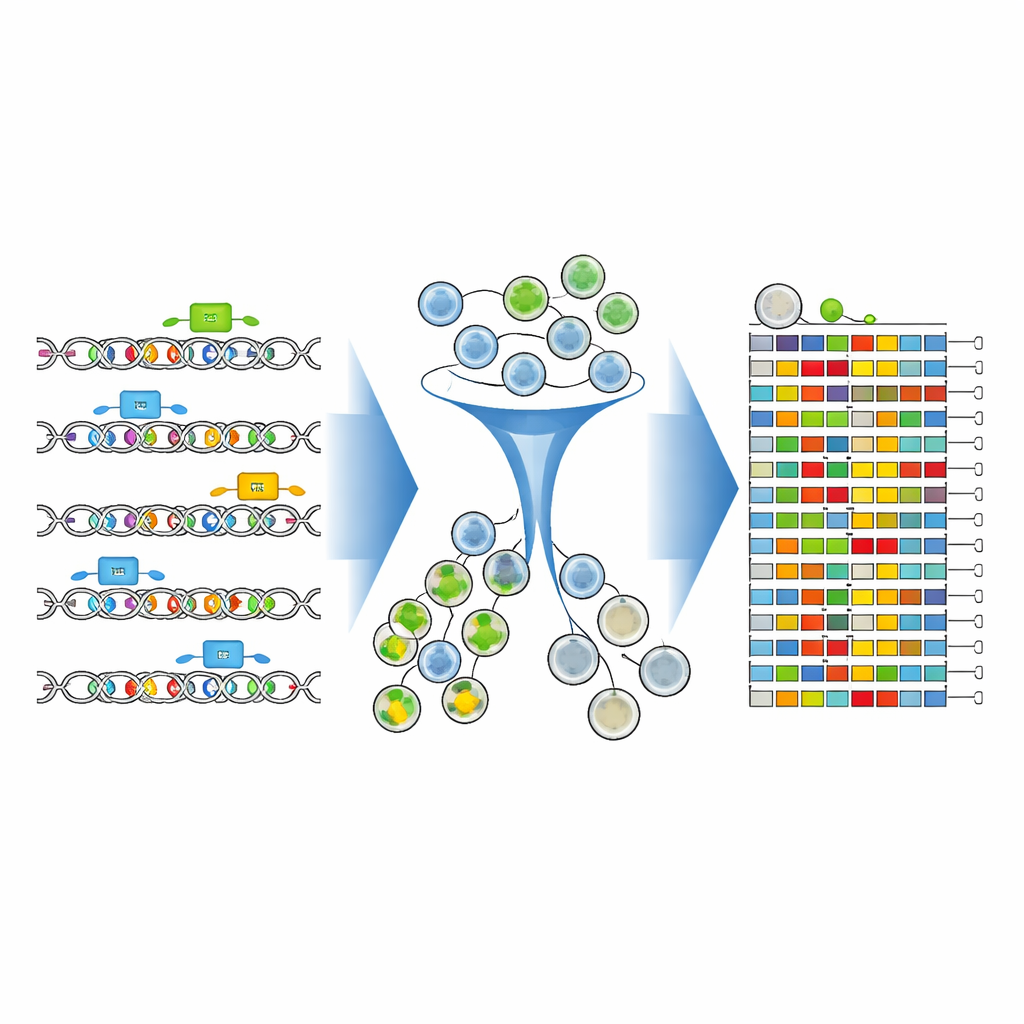
Trovare i siti chiave di ancoraggio delle proteine nell’enhancer
Con questa mappa nucleotide per nucleotide in mano, i ricercatori hanno sovrapposto i risultati con motivi noti di ancoraggio per fattori di trascrizione — proteine che si legano al DNA per aumentare o diminuire l’espressione genica. Hanno scoperto che le lettere con maggiore impatto si raggruppavano all’interno di siti riconosciuti da fattori come MYB, PAX5 ed EBF1, regolatori importanti nelle cellule B. Ricreando deliberatamente queste specifiche mutazioni dell’enhancer e inattivando i corrispondenti fattori di trascrizione, hanno confermato che danneggiare questi siti di legame riduce i livelli di CD19. Hanno inoltre mostrato che alcuni presunti segnali positivi emersi da metodi più vecchi basati sul conteggio delle guide erano falsi positivi dovuti alla mera presenza della massiccia macchina di editing sul DNA piuttosto che a autentici cambiamenti di sequenza, e hanno progettato un editor degradabile per separare questi effetti.
Come piccole modifiche agli enhancer possono compromettere la terapia CAR-T
Infine, il team ha chiesto se questi sottili aggiustamenti regolatori influenzino davvero il trattamento del cancro. Hanno miscelato cellule leucemiche con e senza le mutazioni dell’enhancer ed esposto il tutto a cellule CAR-T anti-CD19. Le cellule editate portatrici di particolari mutazioni dell’enhancer sono sistematicamente cresciute più delle controparti non editate sotto l’attacco CAR-T, rivelando che riduzioni modeste di CD19 — indotte non dalla rottura del gene CD19 ma dalla modifica del suo enhancer — erano sufficienti ad aiutare le cellule tumorali a sopravvivere. Il lavoro dimostra un approccio pratico e scalabile per tracciare causa ed effetto a livello di singola lettera nelle regioni di controllo genico, e mostra che le varianti non codificanti possono silenziosamente indirizzare il successo o il fallimento di immunoterapie all’avanguardia.
Citazione: Becerra, B., Wittibschlager, S., Patel, Z.M. et al. Nucleotide-resolution mapping of regulatory elements via allelic readout of tiled base editing. Nat Commun 17, 3398 (2026). https://doi.org/10.1038/s41467-026-69918-8
Parole chiave: Editing basico CRISPR, regolazione genica, resistenza CD19 CAR-T, varianti non codificanti, mappatura degli enhancer