Clear Sky Science · es
Mapeo a resolución de nucleótido de elementos regulatorios mediante lectura alélica de edición por nucleótido en mosaico
Por qué pequeños cambios en el ADN pueden importar para el tratamiento del cáncer
Los oncólogos confían cada vez más en terapias inmunitarias sofisticadas que persiguen a las células tumorales reconociendo etiquetas específicas en su superficie. Una de las etiquetas más conocidas en las células leucémicas se llama CD19, el objetivo de potentes terapias CAR-T. Sin embargo, algunos pacientes recaen porque sus células cancerosas pierden o atenúan esa etiqueta, escapando al tratamiento. Este estudio muestra cómo los científicos pueden ahora acercarse a tramos de ADN que controlan CD19, identificando qué «letras» individuales en esas regiones reguladoras son importantes para mantener CD19 visible —y cómo cambios en solo unas pocas de esas letras pueden ayudar a las células cancerosas a evadir la terapia. 
Leer los interruptores de control de nuestros genes
Los genes no están simplemente activados o desactivados; se controlan mediante interruptores de ADN cercanos llamados enhancers que afinan la cantidad de una proteína que produce una célula. Muchos cambios de ADN asociados a enfermedades se encuentran en estas regiones de control no codificantes en lugar de en los propios genes que codifican proteínas. Los estudios genéticos tradicionales pueden señalar regiones sospechosas pero tienen dificultades para decir exactamente qué letras del ADN dentro de ellas son críticas, o cómo afectan al comportamiento celular. Para terapias como las CAR-T contra CD19, esta laguna es importante: un cambio sutil en un interruptor de control podría reducir CD19 lo justo para que las células cancerosas se oculten, sin alterar el resto de la maquinaria celular.
Usar «lápices» moleculares para reescribir el ADN una letra a la vez
Los investigadores construyeron un marco experimental y computacional integral para cartografiar estas letras de ADN cruciales con precisión sin precedentes. Se centraron en un enhancer de 346 letras situado justo aguas arriba del gen CD19 en células leucémicas. Usando editores de bases CRISPR avanzados —«lápices» moleculares que pueden cambiar letras individuales del ADN sin cortar la molécula— recorrieron este enhancer con una biblioteca densa de guías. Cada guía apuntaba a un punto ligeramente distinto, esparciendo colectivamente millones de células con cambios de una sola letra y pequeñas combinaciones de cambios dentro del mismo segmento corto de ADN.
Relacionar variantes de ADN con niveles de proteína a gran escala
Para ver cómo cada versión editada del ADN afectaba a CD19, el equipo tiñó las células con un anticuerpo fluorescente que brilla más cuando los niveles de CD19 son altos. Luego usaron una máquina clasificadora de células para dividir la población en grupos con CD19 alto y CD19 bajo. De forma crucial, en lugar de limitarse a contar qué guías estaban presentes, secuenciaron directamente la región del enhancer editada en cada grupo. Nuevas herramientas de análisis —CRISPR-Millipede y una versión adaptada del software DESeq2— les permitieron tratar cada secuencia editada distinta como su propia variante e inferir estadísticamente qué cambios de una sola letra desviaban a las células hacia niveles más bajos o más altos de CD19. 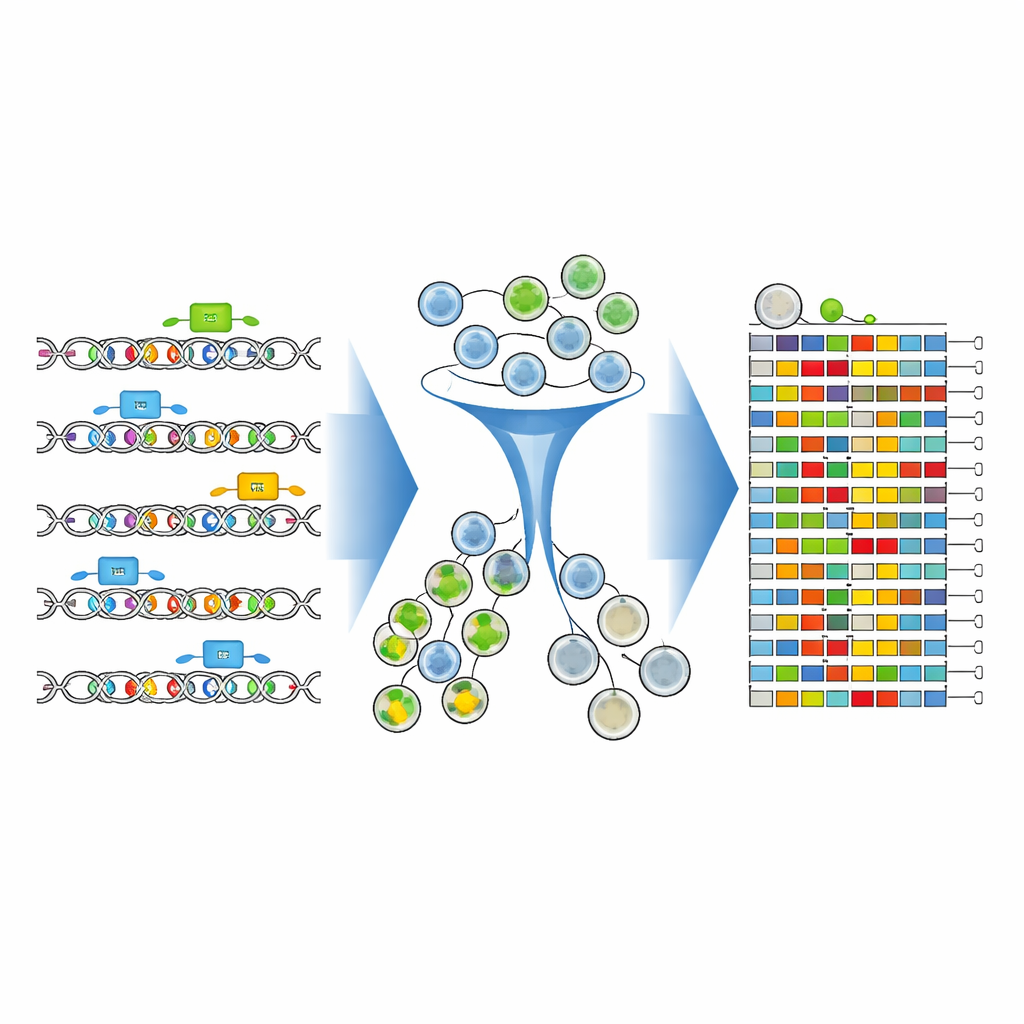
Encontrar los sitios clave de anclaje de proteínas en el enhancer
Con este mapa nucleótido por nucleótido en la mano, los investigadores superpusieron sus resultados con motivos de unión conocidos para factores de transcripción —proteínas que se fijan al ADN para activar o reprimir genes. Encontraron que las letras más impactantes se concentraban dentro de sitios reconocidos por factores como MYB, PAX5 y EBF1, que son reguladores importantes en células B. Recreando deliberadamente estas mutaciones específicas del enhancer y deshabilitando los factores de transcripción correspondientes, confirmaron que dañar estos sitios de anclaje reduce los niveles de CD19. También mostraron que algunos éxitos aparentes de métodos anteriores basados en el recuento de guías eran falsos positivos causados por la mera presencia de la voluminosa maquinaria de edición sobre el ADN y no por cambios genuinos en la secuencia, y diseñaron un editor degradable para separar estos efectos.
Cómo pequeños cambios en enhancers pueden socavar la terapia CAR-T
Finalmente, el equipo preguntó si estos ajustes regulatorios sutiles realmente influyen en el tratamiento del cáncer. Mezclaron células leucémicas con y sin las mutaciones del enhancer y las expusieron a células CAR-T dirigidas a CD19. Las células editadas que llevaban ciertos cambios en el enhancer crecieron consistentemente más que sus contrapartes no editadas bajo el ataque CAR-T, revelando que reducciones moderadas en CD19 —provocadas no por romper el gen CD19 sino por alterar su enhancer— fueron suficientes para ayudar a las células cancerosas a sobrevivir. El trabajo demuestra una forma práctica y escalable de trazar causa y efecto a nivel de letra en regiones de control génico, y muestra que las variantes no codificantes pueden dirigir silenciosamente el éxito o el fracaso de inmunoterapias de vanguardia.
Cita: Becerra, B., Wittibschlager, S., Patel, Z.M. et al. Nucleotide-resolution mapping of regulatory elements via allelic readout of tiled base editing. Nat Commun 17, 3398 (2026). https://doi.org/10.1038/s41467-026-69918-8
Palabras clave: Edición de bases CRISPR, regulación génica, resistencia CD19 CAR-T, variantes no codificantes, cartografía de enhancers