Clear Sky Science · pl
Mapowanie elementów regulacyjnych z rozdzielczością nukleotydową poprzez alleliczne odczytywanie przy użyciu kafelkowego edytowania zasad
Dlaczego drobne zmiany w DNA mogą mieć znaczenie dla leczenia raka
Lekarze onkologowie coraz częściej polegają na wysublimowanych terapiach immunologicznych, które tropią komórki nowotworowe, rozpoznając specyficzne znaczniki na ich powierzchni. Jednym z najlepiej znanych znaczników na komórkach białaczkowych jest CD19 — cel silnych terapii CAR-T. Jednak niektórzy pacjenci doświadczają wznowy, ponieważ komórki nowotworowe po cichu tracą lub przyciemniają ten znacznik, wymykając się leczeniu. To badanie pokazuje, jak naukowcy mogą teraz przybliżyć się do odcinków DNA kontrolujących CD19, wskazując pojedyncze „literki” w tych regionach regulacyjnych, które decydują o widoczności CD19 — i jak zmiany zaledwie kilku takich liter mogą pomóc komórkom nowotworowym uniknąć terapii. 
Odczytywanie przełączników kontrolujących geny
Geny nie są po prostu włączone lub wyłączone; sterują nimi pobliskie przełączniki DNA zwane enhancerami, które precyzyjnie regulują, ile danego białka komórka wytwarza. Wiele zmian DNA związanych z chorobami występuje w tych niekodujących regionach kontrolnych, a nie w samych genach kodujących białka. Tradycyjne badania genetyczne potrafią wskazać podejrzane obszary, ale mają trudność z określeniem, które dokładnie litery DNA w ich obrębie są krytyczne i jak wpływają na zachowanie komórki. Dla terapii takich jak CD19 CAR-T luka ta jest istotna: subtelna zmiana w przełączniku kontrolnym może obniżyć poziom CD19 na tyle, by komórki nowotworowe się ukryły, pozostawiając resztę mechanizmów komórkowych nienaruszoną.
Używanie molekularnych ołówków do przepisywania DNA po jednej literze
Naukowcy zbudowali kompleksowe ramy eksperymentalne i obliczeniowe, aby zmapować te kluczowe litery DNA z bezprecedensową precyzją. Skoncentrowali się na 346-literowym enhancerze tuż powyżej genu CD19 w komórkach białaczkowych. Wykorzystując zaawansowane edytory zasad CRISPR — molekularne „ołówki”, które mogą zmieniać pojedyncze litery DNA bez przecinania nici — przeszukali ten enhancer gęstą biblioteką molekuł prowadzących. Każdy prowadnik celował w nieco inne miejsce, wspólnie obsiewając miliony komórek odrębnymi pojedynczymi zmianami literowymi oraz niewielkimi kombinacjami zmian w tym samym krótkim odcinku DNA.
Łączenie wariantów DNA z poziomami białka w populacji
Aby sprawdzić, jak każda zedytowana wersja DNA wpływa na CD19, zespół znakował komórki fluorescencyjnym przeciwciałem, które świeci silniej przy wysokich poziomach CD19. Następnie użyli sortera komórek, by podzielić populację na grupy z wysokim i niskim poziomem CD19. Kluczowe było to, że zamiast tylko liczyć obecność prowadników, bezpośrednio sekwencjonowali zmodyfikowany region enhancera w każdej grupie. Nowe narzędzia analityczne — CRISPR-Millipede i zaadaptowana wersja oprogramowania DESeq2 — pozwoliły traktować każdą odrębną zedytowaną sekwencję DNA jako własny wariant i statystycznie wywnioskować, które dokładne zmiany pojedynczych liter przesuwały komórki w stronę niższego lub wyższego poziomu CD19. 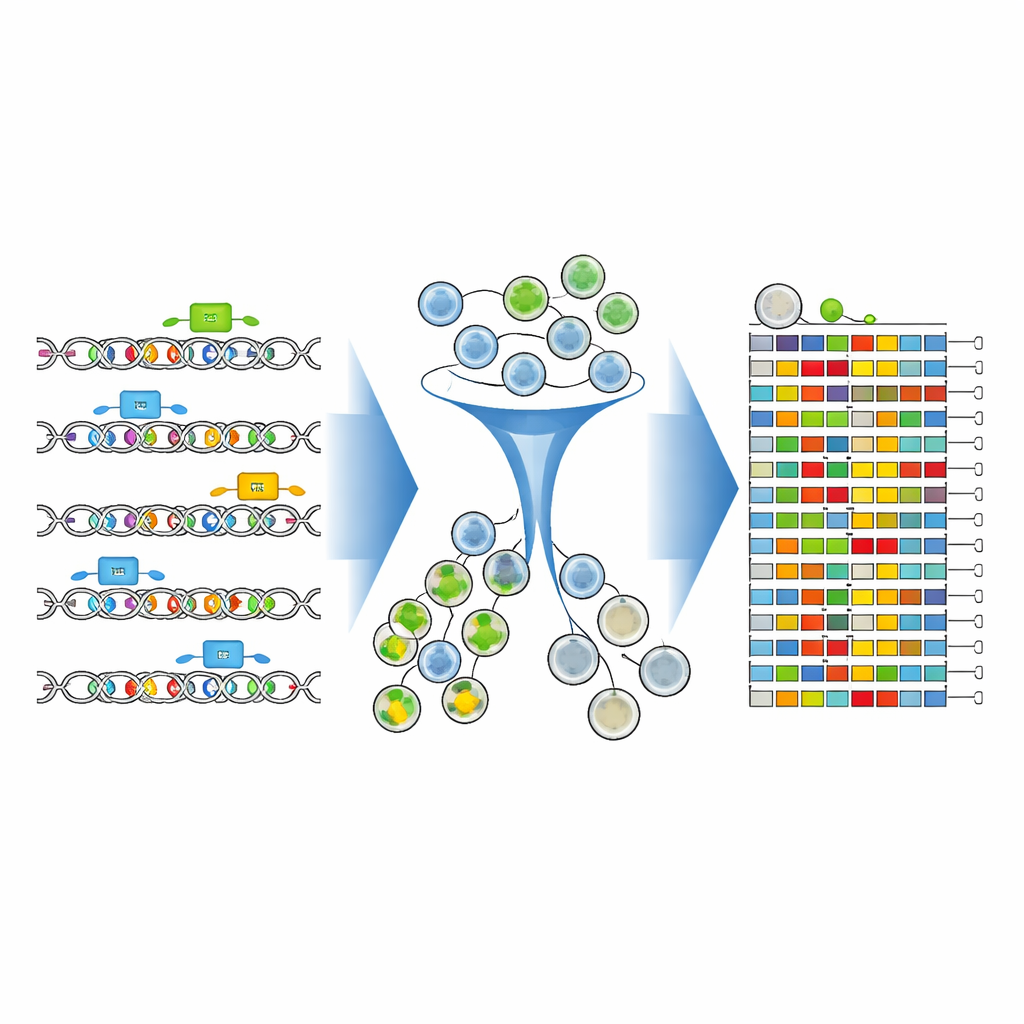
Odnalezienie kluczowych miejsc dokowania białek w enhancerze
Dysponując mapą na poziomie nukleotydu, badacze zestawili swoje wyniki z znanymi motywami dokowania dla czynników transkrypcyjnych — białek, które wiążą DNA, by zwiększać lub zmniejszać ekspresję genów. Odkryli, że najbardziej wpływowe litery skupiały się wewnątrz miejsc rozpoznawanych przez czynniki takie jak MYB, PAX5 i EBF1, które są ważnymi regulatorami w komórkach B. Poprzez celowe odtworzenie tych specyficznych mutacji enhancera oraz wyłączenie odpowiadających im czynników transkrypcyjnych, potwierdzili, że uszkodzenie tych miejsc dokowania obniża poziom CD19. Pokaźna część pozornych trafień z wcześniejszych metod opartych na liczbie prowadników okazała się fałszywie dodatnia — wynikała z samej obecności masywnego sprzętu edytującego na DNA, a nie z rzeczywistych zmian sekwencji — więc zespół opracował degradowalny edytor, by rozdzielić te efekty.
Jak drobne zmiany enhancerów mogą podkopywać terapię CAR-T
Na koniec badacze sprawdzili, czy te subtelne modyfikacje regulacyjne faktycznie wpływają na leczenie. Wymieszali komórki białaczkowe z i bez mutacji w enhancerze i wystawili je na działanie komórek CD19 CAR-T. Komórki z określonymi zmianami w enhancerze konsekwentnie wypierały swoje niezmodyfikowane odpowiedniki pod atakiem CAR-T, ujawniając, że umiarkowane obniżenia CD19 — spowodowane nie uszkodzeniem genu CD19, lecz zmianą jego enhancera — wystarczają, by pomóc komórkom nowotworowym przetrwać. Praca demonstruje praktyczną, skalowalną metodę mapowania przyczyn i skutków na poziomie pojedynczej litery w regionach kontrolnych genów oraz pokazuje, że warianty niekodujące mogą po cichu decydować o powodzeniu lub niepowodzeniu nowoczesnych immunoterapii.
Cytowanie: Becerra, B., Wittibschlager, S., Patel, Z.M. et al. Nucleotide-resolution mapping of regulatory elements via allelic readout of tiled base editing. Nat Commun 17, 3398 (2026). https://doi.org/10.1038/s41467-026-69918-8
Słowa kluczowe: Edytowanie zasad CRISPR, regulacja genów, oporność na CD19 CAR-T, warianty niekodujące, mapowanie enhancerów