Clear Sky Science · de
Nukleotidgenaue Kartierung von Regulatorischen Elementen über allelische Auslese mit getiltem Basenediting
Warum winzige DNA-Veränderungen für die Krebsbehandlung wichtig sein können
Krebsärzte setzen zunehmend auf intelligente Immuntherapien, die Tumorzellen anhand spezifischer Marker auf ihrer Oberfläche aufspüren. Einer der bekanntesten Marker auf Leukämiezellen heißt CD19 und ist Ziel mächtiger CAR-T-Zelltherapien. Dennoch erleiden manche Patientinnen und Patienten Rückfälle, weil ihre Krebszellen diesen Marker leise verlieren oder abschwächen und so der Behandlung entgehen. Diese Studie zeigt, wie Wissenschaftler nun in DNA-Abschnitte hineinzoomen können, die CD19 steuern, und genau bestimmen, welche einzelnen „Buchstaben“ in diesen Kontrollregionen dafür entscheidend sind, CD19 sichtbar zu halten — und wie Veränderungen an nur wenigen dieser Buchstaben Krebszellen helfen können, der Therapie zu entkommen. 
Die Schaltknöpfe unserer Gene lesen
Gene sind nicht einfach ein- oder ausgeschaltet; sie werden von benachbarten DNA-Schaltern, sogenannten Enhancern, gesteuert, die fein regulieren, wie viel eines bestimmten Proteins eine Zelle herstellt. Viele krankheitsassoziierte DNA-Veränderungen liegen in diesen nicht-kodierenden Kontrollregionen und nicht in den protein-codierenden Genen selbst. Traditionelle genetische Studien können verdächtige Regionen markieren, tun sich aber schwer damit, genau zu sagen, welche DNA-Buchstaben innerhalb dieser Regionen kritisch sind oder wie sie das Zellverhalten beeinflussen. Für Therapien wie CD19 CAR-T-Zellen ist diese Lücke wichtig: Eine subtile Änderung in einem Kontrollschalter könnte CD19 gerade genug reduzieren, damit Krebszellen sich verstecken, während der Rest der Zellmaschinerie intakt bleibt.
Molekulare Stifte, um DNA Buchstabe für Buchstabe umzuschreiben
Die Forschenden entwickelten einen durchgängigen experimentellen und rechnerischen Rahmen, um diese entscheidenden DNA-Buchstaben mit beispielloser Präzision zu kartieren. Sie konzentrierten sich auf einen 346 Buchstaben langen Enhancer direkt stromaufwärts des CD19-Gens in Leukämiezellen. Mit fortschrittlichen CRISPR-Baseneditoren — molekularen „Stiften“, die einzelne DNA-Buchstaben ändern können, ohne die DNA zu schneiden — fuhren sie mit einer dichten Bibliothek von Führungsmolekülen über diesen Enhancer. Jede Guide-Sequenz zielte auf eine leicht andere Stelle, sodass Millionen von Zellen jeweils unterschiedliche Einzelbuchstabenänderungen und kleine Kombinationen von Änderungen innerhalb desselben kurzen DNA-Abschnitts erhielten.
DNA-Varianten mit Proteinspiegeln in Masse verknüpfen
Um zu sehen, wie jede editierte DNA-Version CD19 beeinflusste, färbte das Team die Zellen mit einem fluoreszierenden Antikörper, der umso stärker leuchtet, je höher die CD19-Werte sind. Anschließend nutzten sie eine Durchflusszytometrie, um die Population in CD19-hohe und CD19-niedrige Gruppen zu trennen. Entscheidend war, dass sie statt nur die Präsenz der Guides zu zählen, die editierte Enhancer-Region selbst in jeder Gruppe direkt sequenzierten. Neue Analysetools — CRISPR-Millipede und eine angepasste Version der DESeq2-Software — ermöglichten es ihnen, jede unterscheidbare editierte DNA-Sequenz als eigene Variante zu behandeln und statistisch zu bestimmen, welche exakten Einzelbuchstabenänderungen Zellen in Richtung niedrigerem oder höherem CD19 verschoben. 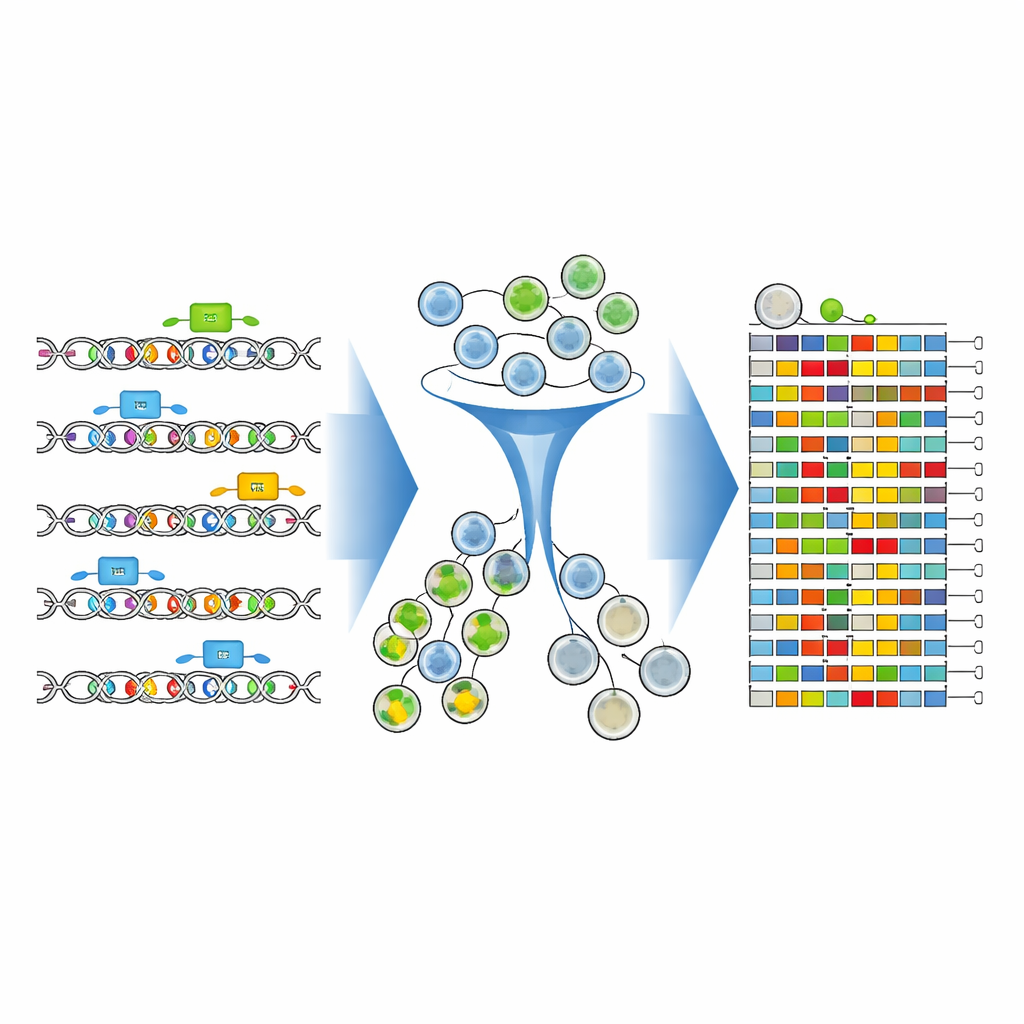
Die wichtigen Protein-Docking-Stellen im Enhancer finden
Mithilfe dieser Nukleotid-für-Nukleotid-Karte überlagerten die Forschenden ihre Ergebnisse mit bekannten Bindungsmotiven für Transkriptionsfaktoren — Proteine, die an DNA binden, um Gene ein- oder auszuschalten. Sie fanden, dass die wirkungsvollsten Buchstaben sich in Bereichen häuften, die von Faktoren wie MYB, PAX5 und EBF1 erkannt werden, die wichtige Regulatoren in B-Zellen sind. Durch gezielte Nachbildung dieser spezifischen Enhancer-Mutationen und durch Deaktivierung der entsprechenden Transkriptionsfaktoren bestätigten sie, dass das Beschädigen dieser Bindungsstellen CD19 senkt. Sie zeigten außerdem, dass einige scheinbare Treffer früherer, guide-basierten Methoden falsch positiv waren — verursacht durch das bloße Vorhandensein der sperrigen Editiermaschinerie auf der DNA statt durch echte Sequenzänderungen — und entwickelten einen abbaubaren Editor, um diese Effekte zu trennen.
Wie kleine Enhancer-Änderungen CAR-T-Therapien untergraben können
Schließlich prüfte das Team, ob diese subtilen regulatorischen Anpassungen tatsächlich die Krebsbehandlung beeinflussen. Sie mischten Leukämiezellen mit und ohne Enhancer-Mutationen und setzten sie CD19 CAR-T-Zellen aus. Unter CAR-T-Angriff wuchsen die editierten Zellen mit bestimmten Enhancer-Änderungen konsequent stärker als ihre uneditierten Gegenstücke, was zeigt, dass moderate Reduktionen von CD19 — nicht durch das Zerbrechen des CD19-Gens, sondern durch Veränderung seines Enhancers verursacht — ausreichen, um Krebszellen das Überleben zu ermöglichen. Die Arbeit demonstriert eine praktische, skalierbare Methode, um Ursache und Wirkung auf Einzelbuchstaben-Ebene in Genkontrollregionen zu ermitteln, und zeigt, dass nicht-kodierende Varianten den Erfolg oder Misserfolg hochmoderner Immuntherapien unbemerkt beeinflussen können.
Zitation: Becerra, B., Wittibschlager, S., Patel, Z.M. et al. Nucleotide-resolution mapping of regulatory elements via allelic readout of tiled base editing. Nat Commun 17, 3398 (2026). https://doi.org/10.1038/s41467-026-69918-8
Schlüsselwörter: CRISPR-Basenediting, Genregulation, CD19 CAR-T-Resistenz, nicht-kodierende Varianten, Enhancer-Kartierung