Clear Sky Science · pt
Mapeamento em resolução de nucleotídeo de elementos regulatórios via leitura alélica de edição em bloco por bases
Por que pequenas mudanças no DNA podem importar para o tratamento do câncer
Médicos que tratam câncer confiam cada vez mais em terapias imunes sofisticadas que caçam células tumorais reconhecendo marcadores específicos na sua superfície. Um dos marcadores mais conhecidos em células de leucemia é o CD19, alvo de poderosas terapias de células CAR-T. Ainda assim, alguns pacientes têm recaída porque as células cancerosas perdem ou diminuem discretamente esse marcador, escapando do tratamento. Este estudo mostra como os cientistas agora podem ampliar segmentos do DNA que controlam o CD19, identificando quais “letras” individuais nessas regiões regulatórias são importantes para manter o CD19 visível — e como alterações em apenas algumas dessas letras podem ajudar as células cancerosas a escapar da terapia. 
Lendo os interruptores de controle dos nossos genes
Genes não estão simplesmente ligados ou desligados; são controlados por interruptores de DNA próximos chamados enhancers, que ajustam quanto de uma dada proteína a célula produz. Muitas mudanças de DNA associadas a doenças residem nessas regiões regulatórias não codificantes, em vez de nos próprios genes codificadores de proteína. Estudos genéticos tradicionais conseguem sinalizar regiões suspeitas, mas têm dificuldade para dizer exatamente quais letras do DNA dentro delas são críticas ou como afetam o comportamento celular. Para terapias como as de CAR-T contra CD19, essa lacuna é importante: uma pequena alteração em um interruptor regulatório pode reduzir o CD19 o bastante para que as células cancerosas se escondam, mantendo intacto o restante da maquinaria celular.
Usando “lápis” moleculares para reescrever o DNA letra por letra
Os pesquisadores construíram uma estrutura experimental e computacional completa para mapear essas letras cruciais do DNA com precisão sem precedentes. Eles se concentraram em um enhancer de 346 letras logo a montante do gene CD19 em células de leucemia. Usando editores de base CRISPR avançados — “lápis” moleculares que podem alterar letras individuais do DNA sem cortar a dupla hélice — eles varreram esse enhancer com uma biblioteca densa de moléculas guia. Cada guia mirava um ponto ligeiramente diferente, coletivamente pulverizando milhões de células com mudanças distintas de uma única letra e pequenas combinações de mudanças dentro do mesmo segmento curto de DNA.
Ligando variantes de DNA a níveis de proteína em massa
Para ver como cada versão editada do DNA afetava o CD19, a equipe corou as células com um anticorpo fluorescente que brilha mais intensamente quando os níveis de CD19 são altos. Em seguida, usaram um equipamento de separação celular para dividir a população em grupos de CD19-alto e CD19-baixo. Crucialmente, em vez de apenas contar quais guias estavam presentes, eles sequenciaram diretamente a região do enhancer editado em cada grupo. Ferramentas analíticas novas — CRISPR-Millipede e uma versão adaptada do software DESeq2 — permitiram tratar cada sequência de DNA editada e distinta como sua própria variante e inferir estatisticamente quais mudanças exatas de uma letra deslocaram as células para níveis menores ou maiores de CD19. 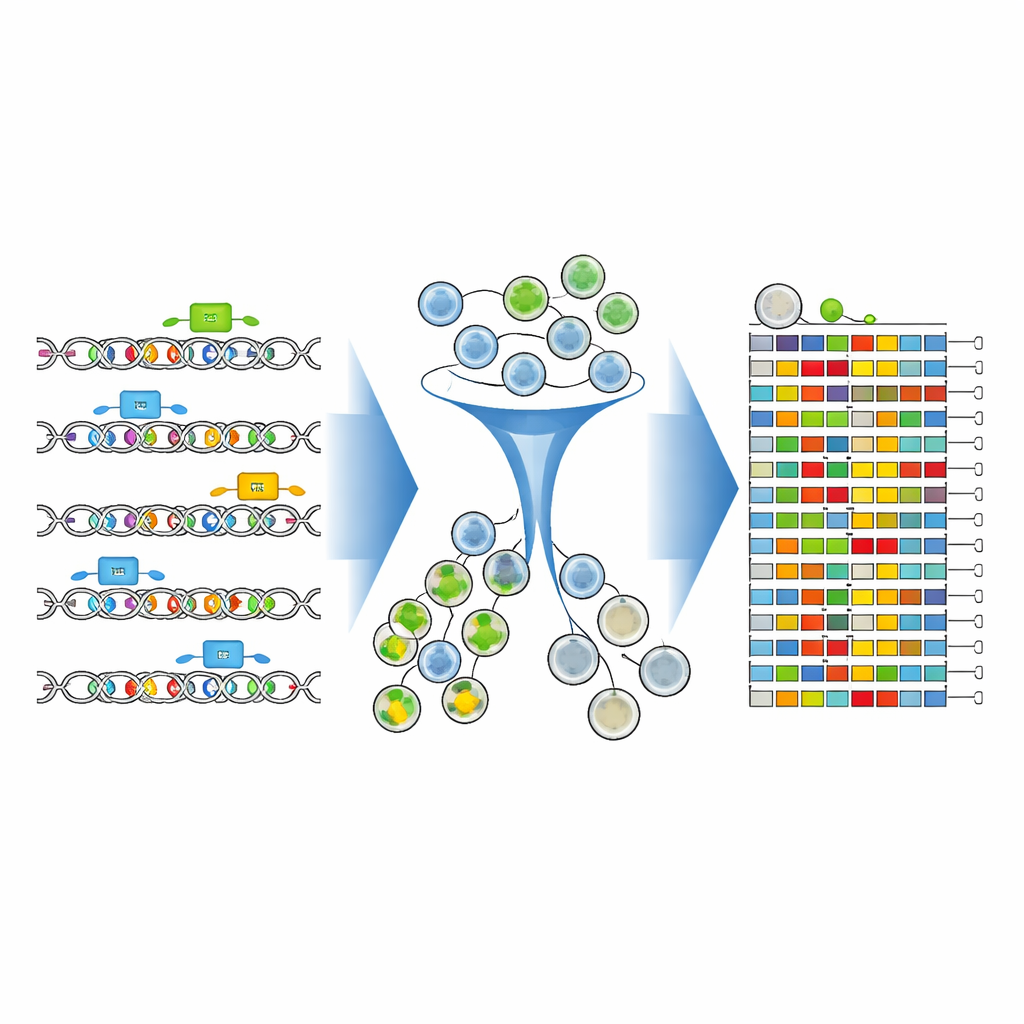
Encontrando os locais-chave de ancoragem de proteínas no enhancer
Com esse mapa nucleotídeo a nucleotídeo em mãos, os pesquisadores sobrepuseram seus resultados a motivos de ancoragem conhecidos para fatores de transcrição — proteínas que se ligam ao DNA para ativar ou reprimir genes. Eles descobriram que as letras com maior impacto se agrupavam dentro de sítios reconhecidos por fatores como MYB, PAX5 e EBF1, reguladores importantes em células B. Recriando deliberadamente essas mutações específicas do enhancer e desabilitando os fatores de transcrição correspondentes, confirmaram que danificar esses sítios de ancoragem reduz os níveis de CD19. Também mostraram que alguns resultados aparentes de métodos mais antigos, baseados na contagem de guias, eram falsos positivos causados apenas pela presença do volumoso maquinário de edição sobre o DNA, e desenvolveram um editor degradável para separar esses efeitos.
Como pequenas mudanças em enhancers podem minar a terapia CAR-T
Por fim, a equipe investigou se esses ajustes regulatórios sutis realmente influenciam o tratamento do câncer. Misturaram células de leucemia com e sem as mutações no enhancer e as expuseram a células CAR-T contra CD19. Células editadas que carregavam certas mudanças no enhancer consistentemente proliferaram mais que suas contrapartes não editadas sob ataque CAR-T, revelando que reduções modestas no CD19 — provocadas não pela quebra do gene CD19, mas pela alteração do seu enhancer — foram suficientes para ajudar as células cancerosas a sobreviver. O trabalho demonstra uma maneira prática e escalável de traçar causa e efeito ao nível de uma única letra em regiões de controle gênico, e mostra que variantes não codificantes podem, silenciosamente, direcionar o sucesso ou o fracasso de imunoterapias de ponta.
Citação: Becerra, B., Wittibschlager, S., Patel, Z.M. et al. Nucleotide-resolution mapping of regulatory elements via allelic readout of tiled base editing. Nat Commun 17, 3398 (2026). https://doi.org/10.1038/s41467-026-69918-8
Palavras-chave: Edição de bases CRISPR, regulação gênica, resistência de CAR-T contra CD19, variantes não codificantes, mapeamento de enhancers