Clear Sky Science · he
מיפוי ברזולוציית נוקלאוטיד של אלמנטים רגולטוריים באמצעות קריאה אללאלית של עריכה בז׳והרת
מדוע שינויים זעירים ב-DNA יכולים להשפיע על טיפול בסרטן
רופאי סרטן נשענים יותר ויותר על טיפולים חיסוניים מתקדמים שמאתרים תאי גידול על ידי זיהוי סימנים ספציפיים על פני התא. אחד הסימנים המוכרים בתאי לוקמיה נקרא CD19, מטרה של טיפולי CAR-T רבי עוצמה. עם זאת, בחלק מהחולים המחלה חוזרת משום שתאי הסרטן מאבדים או מדממים בעדינות את הסימן הזה ונמנעים מהטיפול. המחקר הזה מראה כיצד מדענים יכולים עכשיו להתמקד באזורים של DNA שמווסתים את CD19, לזהות אילו "אותיות" בודדות באזורי הבקרה הללו חשובות לשמירה על נראות CD19 — וכיצד שינויים בכמה אותיות בלבד יכולים לאפשר לתאי סרטן להמלט מהטיפול. 
קריאת מתגי הבקרה של הגנים שלנו
גנים אינם פשוטים דלוקים או כבויים; הם נשלטים על ידי מתגי DNA סמוכים המכונים אנחנסרים שמדייקים כמה חלבון התא מייצר. שינויים רבים הקשורים למחלות נמצאים באזורים לא מקודדים אלה של הבקרה ולא בתוך הגנים שמקודדים חלבון. מחקרים גנטיים מסורתיים יכולים לסמן אזורים חשודים אך מתקשים לומר בדיוק אילו אותיות DNA בתוך האזור קריטיות, או כיצד הן משפיעות על התנהגות התא. עבור טיפולים כמו CAR-T המכוונים ל-CD19, הפער הזה חשוב: שינוי עדין במתג בקרה עלול להוריד את רמת CD19 במידה שמספיקה כדי להסתיר את התאים הסרטניים, תוך שמירה על יתר פעילות התא.
שימוש בעפרונות מולקולריים כדי לשכתב DNA אות אחת בכל פעם
החוקרים בנו מסגרת ניסויית ומחשובית מקצה לקצה כדי למפות אותיות DNA מכריעות אלה ברזולוציה חסרת תקדים. הם התמקדו באנחנסר באורך 346 אותיים שממוקם מייד לפני גן ה-CD19 בתאי לוקמיה. באמצעות עורכי בסיס מתקדמים של CRISPR — "עפרונות" מולקולריים שיכולים לשנות אות אחת ב-DNA בלי לחתוך את ה-DNA — הם סרקו את האנחנסר בספרייה צפופה של מולקולות מנחות. כל מנחה כוונה למיקום מעט שונה, וביחד הם פיזרו מיליוני תאים עם שינויים של אות אחת ושילובים קטנים של שינויים בתוך אותו מקטע קצר של DNA.
קישור וריאנטים בדנ״א לרמות החלבון באוכלוסייה
כדי לראות כיצד כל גרסת DNA ערוכה השפיעה על CD19, הצוות צבע את התאים בנוגדן פלואורסצנטי שמאיר בעוצמה גבוהה יותר כאשר רמת CD19 גבוהה. לאחר מכן השתמשו במכונת מיון תאים כדי לחלק את האוכלוסייה לקבוצות של CD19-גבוה ו-CD19-נמוך. קריטי לכך, במקום לספור רק אילו מנחות היו נוכחות, הם רצפו ישירות את אזור האנחנסר הערוך עצמו בכל קבוצה. כלי ניתוח חדשים — CRISPR-Millipede וגרסה מותאמת של תוכנת DESeq2 — איפשרו להם להתייחס לכל רצף DNA ערוך כמחולל נפרד ולהסיק סטטיסטית אילו שינויים של אות אחת הזיזו תאים לעבר רמות CD19 נמוכות או גבוהות יותר. 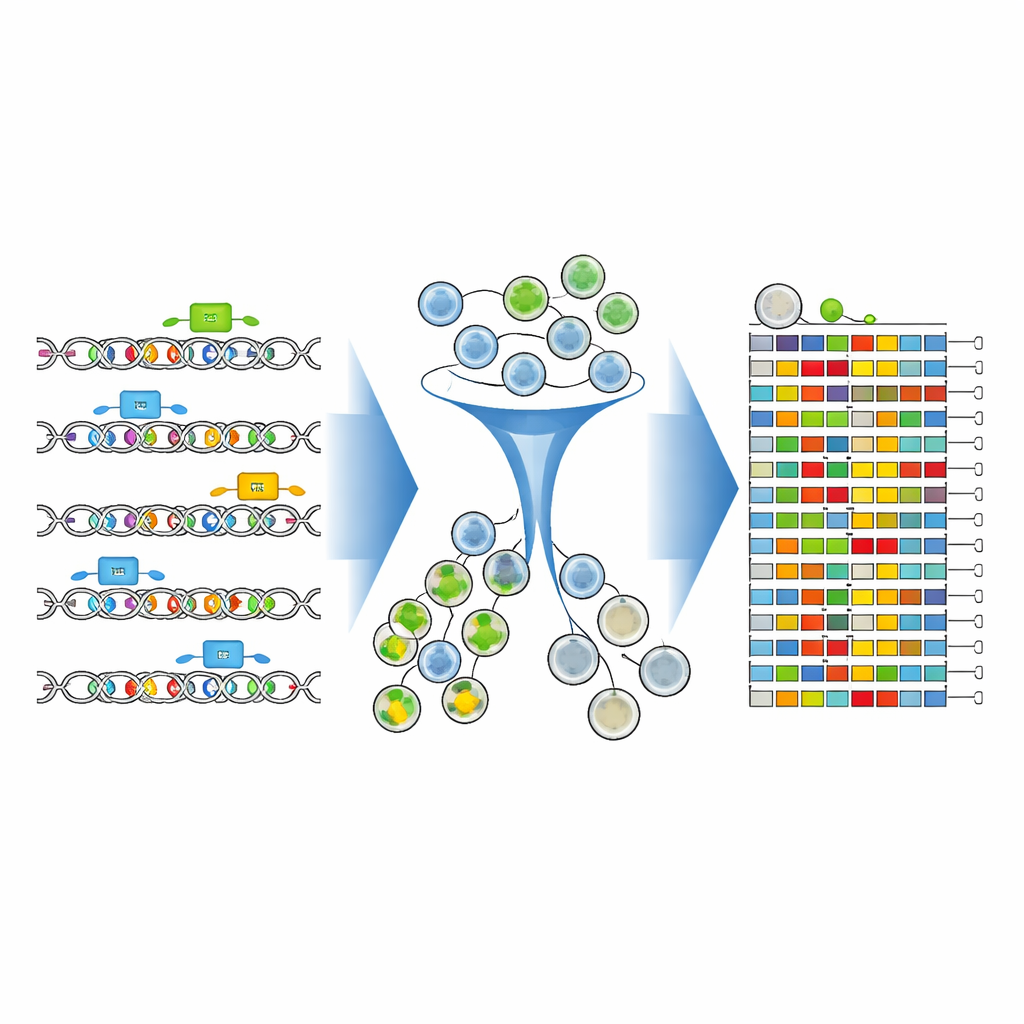
מציאת אתרי העגינה החלבוניים המרכזיים באנחנסר
עם המפה נוקלאוטיד אחר נוקלאוטיד הזו ביד, החוקרים חיפו את התוצאות שלהם על פני מוטיבים ידועים לקישור של גורמי שעתוק — חלבונים הקושרים DNA כדי לכוון ביטוי גנים כלפי מעלה או מטה. הם מצאו שהאותיות עם ההשפעה הגדולה ביותר התקבצו בתוך אתרים שמוכרים על ידי גורמים כמו MYB, PAX5 ו-EBF1, שהם רגולטורים חשובים בתאי B. על ידי שיחזור מכוון של מוטציות אלה באנחנסר ובהשבתה של גורמי השעתוק המתאימים, הם אישרו שפגיעה באתרי העגינה הללו מורידה את רמות CD19. הם גם הראו שחלק מהממצאים הנראים בשיטות ישנות שהתבססו על ספירת מנחות היו חיוביים שגויים שנבעו מהימצאות גוף העריכה הגדול על ה-DNA ולא משינויים רציניים של הרצף, ופיתחו עורך ניתן להרס כדי להפריד בין ההשפעות הללו.
כיצד שינויים קטנים באנחנסר יכולים לערער את תרופת CAR-T
לבסוף, הצוות בדק האם ההתאמות הרגולטוריות העדינות האלה משפיעות באמת על טיפול בסרטן. הם ערבבו תאי לוקמיה עם ובלא המוטציות באנחנסר וחשפו אותם לתאי CAR-T המכוונים ל-CD19. תאים שעברו עריכה וששינוים מסוימים באנחנסר גברו בעקביות על עמיתיהם שלא נערכו תחת מתקפת CAR-T, והדגימו שהפחתות צנועות ב-CD19 — הנגרמות לא על ידי שבירת גן ה-CD19 עצמו אלא על ידי שינוי האנחנסר שלו — הספיקו כדי לסייע לתאי סרטן לשרוד. העבודה ממחישה דרך פרקטית וסקלאבילית למפות יחסי סיבה ותוצאה ברמת האות היחיד באזורי בקרה של גנים, ומדגימה שווריאנטים לא מקודדים יכולים לשנות בדממה את הצלחתם או כישלונם של אימונותרפיות מתקדמות.
ציטוט: Becerra, B., Wittibschlager, S., Patel, Z.M. et al. Nucleotide-resolution mapping of regulatory elements via allelic readout of tiled base editing. Nat Commun 17, 3398 (2026). https://doi.org/10.1038/s41467-026-69918-8
מילות מפתח: עריכת בסיס CRISPR, ויסות גנים, התנגדות CAR-T ל-CD19, וריאנטים לא מקודדים, מיפוי משופע