Clear Sky Science · nl
Nucleotide-resolutiekaart van regulatorische elementen via allelische uitlezing van getilede base editing
Waarom kleine DNA-veranderingen belangrijk kunnen zijn voor kankerbehandeling
Kankerartsen vertrouwen steeds vaker op slimme immuuntherapieën die tumoren opsporen door herkenningsmerkers op hun oppervlak te detecteren. Een van de bekendste merkers op leukemiecellen is CD19, het doelwit van krachtige CAR-T-celtherapieën. Toch herstelt de ziekte bij sommige patiënten omdat kankercellen deze marker stilletjes verliezen of verlagen, waardoor ze aan de behandeling ontsnappen. Deze studie laat zien hoe onderzoekers nu nauwkeurig kunnen inzoomen op DNA-stukken die CD19 reguleren, en precies kunnen aanwijzen welke individuele “letters” in die regulerende regio’s cruciaal zijn om CD19 zichtbaar te houden — en hoe veranderingen in slechts een paar van die letters kankercellen kunnen helpen therapie te ontlopen. 
De schakelaars van onze genen lezen
Genen zijn niet simpelweg aan of uit; ze worden geregeld door nabijgelegen DNA-schakelaars, zogenaamde enhancers, die fijn afstemmen hoeveel van een bepaald eiwit een cel maakt. Veel ziektegerelateerde DNA-veranderingen liggen in deze niet-coderende regelregio’s in plaats van in eiwitcoderende genen zelf. Traditionele genetische studies kunnen verdachte regio’s aanwijzen, maar hebben moeite om precies te bepalen welke DNA-letters daarin kritisch zijn of hoe ze het celdisplay beïnvloeden. Voor therapieën zoals CD19 CAR-T-cellen is die onbekendheid belangrijk: een subtiele wijziging in een regelaar kan CD19 net genoeg verlagen zodat kankercellen zich verbergen, terwijl de rest van de celmechanica intact blijft.
Met moleculaire potloden DNA één letter tegelijk herschrijven
De onderzoekers bouwden een end-to-end experimenteel en computationeel kader om deze cruciale DNA-letters met ongekende precisie in kaart te brengen. Ze richtten zich op een 346-letterlange enhancer net stroomopwaarts van het CD19-gen in leukemiecellen. Met geavanceerde CRISPR-base-editors — moleculaire “potloden” die enkele DNA-letters kunnen veranderen zonder het DNA te knippen — schreven ze deze enhancer systematisch aan met een dichte bibliotheek van gidsmoleculen. Elke gids richtte zich op een iets andere plek, waardoor miljoenen cellen elk voorzien werden van verschillende enkelletterveranderingen en kleine combinaties van wijzigingen binnen hetzelfde korte DNA-segment.
DNA-varianten koppelen aan proteïneniveaus op grote schaal
Om te zien hoe elke bewerkte DNA-versie CD19 beïnvloedde, kleurden het team de cellen met een fluorescerend antilichaam dat sterker oplicht bij hoge CD19-niveaus. Vervolgens gebruikten ze een cel-sorteermachine om de populatie op te splitsen in CD19-hoog en CD19-laag groepen. Cruciaal: in plaats van alleen te tellen welke gidsen aanwezig waren, sequentieerden ze direct de bewerkte enhancerregio zelf in elke groep. Nieuwe analysetools — CRISPR-Millipede en een aangepaste versie van de DESeq2-software — stelden hen in staat elke onderscheidende bewerkte DNA-sequentie als een eigen variant te behandelen en statistisch af te leiden welke exacte enkelletterveranderingen cellen naar lagere of hogere CD19-niveaus duwden. 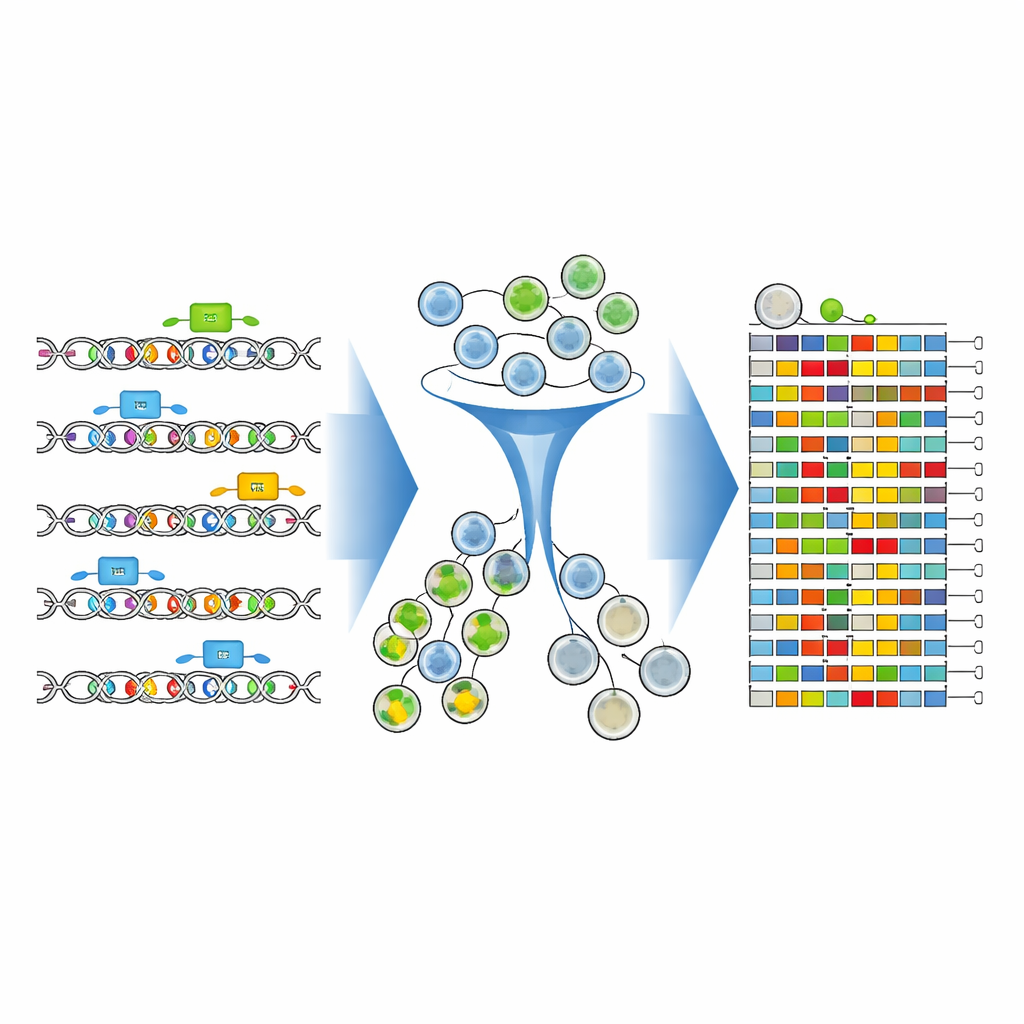
De sleutelplaatsen voor eiwitbinding in de enhancer vinden
Met deze nucleotide-voor-nucleotide kaart in handen legden de onderzoekers hun resultaten naast bekende bindmotieven voor transcriptiefactoren — eiwitten die aan DNA binden om genen te verhogen of verlagen. Ze vonden dat de meest impactvolle letters clusterden binnen sites die worden herkend door factoren zoals MYB, PAX5 en EBF1, belangrijke regelgevers in B-cellen. Door deze specifieke enhancer-mutatues doelbewust te recreëren en door de corresponderende transcriptiefactoren uit te schakelen, bevestigden ze dat het beschadigen van deze bindingssites CD19-niveaus verlaagt. Ze lieten ook zien dat sommige schijnbare treffers uit oudere, op gids-telling gebaseerde methoden vals-positief waren, veroorzaakt door de loutere aanwezigheid van het omvangrijke bewerkerscomplex op het DNA in plaats van door echte sequentieveranderingen, en ze ontwikkelden een afbreekbare editor om deze effecten te scheiden.
Hoe kleine enhancer-wijzigingen CAR-T-therapie kunnen ondermijnen
Ten slotte vroegen de onderzoekers of deze subtiele regulatorische aanpassingen daadwerkelijk invloed hebben op kankerbehandeling. Ze mengden leukemiecellen met en zonder de enhancer-mutaties en zetten ze bloot aan CD19 CAR-T-cellen. Bewerkt materiaal met bepaalde enhancer-veranderingen groeide consequent uit ten koste van de onbewerkte tegenhangers onder CAR-T-aanval, wat aantoonde dat bescheiden verlagingen in CD19 — veroorzaakt niet door het breken van het CD19-gen maar door wijziging van zijn enhancer — genoeg waren om kankercellen te laten overleven. Het werk demonstreert een praktische, schaalbare manier om oorzaak-en-gevolg op enkelletterniveau in genregio’s in kaart te brengen, en toont aan dat niet-coderende varianten stilzwijgend het succes of falen van geavanceerde immunotherapieën kunnen sturen.
Bronvermelding: Becerra, B., Wittibschlager, S., Patel, Z.M. et al. Nucleotide-resolution mapping of regulatory elements via allelic readout of tiled base editing. Nat Commun 17, 3398 (2026). https://doi.org/10.1038/s41467-026-69918-8
Trefwoorden: CRISPR base-editing, genregulatie, CD19 CAR-T-resistentie, niet-coderende varianten, enhancer-mapping