Clear Sky Science · zh
BAX 内的有闸门的疏水漏斗结合生物活性脂质以增强促凋亡功能
脂质如何帮助细胞决定何时死亡
每天,数以百万计的细胞悄然自毁,以维持组织健康并清除受损或危险的细胞。这个内在的自杀程序称为凋亡,依赖于能在线粒体——细胞的能量工厂——膜上打孔的蛋白质。这项研究揭示了某种类似脂质的分子如何将其中一种蛋白 BAX 从沉默的旁观者转变为高效的执行者——并发现了 BAX 内一个隐藏的“漏斗”,未来可能成为新药物的靶点。
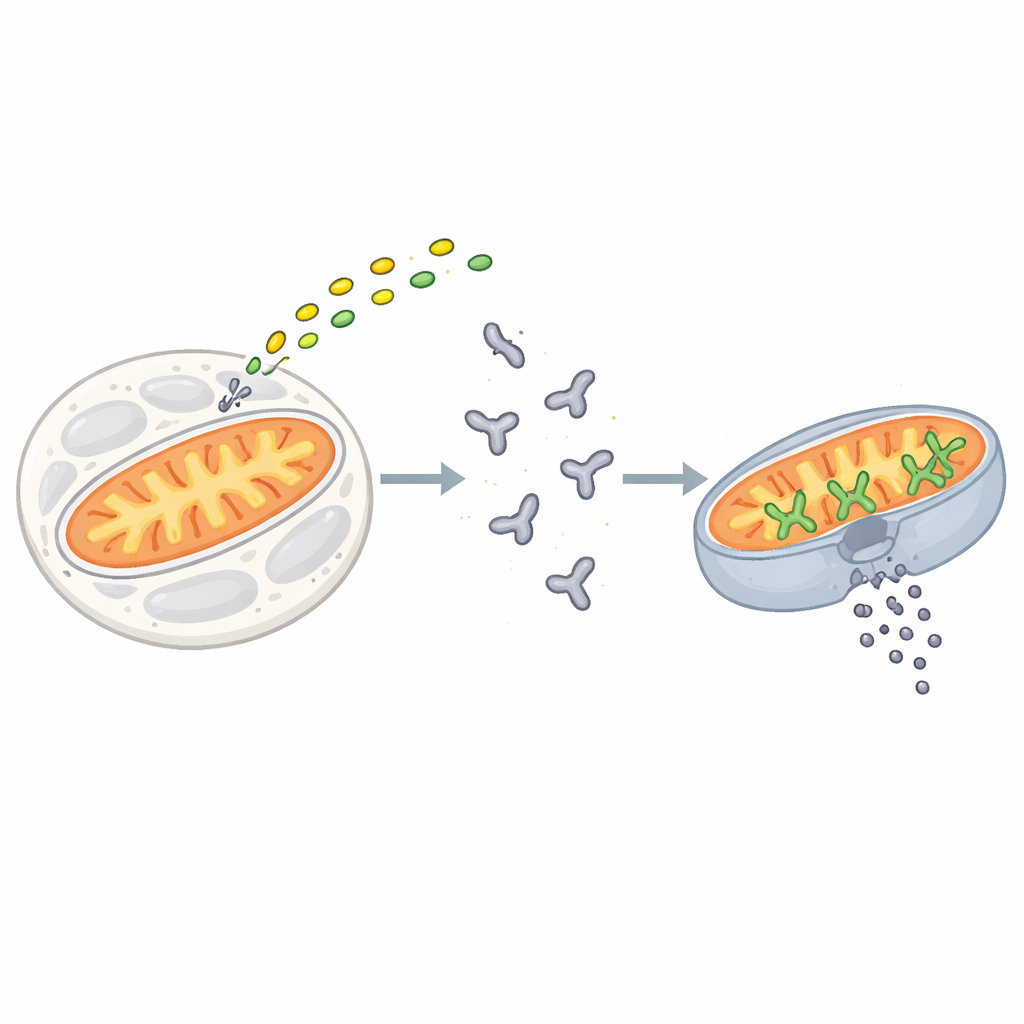
细胞的无归点
当应激或损伤信号汇聚到一类称为 BCL‑2 的蛋白家族时,会触发凋亡。BAX 是该家族中的关键执行者之一。在静息细胞中,BAX 以单个折叠构象悬浮在细胞浆中。当死亡信号到来时,诸如 BIM 之类的短“激活子”蛋白与 BAX 结合并引发一系列构象变化,使 BAX 移向线粒体外膜表面。在那里,BAX 组装成簇,打开膜上的大孔,允许细胞内成分外泄。这个不可逆事件,称为线粒体外膜通透化,是细胞走向死亡的分水岭。
一种活性脂质伙伴登场
早期工作提示,信号分子鞘氨醇‑1‑磷酸的分解产物 2‑反‑十六烯醛(2‑trans‑hexadecenal)对于 BAX 高效形成孔是必需的。但尚不清楚这种疏油分子是单纯改变线粒体膜,还是直接与 BAX 接触。作者首先测试了外加 2‑反‑十六烯醛对活体小鼠细胞的影响。通过实时追踪细胞死亡,他们发现该脂质单独只引起有限的凋亡,但在存在一种使 BAX 抗死亡伴侣失活的药物时,细胞死亡显著上升——且仅在 BAX 及其近亲 BAK 存在时发生。在使用人工膜囊泡的纯化体系中,2‑反‑十六烯醛 本身并不损伤膜,但强烈增强了 BAX(尤其在 BIM 也存在时)打孔的能力。
BAX 内的隐藏漏斗
为弄清该脂质的作用位置与方式,团队采用了一系列结构与生物物理工具。他们证明 2‑反‑十六烯醛以非共价方式与 BAX 结合,移除 BAX 的天然半胱氨酸“把手”并不会削弱这一效应。核磁共振实验证明,结合导致 BAX 内部特定氨基酸发生细微位移,尤以被称为 α5、α6 和 α8 的螺旋周围最为明显。基于这些改变的计算模型揭示了 BAX 核心处先前被忽视的漏斗状空腔,其由灵活的 α8 螺旋封盖。当激活子 BIM 与 BAX 结合时,α8 移动,漏斗张开,停靠模拟预测 2‑反‑十六烯醛 的脂链能紧密嵌入这个疏水通道的深颈部。作者将该口袋命名为“BAX 驱动漏斗”,简称 BAF。
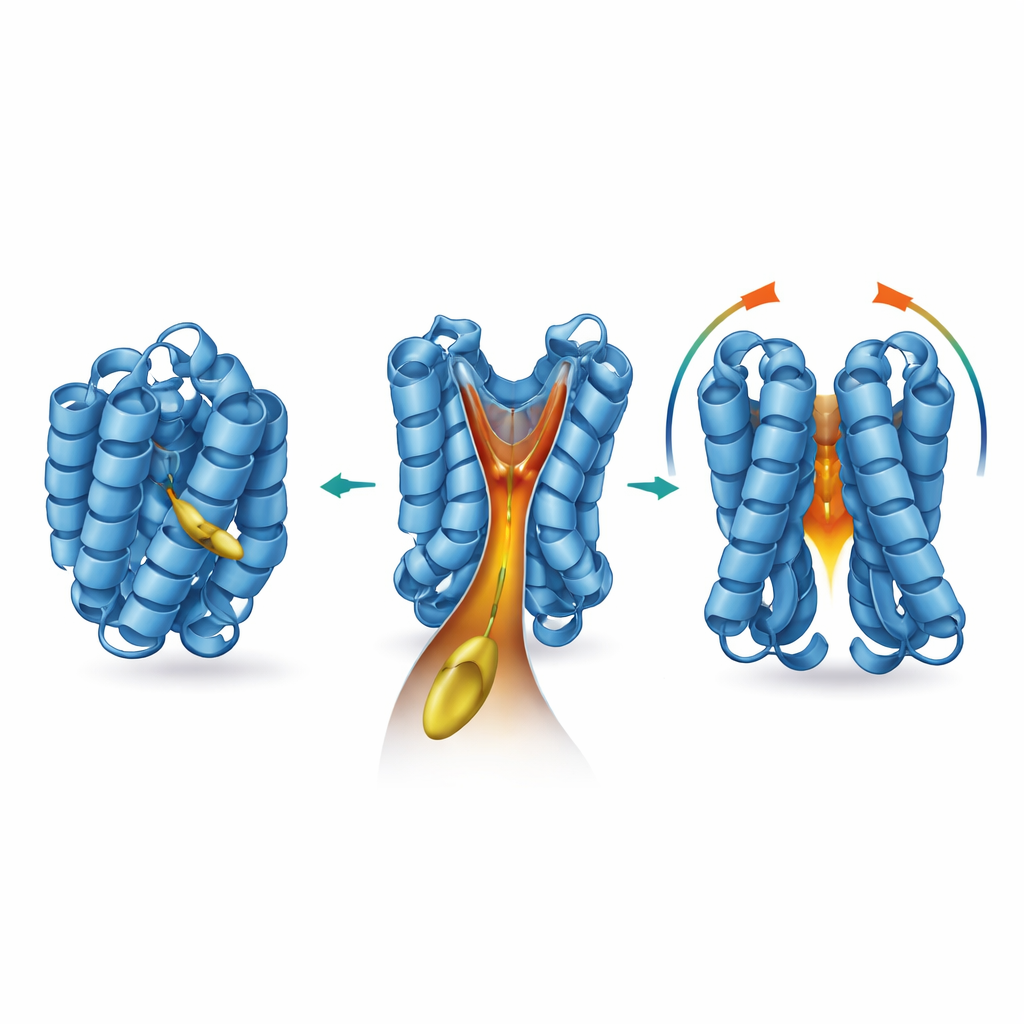
用化学和突变调谐漏斗
研究者接着探问该脂质与 BAX 本身的哪些特征对这种合作至关重要。较短或化学上修饰的脂质仍可与 BAX 接触,但远不如原物触发其激活或打孔活性。相比之下,与 2‑反‑十六烯醛 最相似的长链版本最能开启 BAX,表明链长与亲头基结构必须与漏斗形状相匹配。当团队引入精确突变以略微填充或扭曲漏斗壁时,BAX 仍对 BIM 有反应,但失去了对 2‑反‑十六烯醛 的敏感性。位于两段螺旋之间铰链处的天然关键残基脯氨酸168(P168)以远程方式控制该漏斗。改变这一单个氨基酸重塑了空腔,使 BAX 在静息构象中更稳定,并使纯化蛋白与细胞对该脂质辅因子的响应显著降低。
脂质与蛋白如何联手终结细胞
综合而言,该工作支持了 BAX 激活的阶梯式视角。首先,像 BIM 这样的激活子蛋白与 BAX 结合并启动早期重排,包括放松 α8 “闸门”螺旋。此运动暴露出 BAX 驱动漏斗,2‑反‑十六烯醛 可像楔子般插入其中。占据这个内部通道会破坏 BAX 紧密包装的核心,有利于其相互作用表面的暴露,并促进二聚体及更大簇的形成,从而穿孔线粒体膜。作为一种活性脂质,它不是简单地作为膜溶剂,而是作为真正的分子伙伴,调节 BAX 的致死准备状态。将 BAF 定义为关键控制位点,这项研究为设计能够增强 BAX 活性(在抗癌方面可能有用)或抑制其活性以保护退行性或炎症性疾病中健康组织的小分子奠定了基础。
引用: Gelles, J.D., Chen, Y., Luna-Vargas, M.P.A. et al. A gated hydrophobic funnel within BAX binds bioactive lipids to potentiate pro-apoptotic function. Nat Commun 17, 3180 (2026). https://doi.org/10.1038/s41467-026-69836-9
关键词: BAX, 凋亡, 生物活性脂质, 线粒体, 蛋白-脂质相互作用