Clear Sky Science · pt
Um funil hidrofóbico com portão dentro de BAX se liga a lipídios bioativos para potencializar a função pró‑apoptótica
Como as gorduras ajudam as células a decidir quando morrer
Todos os dias, milhões de nossas células se autodestruíram silenciosamente para manter os tecidos saudáveis e remover células danificadas ou perigosas. Esse programa de suicídio embutido, chamado apoptose, depende de proteínas capazes de abrir buracos nas membranas das mitocôndrias, as usinas de energia da célula. Este estudo revela como uma molécula semelhante a gordura ajuda a converter uma dessas proteínas, BAX, de uma espectadora silenciosa em uma executora eficiente — revelando um “funil” oculto em BAX que, um dia, poderá ser alvo de novos medicamentos.
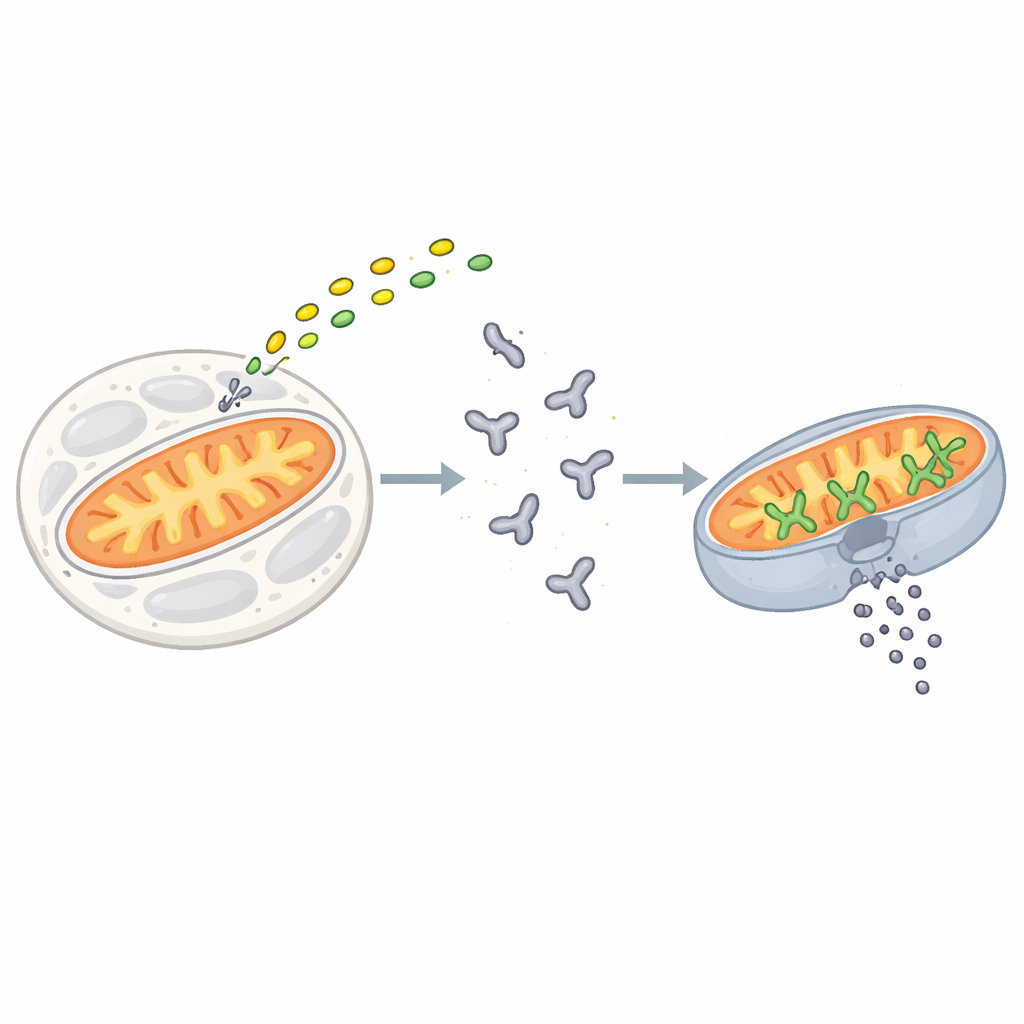
O ponto sem volta de uma célula
A apoptose é desencadeada quando sinais de estresse ou dano convergem numa família de proteínas conhecidas como proteínas BCL‑2. BAX é um dos principais executores dessa família. Em células em repouso, BAX flutua no interior aquoso como uma unidade única e dobrada. Quando chegam sinais de morte, proteínas curtas “ativadoras”, como BIM, ligam‑se a BAX e iniciam uma série de mudanças conformacionais que movem BAX para a superfície externa das mitocôndrias. Lá, BAX se organiza em agregados que abrem grandes poros na membrana, permitindo que o conteúdo interno vaze. Esse evento irreversível, chamado permeabilização da membrana externa mitocondrial, marca o ponto sem volta para a célula.
Entra em cena um lipídio reativo
Trabalhos anteriores sugeriram que um produto de degradação do mensageiro esfingosina‑1‑fosfato, chamado 2‑trans‑hexadecenal, é necessário para que BAX forme poros de modo eficiente. Mas não estava claro se essa molécula oleosa simplesmente alterava a membrana mitocondrial ou se tocava diretamente BAX. Os autores primeiro testaram como a adição de 2‑trans‑hexadecenal afetava células vivas de camundongo. Ao acompanhar a morte celular em tempo real, descobriram que o lipídio por si só causava apoptose limitada, mas na presença de um fármaco que desativa os parceiros anti‑morte de BAX, a morte celular aumentava acentuadamente — e somente quando BAX e seu parente próximo BAK estavam presentes. Em sistemas purificados usando vesículas membranares artificiais, 2‑trans‑hexadecenal não danificou membranas por conta própria, mas impulsionou fortemente a capacidade de BAX, especialmente quando BIM também estava presente, de perfurar membranas.
Um funil oculto dentro de BAX
Para descobrir onde e como esse lipídio age, a equipe recorreu a um conjunto de ferramentas estruturais e biofísicas. Eles mostraram que 2‑trans‑hexadecenal se liga a BAX sem formar ligações químicas permanentes, e que remover as “alças” naturais de cisteína de BAX não reduz o efeito. Experimentos de ressonância magnética nuclear revelaram que a ligação causa deslocamentos sutis em aminoácidos específicos enterrados dentro de BAX, especialmente ao redor das hélices conhecidas como α5, α6 e α8. Modelos computacionais baseados nessas mudanças descobriram uma cavidade em forma de funil até então negligenciada no núcleo de BAX, tampada pela flexível hélice α8. Quando o ativador BIM interage com BAX, α8 se move, o funil se amplia, e simulações de encaixe preveem que a cadeia lipídica do 2‑trans‑hexadecenal se acomoda perfeitamente no estreito pescoço desse túnel hidrofóbico. Os autores nomeiam esse bolso de “funil atuador de BAX”, ou BAF.
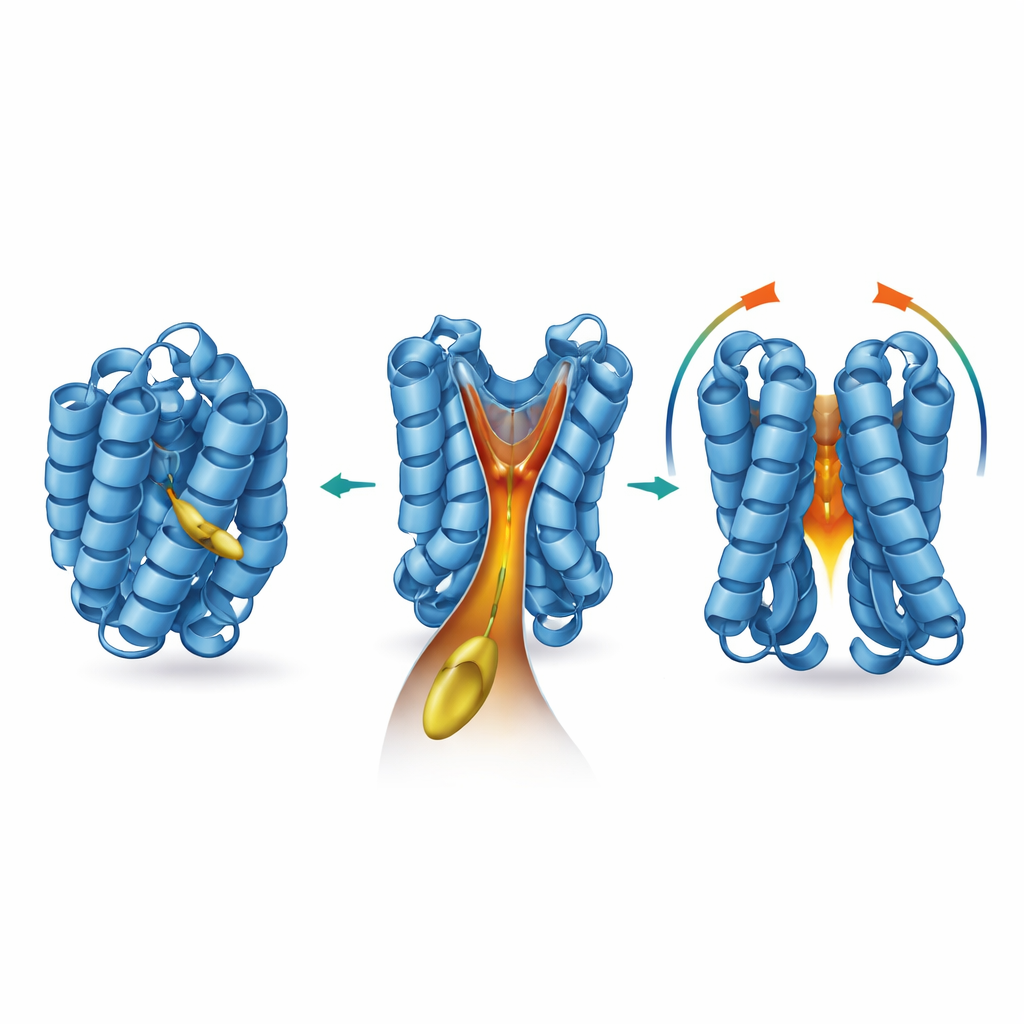
Ajustando o funil com química e mutações
Os pesquisadores então investigaram quais características do lipídio e do próprio BAX são cruciais para essa parceria. Versões mais curtas ou quimicamente alteradas do lipídio ainda podiam se aproximar de BAX, mas tinham muito menos capacidade de disparar sua ativação ou sua atividade formadora de poros. Em contraste, versões de cadeia longa mais semelhantes ao 2‑trans‑hexadecenal foram as melhores em ligar BAX, indicando que o comprimento da cadeia e a estrutura do grupo cabeça devem corresponder à forma do funil. Quando a equipe introduziu mutações precisas que preenchiam ou distorciam ligeiramente as paredes do funil, BAX ainda respondia a BIM, mas perdeu sua sensibilidade ao 2‑trans‑hexadecenal. Um resíduo naturalmente importante, prolina 168, que fica numa dobradiça entre duas hélices, controlou o funil à distância. Mudar esse único aminoácido remodelou a cavidade, estabilizou BAX em sua forma de repouso e tornou tanto proteínas purificadas quanto células muito menos responsivas ao cofator lipídico.
Como lipídios e proteínas se unem para acabar com uma célula
Em conjunto, o trabalho apoia uma visão passo a passo de como BAX é ativado. Primeiro, proteínas ativadoras como BIM se ligam a BAX e iniciam rearranjos precoces, incluindo o afrouxamento da hélice “trava” α8. Esse movimento expõe o funil atuador de BAX, no qual o 2‑trans‑hexadecenal pode se inserir como uma cunha. Ocupando esse túnel interno, o lipídio desestabiliza o núcleo compactamente empacotado de BAX, favorece a exposição de sua superfície de interação e promove a formação de dímeros e agregados maiores que perfuram a membrana mitocondrial. Em vez de atuar como um simples solvente de membrana, esse lipídio bioativo surge como um verdadeiro parceiro molecular que ajusta a prontidão de BAX para matar. Ao definir o BAF como um sítio de controle crítico, o estudo abre a porta para projetar pequenas moléculas que aumentem a atividade de BAX — potencialmente úteis contra o câncer — ou a diminuam para proteger tecidos saudáveis em doenças degenerativas ou inflamatórias.
Citação: Gelles, J.D., Chen, Y., Luna-Vargas, M.P.A. et al. A gated hydrophobic funnel within BAX binds bioactive lipids to potentiate pro-apoptotic function. Nat Commun 17, 3180 (2026). https://doi.org/10.1038/s41467-026-69836-9
Palavras-chave: BAX, apoptose, lipídios bioativos, mitocôndrias, interação proteína‑lipídio