Clear Sky Science · de
Ein abgeschirmter hydrophober Trichter in BAX bindet bioaktive Lipide und verstärkt die pro‑apoptotische Funktion
Wie Fette Zellen bei der Entscheidung zu sterben helfen
Jeden Tag zerstören sich Millionen unserer Zellen stillschweigend selbst, um Gewebe gesund zu halten und beschädigte oder gefährliche Zellen zu beseitigen. Dieses eingebaute Suizidprogramm, Apoptose genannt, hängt von Proteinen ab, die Löcher in die Membranen der Mitochondrien — den Kraftwerken der Zelle — schlagen können. Diese Studie zeigt, wie ein bestimmtes fettähnliches Molekül ein solches Protein, BAX, von einem ruhenden Beobachter in einen effizienten Vollstrecker verwandelt — und legt einen verborgenen „Trichter“ in BAX offen, der eines Tages Ziel neuer Medikamente sein könnte.
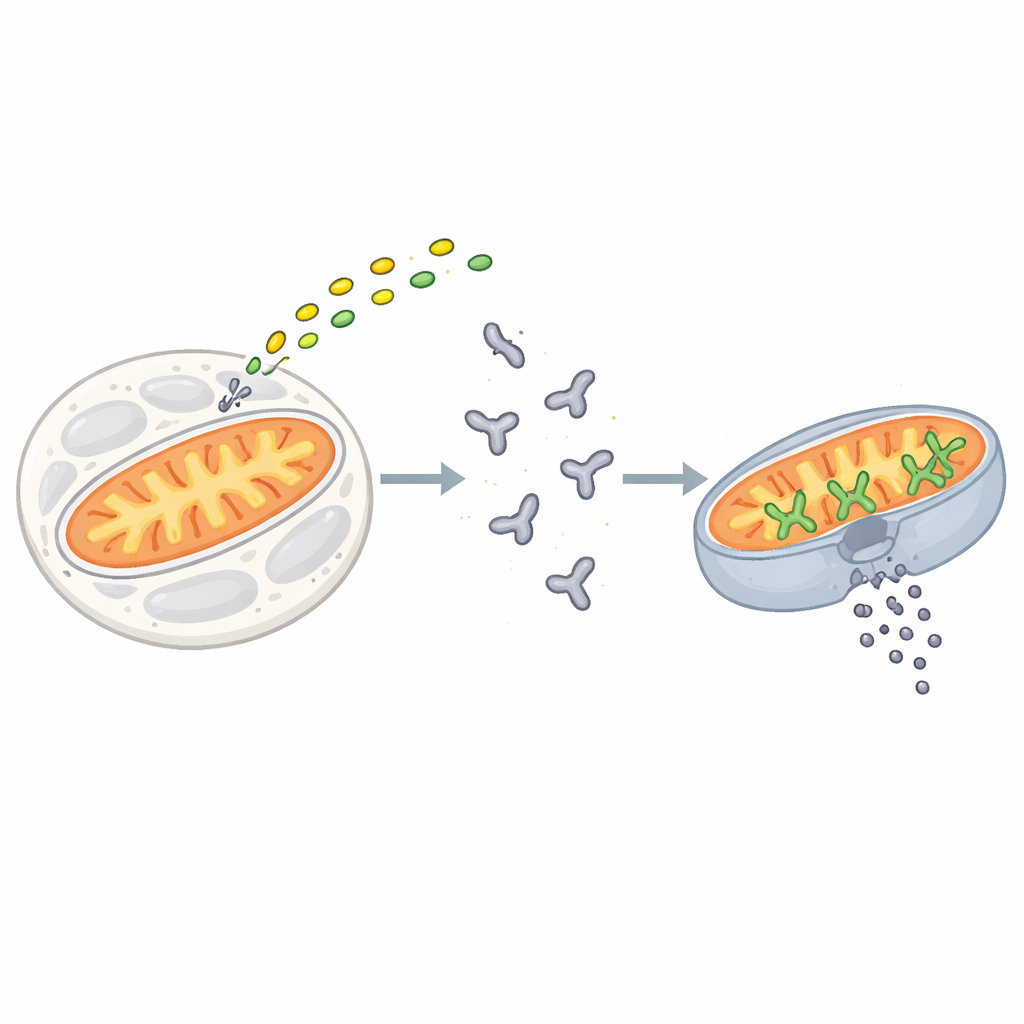
Der Punkt ohne Rückkehr einer Zelle
Apoptose wird ausgelöst, wenn Stress‑ oder Schadenssignale auf eine Familie von Proteinen treffen, die als BCL‑2‑Proteine bekannt sind. BAX ist einer der zentralen Durchsetzer dieser Familie. In ruhenden Zellen treibt BAX als einzelnes, gefaltetes Molekül im wässrigen Inneren umher. Treffen Todessignale ein, heften sich kurze „Aktivator“-Proteine wie BIM an BAX und lösen eine Reihe von Konformationsänderungen aus, die BAX an die Außenseite der Mitochondrien verlagern. Dort bildet BAX Cluster, die große Poren in der Membran öffnen und das Auslaufen des inneren Inhalts erlauben. Dieses irreversible Ereignis, die Permeabilisierung der äußeren Mitochondrienmembran, markiert den Punkt ohne Rückkehr für eine Zelle.
Ein reaktiver Lipidpartner betritt die Bühne
Frühere Arbeiten legten nahe, dass ein Abbauprodukt des Signalmoleküls Sphingosin‑1‑phosphat, genannt 2‑trans‑hexadecenal, für die effiziente Porenbildung durch BAX erforderlich ist. Es war jedoch unklar, ob dieses ölige Molekül einfach die Mitochondrienmembran veränderte oder ob es BAX direkt berührte. Die Autoren testeten zunächst, wie zugefügtes 2‑trans‑hexadecenal lebende Mäusezellen beeinflusst. Durch Echtzeitverfolgung des Zelltods fanden sie heraus, dass das Lipid allein nur begrenzt Apoptose auslöste, aber in Gegenwart eines Wirkstoffs, der BAXs Anti‑Todes‑Partner außer Gefecht setzt, der Zelltod stark anstieg — und zwar nur, wenn BAX und sein enger Verwandter BAK vorhanden waren. In gereinigten Systemen mit künstlichen Membranbläschen beschädigte 2‑trans‑hexadecenal die Membranen nicht selbst, verstärkte jedoch stark die Fähigkeit von BAX, insbesondere in Gegenwart von BIM, Löcher zu schlagen.
Ein verborgener Trichter im Inneren von BAX
Um herauszufinden, wo und wie dieses Lipid wirkt, griff das Team zu einer Reihe struktureller und biophysikalischer Methoden. Sie zeigten, dass 2‑trans‑hexadecenal an BAX bindet, ohne kovalente Bindungen zu bilden, und dass das Entfernen der natürlichen Cystein‑„Griffe“ von BAX die Wirkung nicht abschwächt. Kernspinresonanz‑Experimente zeigten, dass die Bindung subtile Verschiebungen bestimmter, im Inneren von BAX verborgener Aminosäuren verursacht, insbesondere in der Umgebung der Helices α5, α6 und α8. Computermodelle, die auf diesen Veränderungen basieren, enthüllten eine zuvor übersehene, trichterförmige Höhlung im Kern von BAX, die von der flexiblen α8‑Helix verschlossen wird. Wenn der Aktivator BIM an BAX bindet, bewegt sich α8, der Trichter weitet sich, und Andock‑Simulationen sagen voraus, dass die Alkylkette von 2‑trans‑hexadecenal sich passgenau in den tiefen Hals dieses hydrophoben Tunnels einfügt. Die Autoren nennen diese Tasche den „BAX actuating funnel“, kurz BAF.
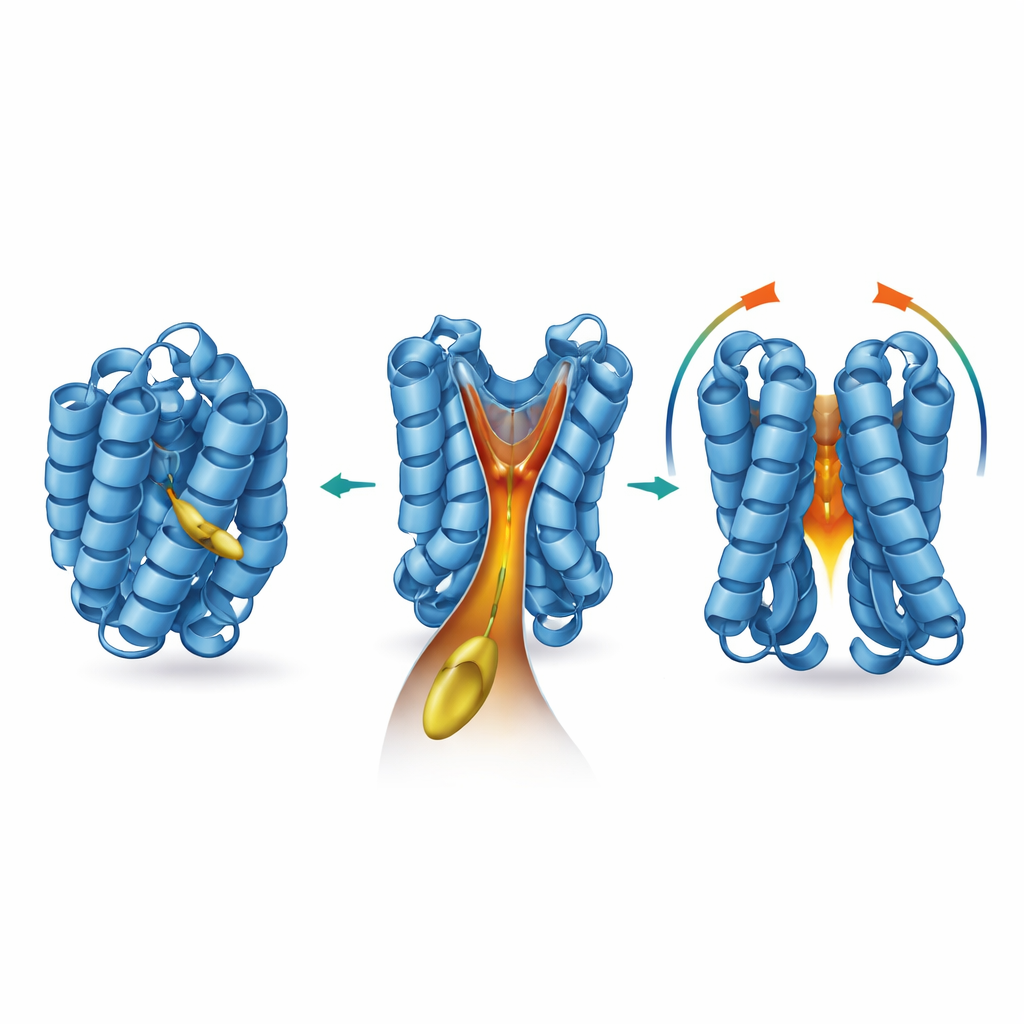
Den Trichter mit Chemie und Mutationen feinabstimmen
Die Forscher fragten dann, welche Merkmale des Lipids und von BAX selbst für diese Partnerschaft entscheidend sind. Kürzere oder chemisch veränderte Versionen des Lipids konnten zwar noch an BAX anstoßen, waren aber weitaus weniger in der Lage, seine Aktivierung oder die Porenbildungsaktivität auszulösen. Im Gegensatz dazu schalteten langkettige Varianten, die 2‑trans‑hexadecenal am ähnlichsten waren, BAX am besten ein, was darauf hindeutet, dass Kettenlänge und Kopfgruppenstruktur zur Form des Trichters passen müssen. Als das Team präzise Mutationen einführte, die die Trichterwände leicht auffüllten oder verzerrten, reagierte BAX weiterhin auf BIM, verlor jedoch seine Empfindlichkeit gegenüber 2‑trans‑hexadecenal. Eine natürlich wichtige Aminosäure, Prolin 168, das in einem Scharnier zwischen zwei Helices sitzt, erwies sich als fernsteuernder Regulator des Trichters. Der Austausch dieser einzigen Aminosäure veränderte die Höhlung, stabilisierte BAX in seiner Ruhform und machte sowohl gereinigte Proteine als auch Zellen deutlich weniger ansprechbar auf den lipidischen Cofaktor.
Wie Lipide und Proteine zusammenarbeiten, um eine Zelle zu beenden
In der Summe stützt die Arbeit eine schrittweise Auffassung davon, wie BAX aktiviert wird. Zuerst binden Aktivatorproteine wie BIM an BAX und lösen frühe Umordnungen aus, darunter das Lockern der α8‑„Tor“‑Helix. Diese Bewegung legt den BAX actuating funnel frei, in den 2‑trans‑hexadecenal wie ein Keil eindringen kann. Die Besetzung dieses internen Tunnels destabilisiert den dicht gepackten Kern von BAX, begünstigt die Freilegung seiner Interaktionsfläche und fördert die Bildung von Dimeren und größeren Clustern, die die mitochondriale Membran perforieren. Anstatt als einfacher Membranlöser zu fungieren, tritt dieses bioaktive Lipid als echter molekularer Partner hervor, der die Bereitschaft von BAX zu töten einstellt. Indem die Studie den BAF als kritische Kontrollstelle definiert, öffnet sie die Tür zur Entwicklung kleiner Moleküle, die entweder die BAX‑Aktivität verstärken — potenziell nützlich gegen Krebs — oder sie dämpfen, um gesundes Gewebe bei degenerativen oder entzündlichen Erkrankungen zu schützen.
Zitation: Gelles, J.D., Chen, Y., Luna-Vargas, M.P.A. et al. A gated hydrophobic funnel within BAX binds bioactive lipids to potentiate pro-apoptotic function. Nat Commun 17, 3180 (2026). https://doi.org/10.1038/s41467-026-69836-9
Schlüsselwörter: BAX, Apoptose, bioaktive Lipide, Mitochondrien, Protein‑Lipid‑Interaktion