Clear Sky Science · nl
Een afgeschermde hydrofobe trechter in BAX bindt bioactieve lipiden om pro-apoptotische functie te versterken
Hoe vetten helpen cellen beslissen wanneer ze moeten sterven
Elke dag voeren miljoenen van onze cellen stilletjes zelfmoord uit om weefsels gezond te houden en beschadigde of gevaarlijke cellen te verwijderen. Dit ingebouwde zelfmoordprogramma, apoptose genoemd, hangt af van eiwitten die gaten in de membranen van mitochondriën, de energiecentrales van de cel, kunnen slaan. Deze studie onthult hoe een bepaald vetachtig molecuul helpt om een van deze eiwitten, BAX, te schakelen van een passieve toeschouwer naar een efficiënte uitvoerder — en onthult een verborgen “trechter” in BAX die ooit door nieuwe geneesmiddelen kan worden gericht.
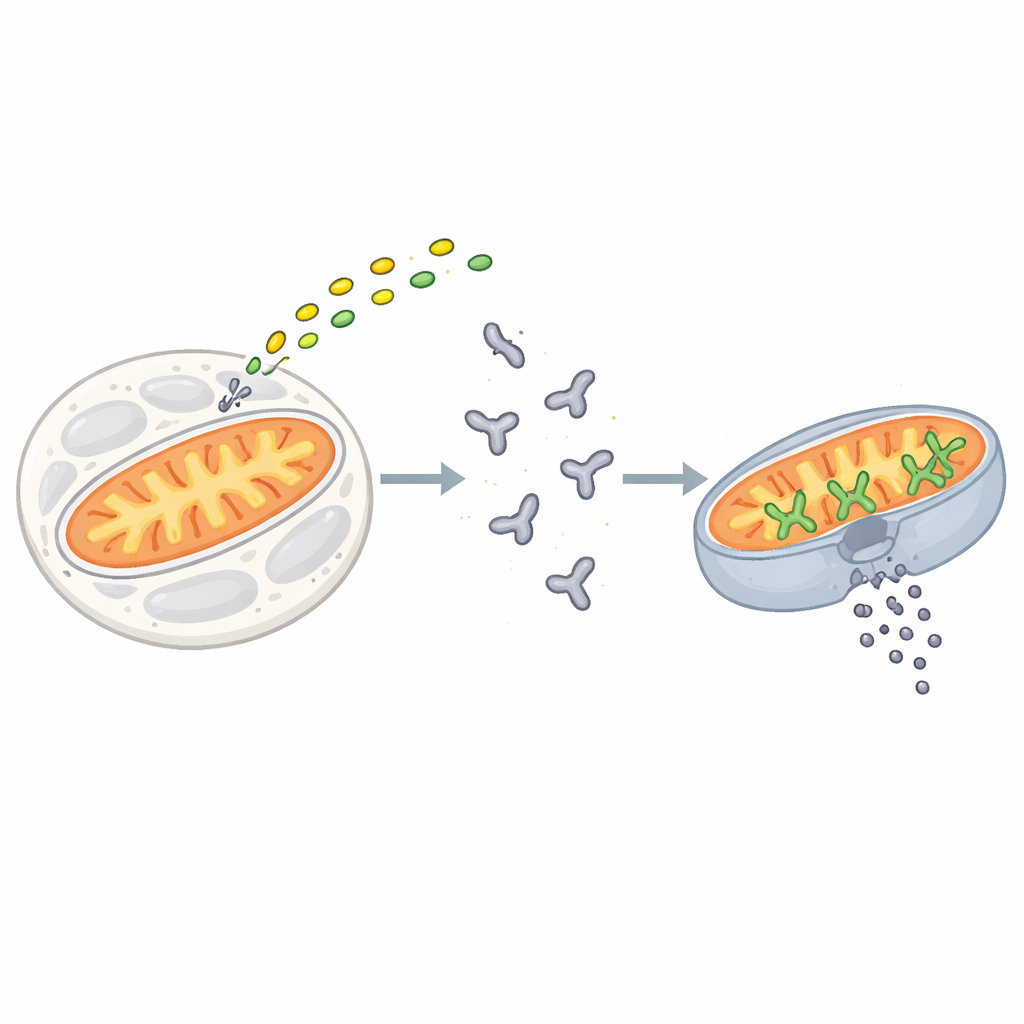
Het punt zonder weg terug voor een cel
Apoptose wordt in gang gezet wanneer stress- of schade‑signalen samenkomen bij een familie van eiwitten die bekendstaan als BCL‑2-eiwitten. BAX is een van de belangrijkste handhavers in deze familie. In rustende cellen drijft BAX als een enkele, gevouwen eenheid in de waterige binnenkant. Wanneer doodssignalen arriveren, hechten korte “activator”-eiwitten zoals BIM zich aan BAX en zetten een reeks vormveranderingen in gang die BAX naar het buitenoppervlak van mitochondriën verplaatsen. Daar assembleert BAX in clusters die grote poriën in het membraan openen, waardoor inhoud naar buiten kan lekken. Deze onomkeerbare gebeurtenis, mitochondriale buitenmembraanpermeabilisatie genoemd, markeert het punt zonder weg terug voor een cel.
Een reactief lipidepartner betreedt het toneel
Vorig werk suggereerde dat een afbraakproduct van het signaalmolecuul sphingosine‑1‑phosphate, genaamd 2‑trans‑hexadeceenal, nodig is voor BAX om efficiënt poriën te vormen. Maar het was onduidelijk of dit olieachtige molecuul eenvoudigweg het mitochondriale membraan veranderde of dat het BAX rechtstreeks raakte. De auteurs onderzochten eerst hoe toegevoegd 2‑trans‑hexadeceenal levende muizencellen beïnvloedde. Door celdood in realtime te volgen, ontdekten ze dat het lipide op zichzelf beperkte apoptose veroorzaakte, maar in aanwezigheid van een middel dat BAX’ anti‑doods‑partners uitschakelt, steeg celdood scherp — en alleen wanneer BAX en zijn nauwe verwant BAK aanwezig waren. In gezuiverde systemen met kunstmatige membraangebubbelingen beschadigde 2‑trans‑hexadeceenal membranen niet op zichzelf, maar versterkte het sterk het vermogen van BAX, vooral wanneer BIM ook aanwezig was, om gaten te slaan.
Een verborgen trechter binnen BAX
Om te achterhalen waar en hoe dit lipide werkt, wendde het team zich tot een reeks structurele en biofysische technieken. Ze toonden aan dat 2‑trans‑hexadeceenal aan BAX bindt zonder permanente chemische bindingen te vormen, en dat het weghalen van BAX’ natuurlijke cysteïne-“grepen” het effect niet dempt. Nucleaire magnetische resonantie-experimenten onthulden dat binding subtiele verschuivingen veroorzaakt in specifieke aminozuren die diep in BAX verborgen liggen, vooral rond helices die bekendstaan als α5, α6 en α8. Computermodellen gebaseerd op deze veranderingen onthulden een eerder over het hoofd geziene, trechtervormige holte in de kern van BAX, afgedekt door de flexibele α8-helix. Wanneer activator BIM zich aan BAX bindt, verplaatst α8 zich, verwijdt de trechter en voorspellen dockingsimulaties dat de lipideketen van 2‑trans‑hexadeceenal precies in de diepe hals van deze hydrofobe tunnel past. De auteurs noemen dit pocket de “BAX actuating funnel”, of BAF.
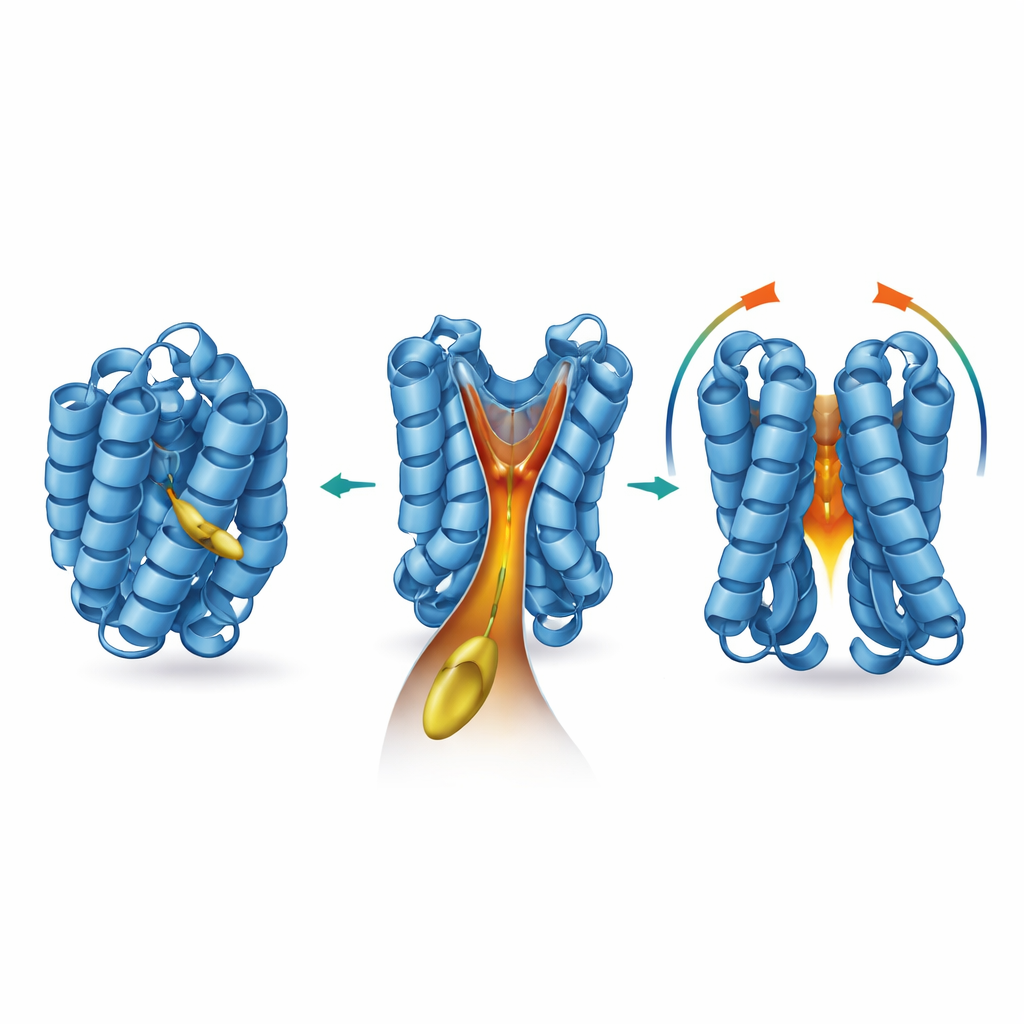
Het afstemmen van de trechter met chemie en mutaties
De onderzoekers vroegen vervolgens welke kenmerken van het lipide en van BAX zelf cruciaal zijn voor dit partnerschap. Kortere of chemisch gewijzigde versies van het lipide konden nog wel BAX aanraken maar waren veel minder in staat om zijn activatie of pore‑vormende activiteit te triggeren. Daarentegen waren langeketenvormen die het meest leken op 2‑trans‑hexadeceenal het beste in het inschakelen van BAX, wat aangeeft dat ketenlengte en de structuur van de kopgroep moeten passen bij de vorm van de trechter. Toen het team precieze mutaties introduceerde die de trechterwanden licht opvulden of vervormden, reageerde BAX nog wel op BIM maar verloor het zijn gevoeligheid voor 2‑trans‑hexadeceenal. Een van nature belangrijke residu, proline 168, dat in een scharnier tussen twee helices ligt, bleek de trechter op afstand te regelen. Het wijzigen van dit enkele aminozuur herschikte de holte, stabiliseerde BAX in zijn rustvorm en maakte zowel gezuiverde eiwitten als cellen veel minder responsief voor de lipide co‑factor.
Hoe lipiden en eiwitten samenwerken om een cel te beëindigen
Gezamenlijk ondersteunen de bevindingen een stapsgewijs beeld van hoe BAX wordt geactiveerd. Eerst binden activator‑eiwitten zoals BIM aan BAX en starten vroege herschikkingen, waaronder het losser worden van de α8-“sluiter”-helix. Deze beweging maakt de BAX actuating funnel zichtbaar, waarin 2‑trans‑hexadeceenal als een wig kan schuiven. Bezetting van deze interne tunnel destabiliseert BAX’ strak verpakte kern, bevordert de blootstelling van zijn interactieoppervlak en stimuleert de vorming van dimeren en grotere clusters die het mitochondriale membraan perforeren. In plaats van te werken als een eenvoudige membraansolvent, blijkt dit bioactieve lipide een echte moleculaire partner die BAX’ gereedheid om te doden afstemt. Door de BAF als een kritisch controlesite te definiëren, opent de studie de deur naar het ontwerpen van kleine moleculen die ofwel BAX‑activiteit versterken — mogelijk nuttig tegen kanker — of deze dempen om gezonde weefsels te beschermen bij degeneratieve of inflammatoire aandoeningen.
Bronvermelding: Gelles, J.D., Chen, Y., Luna-Vargas, M.P.A. et al. A gated hydrophobic funnel within BAX binds bioactive lipids to potentiate pro-apoptotic function. Nat Commun 17, 3180 (2026). https://doi.org/10.1038/s41467-026-69836-9
Trefwoorden: BAX, apoptose, bioactieve lipiden, mitochondriën, eiwit-lipide interactie