Clear Sky Science · pl
Hydrofobowy lejek z zamkiem w BAX wiąże bioaktywne lipidy, wzmagając funkcję proapoptotyczną
Jak tłuszcze pomagają komórkom zdecydować, kiedy umrzeć
Każdego dnia miliony naszych komórek cicho się autodestrukują, by utrzymać tkanki w zdrowiu i usunąć komórki uszkodzone lub potencjalnie niebezpieczne. Ten wbudowany program samobójczy, nazywany apoptozą, zależy od białek zdolnych do wykonywania otworów w błonach mitochondriów — elektrowni komórki. Badanie to odkrywa, w jaki sposób określona cząsteczka przypominająca tłuszcz pomaga przestawić jedno z tych białek, BAX, z cichego obserwatora w wydajnego egzekutora — ujawniając ukryty „lejek” w BAX, który być może w przyszłości będzie można celurować nowymi lekami.
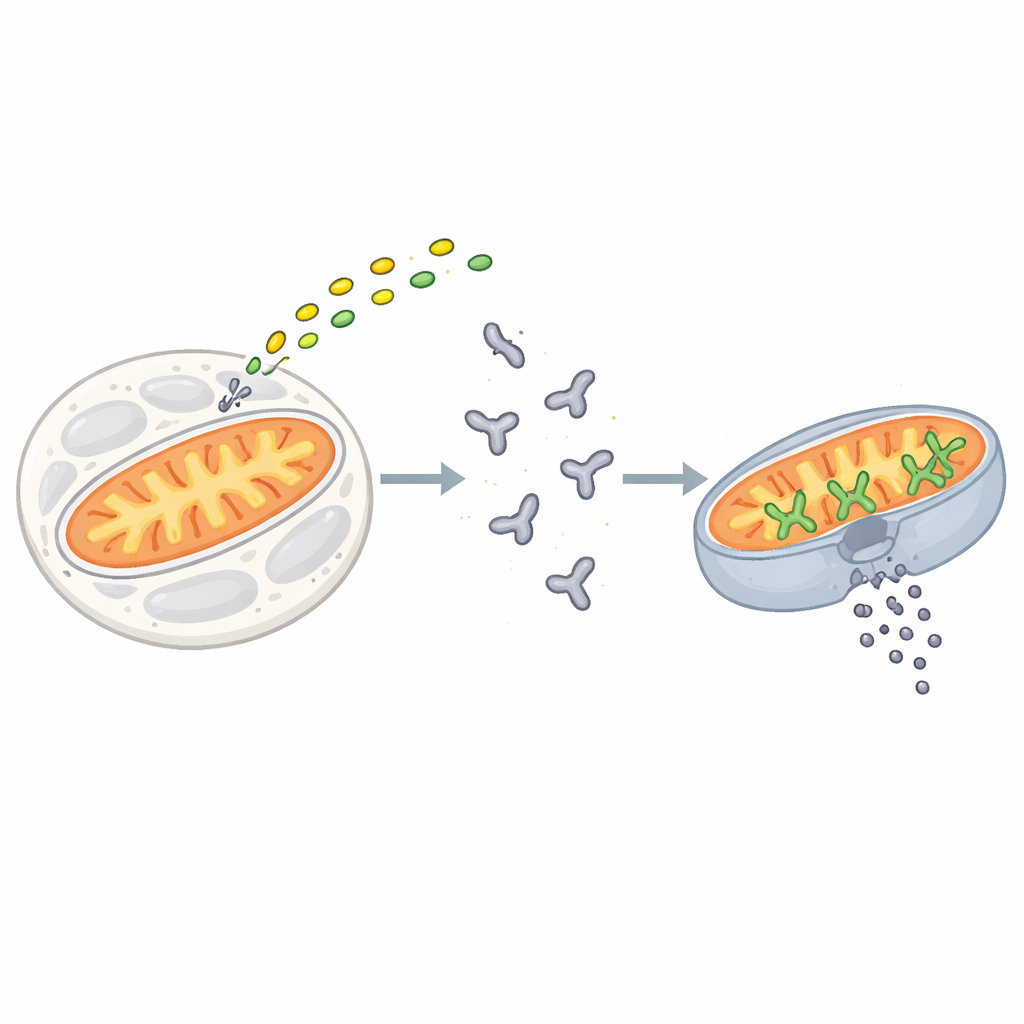
Punkt bez powrotu dla komórki
Apoptoza jest wywoływana, gdy sygnały stresu lub uszkodzeń zbiegają się na rodzinie białek znanych jako białka BCL‑2. BAX jest jednym z kluczowych egzekutorów w tej rodzinie. W komórkach spoczynkowych BAX krąży w wodnym wnętrzu jako pojedyncza, złożona cząsteczka. Gdy nadchodzą sygnały śmierci, krótkie „aktywatory” takie jak BIM przyczepiają się do BAX i inicjują serię zmian kształtu, które przemieszczają BAX na zewnętrzną powierzchnię mitochondriów. Tam BAX organizuje się w skupiska, które otwierają duże pory w błonie, pozwalając na wydostanie się zawartości wewnętrznej. To nieodwracalne zdarzenie, zwane przepuszczalnością zewnętrznej błony mitochondrialnej, stanowi punkt bez powrotu dla komórki.
W scenerię wchodzi reaktywny lipid
Wcześniejsze prace sugerowały, że produkt rozpadu cząsteczki sygnalizacyjnej sfingozyno‑1‑fosforanu, zwany 2‑trans‑heksadecenalem, jest potrzebny, by BAX efektywnie tworzył pory. Nie było jednak jasne, czy ta oleista cząsteczka po prostu zmieniała właściwości błony mitochondrialnej, czy też oddziaływała bezpośrednio z BAX. Autorzy najpierw przetestowali, jak dodany 2‑trans‑heksadecenal wpływa na żywe komórki myszy. Śledząc śmierć komórek w czasie rzeczywistym, stwierdzili, że sam lipid wywoływał ograniczoną apoptozę, lecz w obecności leku wyłączającego przeciwśmiercionośnych partnerów BAX śmierć komórek gwałtownie wzrosła — i tylko jeśli obecne były BAX oraz jego bliski krewny BAK. W oczyszczonych układach używających sztucznych pęcherzyków błonowych 2‑trans‑heksadecenal nie uszkadzał sam błon, ale silnie wzmacniał zdolność BAX, zwłaszcza w obecności BIM, do wykonywania otworów.
Ukryty lejek wewnątrz BAX
Aby ustalić, gdzie i jak działa ten lipid, zespół sięgnął po zestaw narzędzi strukturalnych i biofizycznych. Pokazali, że 2‑trans‑heksadecenal wiąże się z BAX bez tworzenia trwałych wiązań chemicznych, a usunięcie naturalnych cystein „uchwytów” BAX nie osłabia tego efektu. Doświadczenia z rezonansu magnetycznego jądrowego ujawniły, że wiązanie powoduje subtelne przesunięcia w specyficznych aminokwasach zanurzonych wewnątrz BAX, szczególnie wokół helis znanych jako α5, α6 i α8. Modele komputerowe oparte na tych zmianach odkryły wcześniej pomijaną, lejkopodobną jamę w rdzeniu BAX, zamykaną przez elastyczną helisę α8. Gdy aktywator BIM wiąże się z BAX, α8 przesuwa się, lejek się rozszerza, a symulacje dokowania przewidują, że łańcuch lipidowy 2‑trans‑heksadecenalu wpasowuje się ciasno w głęboki szyjkę tego hydrofobowego tunelu. Autorzy nazywają tę kieszeń „BAX actuating funnel”, czyli BAF.
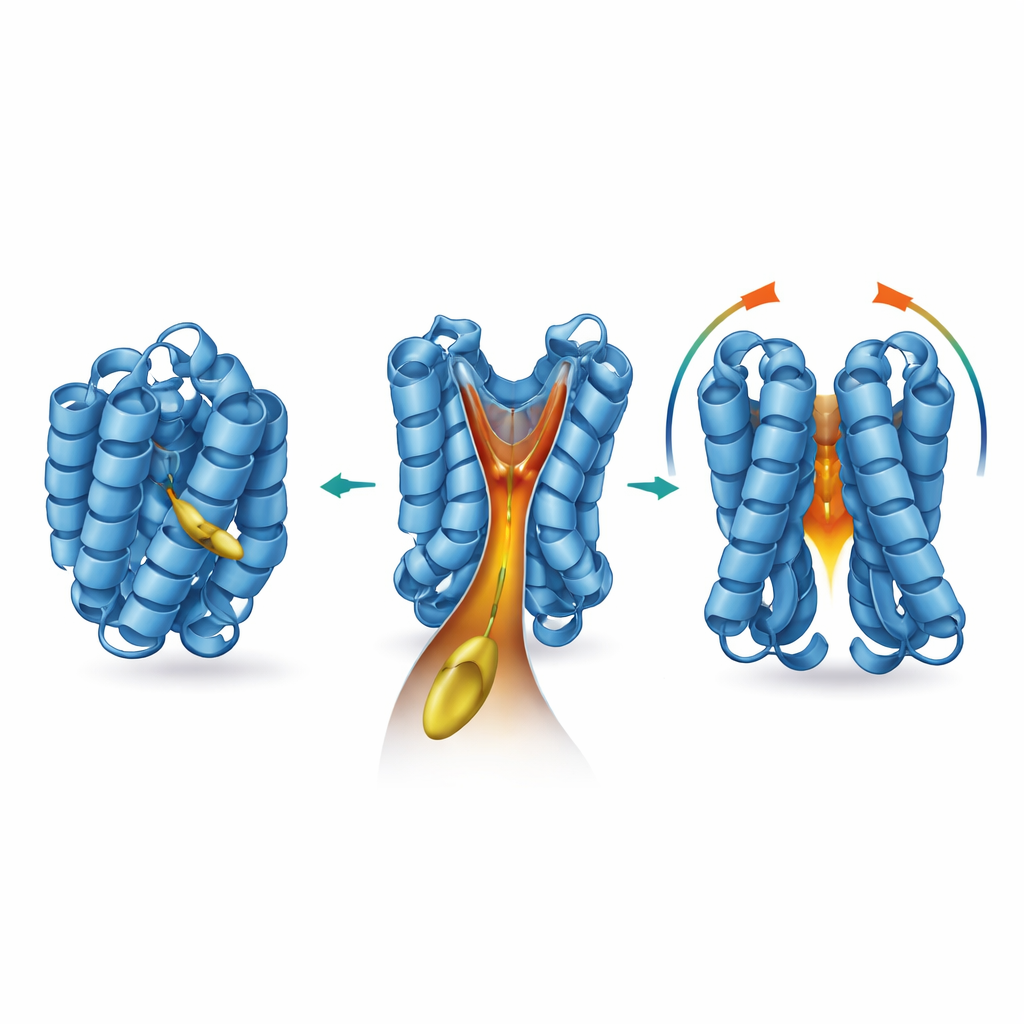
Dostrajanie lejka za pomocą chemii i mutacji
Następnie badacze zapytali, które cechy lipidu i samego BAX są kluczowe dla tego partnerstwa. Krótsze lub chemicznie zmodyfikowane wersje lipidu nadal mogły stykać się z BAX, ale znacznie słabiej wywoływały jego aktywację lub aktywność tworzenia porów. Natomiast długie łańcuchy najbardziej podobne do 2‑trans‑heksadecenalu najlepiej przełączały BAX, co wskazuje, że długość łańcucha i struktura grupy głównej muszą odpowiadać kształtowi lejka. Gdy zespół wprowadził precyzyjne mutacje, które nieco wypełniały lub odkształcały ściany lejka, BAX nadal reagował na BIM, ale utracił wrażliwość na 2‑trans‑heksadecenal. Naturalnie istotne resztę, prolina 168, która znajduje się na zawiasie między dwiema helisami, okazała się zdalnie kontrolować lejek. Zmiana tego pojedynczego aminokwasu przeformowała wnękę, ustabilizowała BAX w formie spoczynkowej i uczyniła zarówno oczyszczone białka, jak i komórki znacznie mniej wrażliwymi na lipidowy kofaktor.
Jak lipidy i białka współdziałają, by zakończyć życie komórki
W całości praca wspiera etapowy obraz aktywacji BAX. Najpierw aktywatory takie jak BIM wiążą BAX i inicjują wczesne przearanżowania, w tym poluzowanie „furtki” helisy α8. Ten ruch odsłania BAX actuating funnel, do którego 2‑trans‑heksadecenal może wsunąć się niczym klin. Zajęcie tego wewnętrznego tunelu destabilizuje ciasno upakowane jądro BAX, sprzyja odsłonięciu powierzchni interakcji i promuje tworzenie dimerów oraz większych skupisk, które perforują błonę mitochondrialną. Zamiast działać jako prosty rozpuszczalnik błonowy, ten bioaktywny lipid wyłania się jako prawdziwy partner molekularny, który stroi gotowość BAX do zabijania. Zdefiniowanie BAF jako krytycznego miejsca kontroli otwiera drogę do projektowania małych cząsteczek, które albo wzmocnią aktywność BAX — potencjalnie użyteczne przeciwko rakowi — albo ją stłumią, by chronić zdrowe tkanki w chorobach zwyrodnieniowych lub zapalnych.
Cytowanie: Gelles, J.D., Chen, Y., Luna-Vargas, M.P.A. et al. A gated hydrophobic funnel within BAX binds bioactive lipids to potentiate pro-apoptotic function. Nat Commun 17, 3180 (2026). https://doi.org/10.1038/s41467-026-69836-9
Słowa kluczowe: BAX, apoptoza, bioaktywne lipidy, mitochondria, interakcja białko-lipid