Clear Sky Science · es
Un embudo hidrofóbico con compuerta dentro de BAX se une a lípidos bioactivos para potenciar la función proapoptótica
Cómo las grasas ayudan a las células a decidir cuándo morir
Cada día, millones de nuestras células se autodestruyen en silencio para mantener los tejidos sanos y eliminar células dañadas o peligrosas. Este programa de suicidio incorporado, llamado apoptosis, depende de proteínas capaces de perforar las membranas de las mitocondrias, las centrales energéticas de la célula. Este estudio desvela cómo una molécula similar a una grasa ayuda a convertir a una de estas proteínas, BAX, de un observador silencioso en un ejecutor eficaz, revelando un “embudo” oculto en BAX que algún día podría ser blanco de nuevos fármacos.
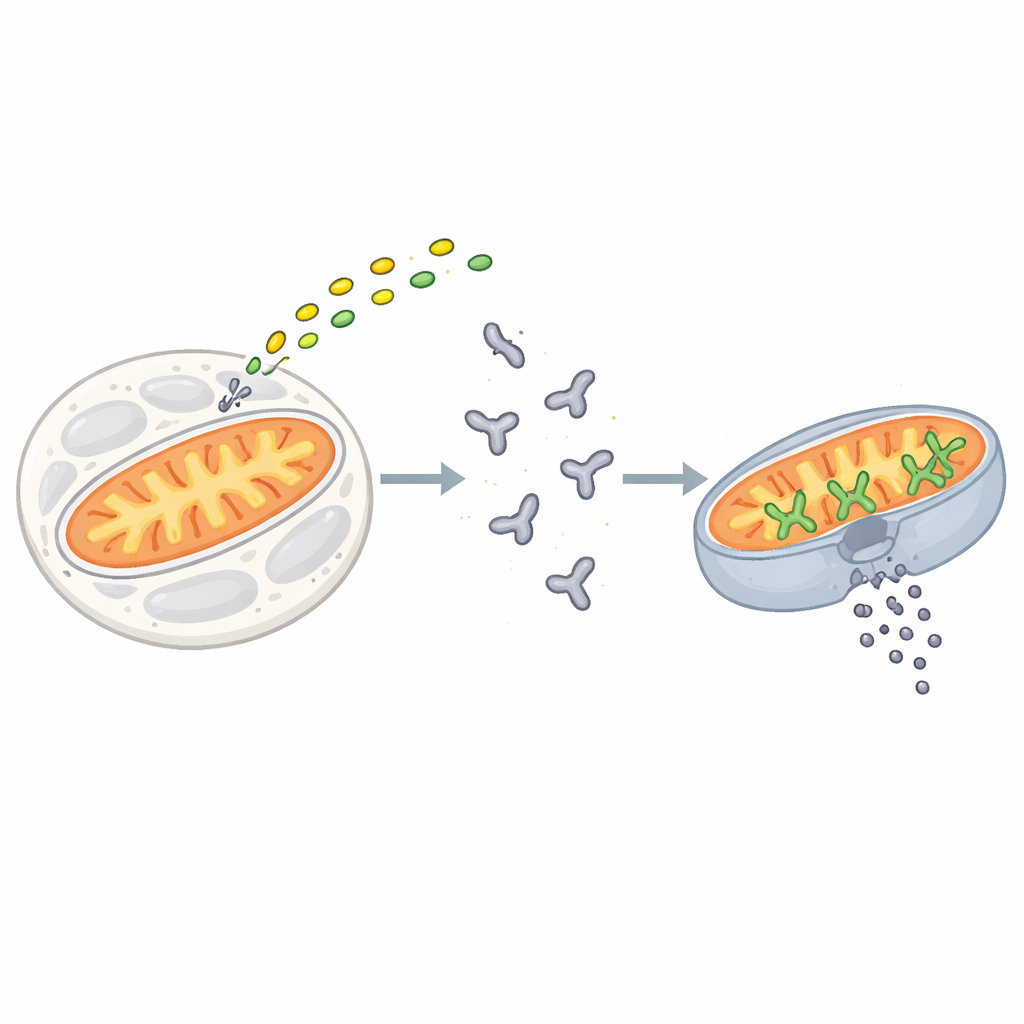
El punto sin retorno de una célula
La apoptosis se desencadena cuando señales de estrés o daño convergen en una familia de proteínas conocidas como las BCL‑2. BAX es uno de los principales agentes ejecutores de esta familia. En las células en reposo, BAX flota en el interior acuoso como una unidad plegada y solitaria. Cuando llegan señales de muerte, proteínas activadoras cortas como BIM se adhieren a BAX e inician una serie de cambios conformacionales que trasladan a BAX a la superficie externa de las mitocondrias. Allí, BAX se ensambla en cúmulos que abren poros grandes en la membrana, permitiendo que el contenido interno se derrame. Este evento irreversible, llamado permeabilización de la membrana externa mitocondrial, marca el punto sin retorno para la célula.
Entra en escena un lípido reactivo
Trabajos anteriores sugerían que un producto de descomposición del mensajero esfingosina‑1‑fosfato, llamado 2‑trans‑hexadecenal, es necesario para que BAX forme poros de manera eficiente. Pero no estaba claro si esta molécula oleosa alteraba simplemente la membrana mitocondrial o si tocaba directamente a BAX. Los autores probaron primero cómo afectaba el 2‑trans‑hexadecenal a células de ratón vivas. Mediante el seguimiento en tiempo real de la muerte celular, encontraron que el lípido por sí solo provocaba una apoptosis limitada, pero en presencia de un fármaco que desactiva los socios anti‑muerte de BAX, la muerte celular aumentó bruscamente —y solo cuando BAX y su pariente cercano BAK estaban presentes. En sistemas purificados usando burbujas de membrana artificiales, el 2‑trans‑hexadecenal no dañó las membranas por sí mismo, pero potenció fuertemente la capacidad de BAX, especialmente cuando BIM también estaba presente, para perforarlas.
Un embudo oculto dentro de BAX
Para averiguar dónde y cómo actúa este lípido, el equipo recurrió a una batería de herramientas estructurales y biofísicas. Mostraron que el 2‑trans‑hexadecenal se une a BAX sin formar enlaces químicos permanentes, y que eliminar las “manijas” naturales de cisteína de BAX no reduce el efecto. Experimentos de resonancia magnética nuclear revelaron que la unión provoca desplazamientos sutiles en aminoácidos específicos enterrados dentro de BAX, especialmente alrededor de las hélices conocidas como α5, α6 y α8. Modelos computacionales basados en estos cambios descubrieron una cavidad en forma de embudo en el núcleo de BAX, hasta entonces pasada por alto, rematada por la flexible hélice α8. Cuando el activador BIM se une a BAX, α8 se mueve, el embudo se ensancha y simulaciones de acoplamiento predicen que la cadena lipídica del 2‑trans‑hexadecenal encaja ajustadamente en el cuello profundo de este túnel hidrofóbico. Los autores denominan a este bolsillo el “embudo activador de BAX”, o BAF.
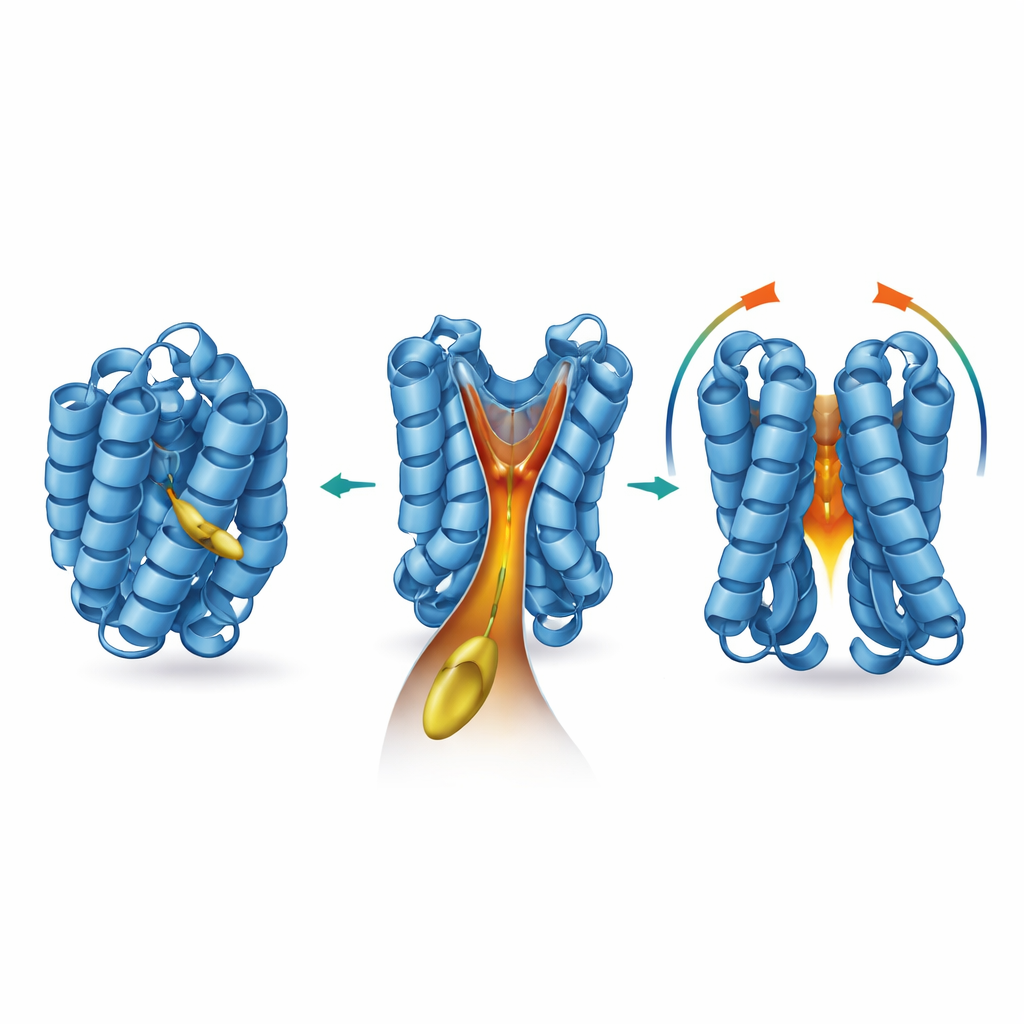
Ajustando el embudo con química y mutaciones
Los investigadores preguntaron luego qué características del lípido y del propio BAX son cruciales para esta asociación. Versiones más cortas o químicamente alteradas del lípido podían aún rozar BAX pero eran mucho menos capaces de desencadenar su activación o su actividad formadora de poros. En contraste, las versiones de cadena larga más similares al 2‑trans‑hexadecenal fueron las más eficaces para activar BAX, lo que indica que la longitud de la cadena y la estructura del grupo polar deben coincidir con la forma del embudo. Cuando el equipo introdujo mutaciones precisas que rellenaban ligeramente o distorsionaban las paredes del embudo, BAX siguió respondiendo a BIM pero perdió su sensibilidad al 2‑trans‑hexadecenal. Un residuo de importancia natural, la prolina 168, que se sitúa en una bisagra entre dos hélices, resultó controlar el embudo a distancia. Cambiar este único aminoácido remodeló la cavidad, estabilizó a BAX en su forma de reposo y hizo que tanto las proteínas purificadas como las células fueran mucho menos sensibles al cofactor lipídico.
Cómo lípidos y proteínas se coordinan para acabar con una célula
En conjunto, el trabajo avala una visión escalonada de cómo se activa BAX. Primero, proteínas activadoras como BIM se unen a BAX e inician las primeras reordenaciones, incluida la relajación de la hélice “puerta” α8. Este movimiento expone el embudo activador de BAX, en el que el 2‑trans‑hexadecenal puede insertarse como una cuña. Ocupar este túnel interno desestabiliza el núcleo compactado de BAX, favorece la exposición de su superficie de interacción y promueve la formación de dímeros y cúmulos mayores que perforan la membrana mitocondrial. En lugar de actuar como un simple disolvente de membranas, este lípido bioactivo emerge como un verdadero socio molecular que ajusta la predisposición de BAX para matar. Al definir el BAF como un sitio de control crítico, el estudio abre la puerta al diseño de pequeñas moléculas que potencien la actividad de BAX —potencialmente útiles contra el cáncer— o que la atenúen para proteger tejidos sanos en enfermedades degenerativas o inflamatorias.
Cita: Gelles, J.D., Chen, Y., Luna-Vargas, M.P.A. et al. A gated hydrophobic funnel within BAX binds bioactive lipids to potentiate pro-apoptotic function. Nat Commun 17, 3180 (2026). https://doi.org/10.1038/s41467-026-69836-9
Palabras clave: BAX, apoptosis, lípidos bioactivos, mitocondrias, interacción proteína-lípido