Clear Sky Science · sv
En grindad hydrofob tratt i BAX binder bioaktiva lipider för att förstärka pro-apoptotisk funktion
Hur fetter hjälper celler att avgöra när de ska dö
Varje dag genomgår miljontals av våra celler tyst självdestruktion för att hålla vävnader friska och avlägsna skadade eller farliga celler. Detta inbyggda självmordsprogram, kallat apoptos, beror på proteiner som kan göra hål i mitokondriernas membran, cellens kraftverk. Den här studien avslöjar hur en viss fettlik molekyl hjälper till att växla ett av dessa proteiner, BAX, från en tyst åskådare till en effektiv bödel — och blottar en dold “tratt” i BAX som en dag skulle kunna riktas av nya läkemedel.
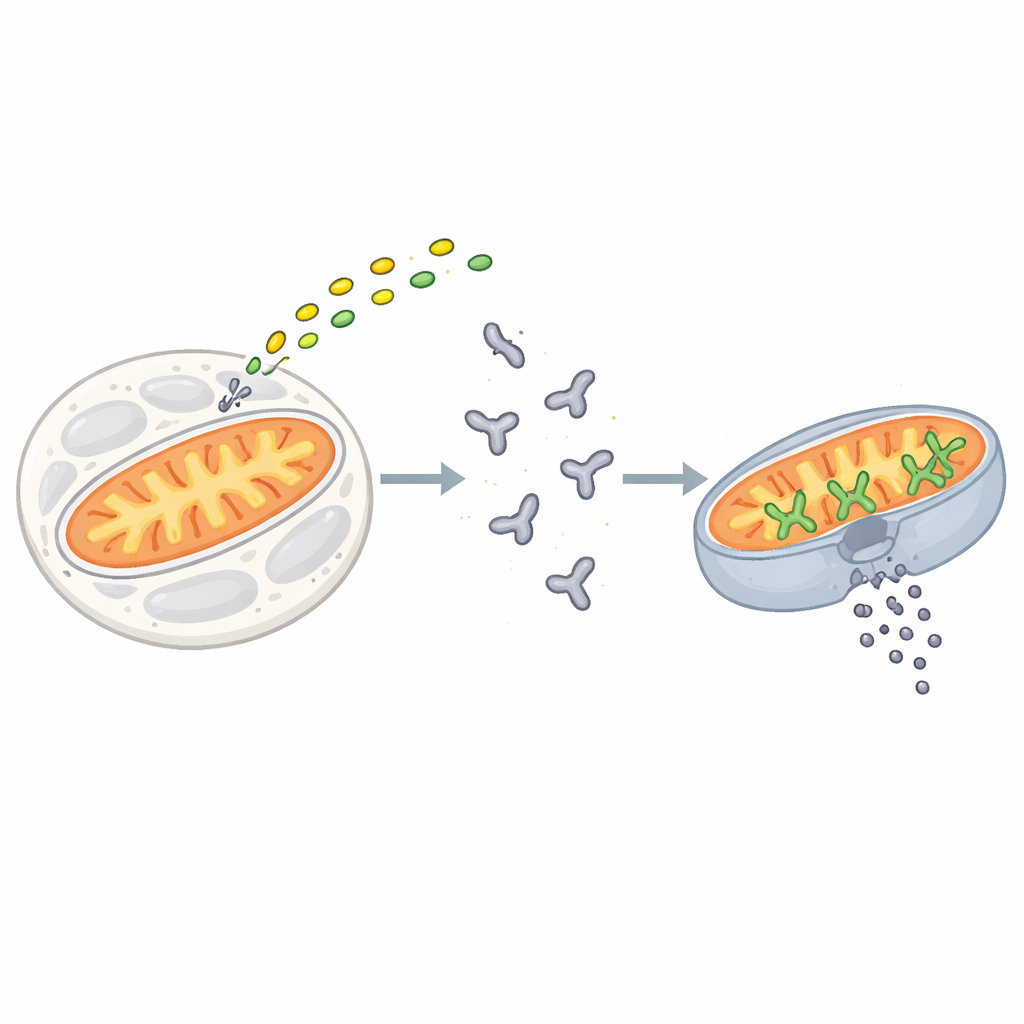
Cellens punkt utan återvändo
Apoptos utlöses när stress- eller skade-signaler konvergerar på en familj proteiner kända som BCL-2-proteiner. BAX är en av huvudutförarna i denna familj. I vilande celler driver BAX omkring i det vattenrika inre som en enda, veckad enhet. När dödssignaler anländer hakar korta “aktivator”-proteiner som BIM fast vid BAX och startar en serie formförändringar som flyttar BAX till mitokondriens yttre yta. Där samlas BAX i kluster som öppnar stora porer i membranet och tillåter cellens innehåll att läcka ut. Denna irreversibla händelse, kallad permeabilisering av mitokondriens yttre membran, markerar cellens punkt utan återvändo.
En reaktiv lipidpartner träder in
Tidigare arbete antydde att en nedbrytningsprodukt av signalsubstansen sfingosin-1-fosfat, kallad 2-trans-hexadecenal, krävs för att BAX effektivt ska bilda porer. Men det var oklart om denna oljiga molekyl helt enkelt ändrade mitokondriemembranet eller om den berörde BAX direkt. Författarna testade först hur tillsatt 2-trans-hexadecenal påverkade levande musceller. Genom att följa celldöd i realtid fann de att lipiden i sig gav begränsad apoptos, men i närvaro av ett läkemedel som inaktiverar BAXs anti-döds-partners ökade celldöden kraftigt — och endast när BAX och dess nära släkting BAK var närvarande. I renade system med artificiella membranbubblor skadade inte 2-trans-hexadecenal membranen på egen hand, men förstärkte starkt BAXs förmåga, särskilt i närvaro av BIM, att göra hål.
En dold tratt inuti BAX
För att ta reda på var och hur denna lipid verkar använde teamet en rad strukturella och biofysiska verktyg. De visade att 2-trans-hexadecenal binder till BAX utan att bilda permanenta kemiska bindningar, och att borttagning av BAXs naturliga cysteinhakar inte dämpar effekten. NMR-experiment avslöjade att bindning orsakar subtila förskjutningar i specifika aminosyror begravda inne i BAX, särskilt runt helixar kända som α5, α6 och α8. Datorbaserade modeller utifrån dessa förändringar avslöjade en tidigare förbisedd, trattformad kavitet i kärnan av BAX, täckt av den flexibla α8-helixen. När aktivatorn BIM engagerar BAX rör sig α8, tratten vidgas och dockningsimuleringar förutspår att lipidsvansen hos 2-trans-hexadecenal passar tätt in i den djupa nacken av denna hydrofoba tunnel. Författarna namnger denna ficka ”BAX actuating funnel”, eller BAF.
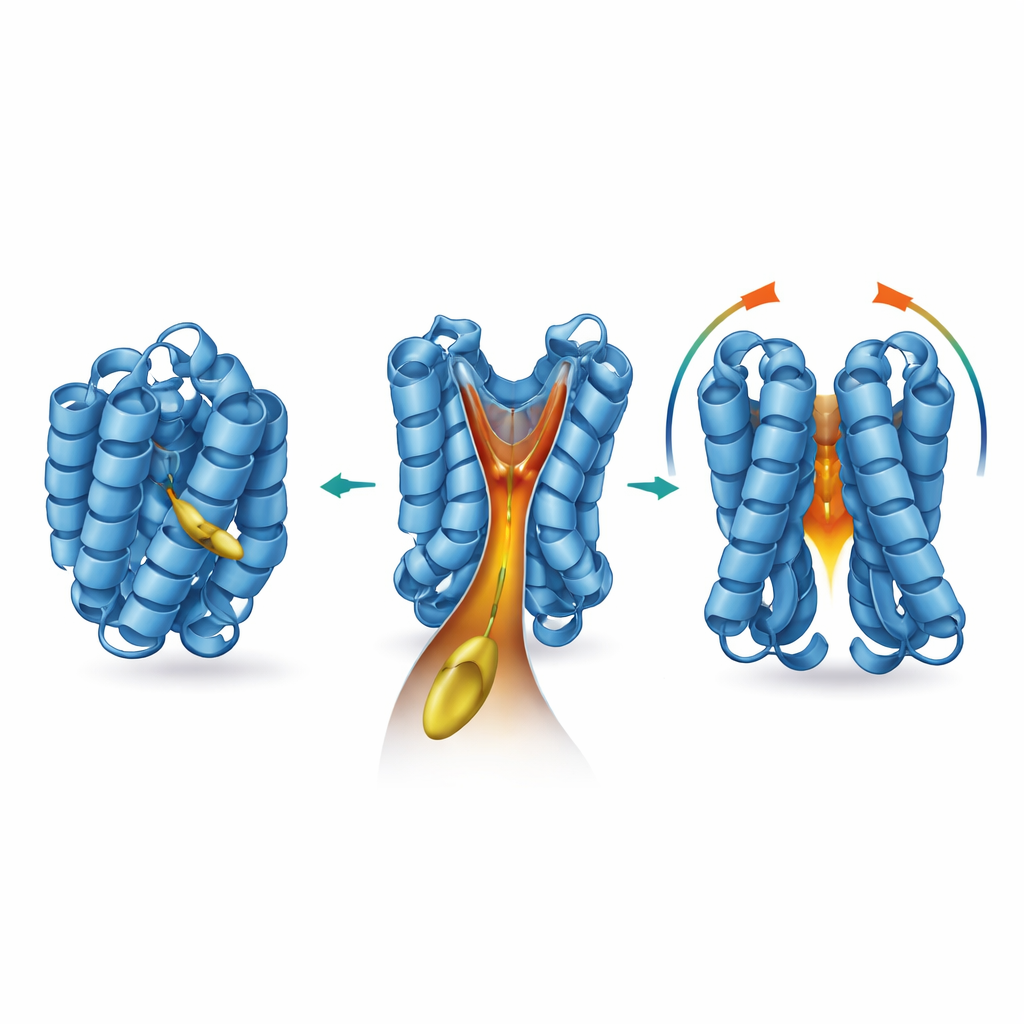
Finjustera tratten med kemi och mutationer
Forskarna frågade sedan vilka egenskaper hos lipiden och hos BAX som är avgörande för detta partnerskap. Kortare eller kemiskt förändrade versioner av lipiden kunde fortfarande komma i kontakt med BAX men var mycket mindre effektiva på att utlösa dess aktivering eller porbildande aktivitet. Däremot var långkedjade versioner som mest liknade 2-trans-hexadecenal bäst på att slå på BAX, vilket indikerar att kedjelängd och huvudgruppens struktur måste matcha trattens form. När teamet införde precisa mutationer som delvis fyllde igen eller förvrängde trattväggarna svarade BAX fortfarande på BIM men förlorade sin känslighet för 2-trans-hexadecenal. En naturligt viktig rest, prolin 168, som sitter i ett gångjärn mellan två helixar, visade sig styra tratten på avstånd. Att byta ut denna enda aminosyra omformade kaviteten, stabiliserade BAX i dess vilande form och gjorde både renade proteiner och celler mycket mindre responsiva mot lipidcofaktorn.
Hur lipider och proteiner samarbetar för att avsluta en cell
Sammantaget stödjer arbetet en stegvis bild av hur BAX aktiveras. Först binder aktivatorproteiner som BIM till BAX och startar tidiga omarrangemang, inklusive en uppluckring av α8-"grind"-helixen. Denna rörelse exponerar BAX actuating funnel, dit 2-trans-hexadecenal kan skjuta in som en kil. Att ockupera denna interna tunnel destabiliserar BAXs tätt packade kärna, gynnar exponering av dess interaktionsyta och främjar bildandet av dimerer och större kluster som perforerar mitokondriemembranet. Istället för att agera som ett enkelt membranlösningsmedel framträder denna bioaktiva lipid som en verklig molekylär partner som justerar BAXs beredskap att döda. Genom att definiera BAF som en kritisk kontrollpunkt öppnar studien dörren för att designa små molekyler som antingen kan öka BAX-aktivitet — potentiellt användbart mot cancer — eller dämpa den för att skydda friska vävnader vid degenerativa eller inflammatoriska sjukdomar.
Citering: Gelles, J.D., Chen, Y., Luna-Vargas, M.P.A. et al. A gated hydrophobic funnel within BAX binds bioactive lipids to potentiate pro-apoptotic function. Nat Commun 17, 3180 (2026). https://doi.org/10.1038/s41467-026-69836-9
Nyckelord: BAX, apoptos, bioaktiva lipider, mitokondrier, protein-lipid-interaktion