Clear Sky Science · ar
قُمع هيدروفوبي مُغلق داخل BAX يرتبط بالليبيذات النشيطة حيوياً لتعزيز وظيفة تحفيز الموت الخلوي المبرمج
كيف تساعد الدهون الخلايا على اتخاذ قرار الموت
يوميًا، تنهار ملايين من خلايانا بهدوء ذاتيًا للحفاظ على صحة الأنسجة وإزالة الخلايا التالفة أو الخطيرة. يعتمد هذا البرنامج الذاتي للموت، المسمى بالاستماتة (الابوبتوز)، على بروتينات قادرة على ثقب أغشية الميتوكوندريا، مصانع الطاقة في الخلية. يكشف هذا البحث كيف يساعد جزيء شبيه بالدهون في تحويل أحد هذه البروتينات، BAX، من مراقب صامت إلى منفذ فعال — كاشفًا عن «قُمع» مخفي داخل BAX قد يُستهدف يومًا ما بأدوية جديدة.
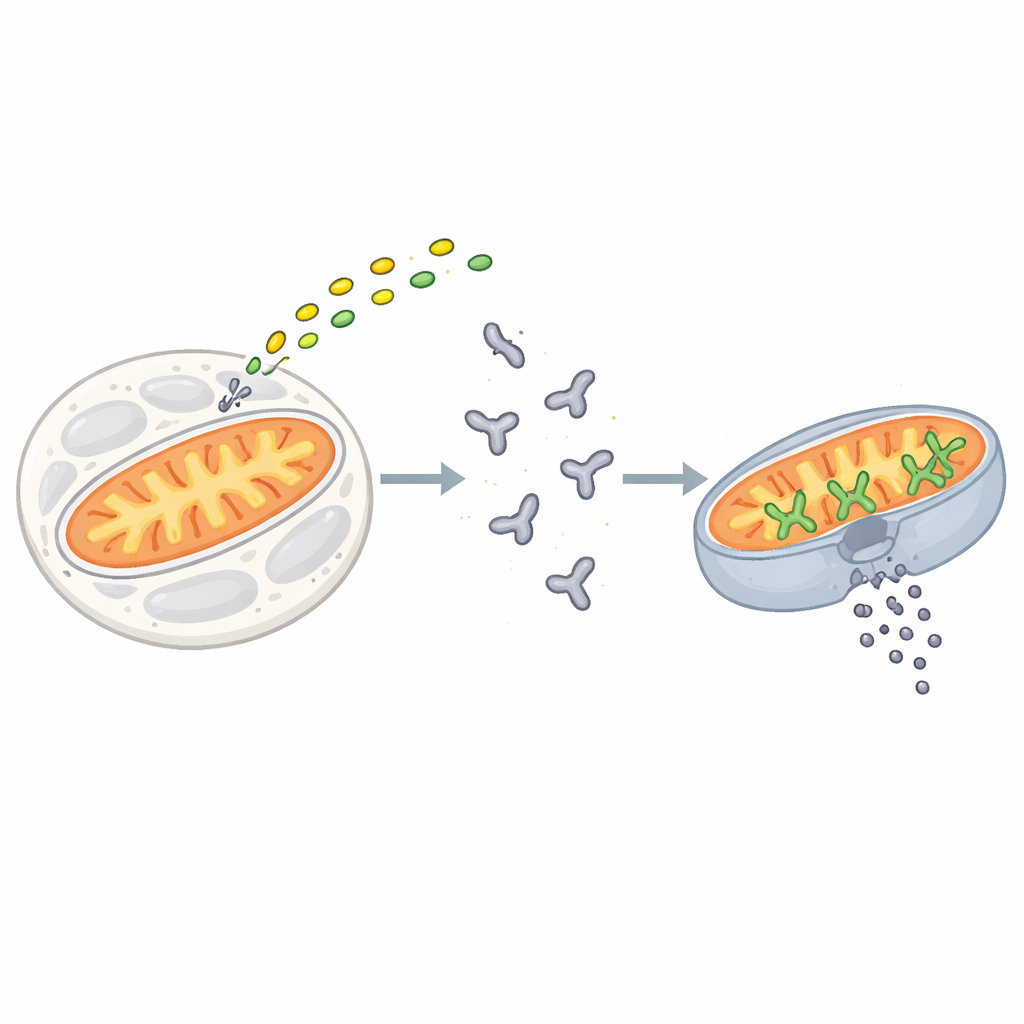
نقطة اللاعودة في الخلية
يُثار مسار الاستماتة عندما تتلاقى إشارات الإجهاد أو الضرر على عائلة من البروتينات تُعرف باسم بروتينات BCL‑2. يعد BAX واحدًا من المنفذين الرئيسيين في هذه العائلة. في الخلايا الهادئة، يطفو BAX في الوسط المائي كوحيد مطوي. عند وصول إشارات الموت، تلتصق بروتينات «المُفعِلة» القصيرة مثل BIM بـBAX وتبدأ سلسلة من التغييرات الشكلية التي تنقل BAX إلى السطح الخارجي للميتوكوندريا. هناك، يتجمع BAX في عناقيد تفتح مسامات كبيرة في الغشاء، مما يسمح لمحتويات الخلية الداخلية بالتسرب. هذا الحدث الذي لا رجعة فيه، المسمى نفاذية الغشاء الخارجي للميتوكوندريا، يمثل نقطة اللاعودة للخلية.
شريك ليبيدي تفاعلي يدخل المشهد
أشارت أعمال سابقة إلى أن منتج تحلل لجزيء الإشارة سفينغوزين‑1‑فوسفات، يُدعى 2‑ترانس‑هيكساديصينال، مطلوب لكي يشكل BAX مسامات بكفاءة. لكن لم يكن واضحًا ما إذا كان هذا الجزيء الدهني يغيّر الغشاء الميتوكوندري فحسب أم أنه يتلامس مباشرةً مع BAX. اختبر المؤلفون أولًا كيف يؤثر إضافة 2‑ترانس‑هيكساديصينال على خلايا الفئران الحية. من خلال تتبّع موت الخلايا في الوقت الحقيقي، وجدوا أن الليبيد بمفرده سبب قدرًا محدودًا من الاستماتة، لكن في وجود دواء يعطل شركاء BAX المضادين للموت ارتفع معدل موت الخلايا بشكل حاد — وفقط عندما كان BAX وقريبه القريب BAK موجودين. في أنظمة مُنقاة تستخدم فقاعات غشائية اصطناعية، لم يَحدث 2‑ترانس‑هيكساديصينال تلفًا بالغشاء بمفرده، لكنه عزز بشدة قدرة BAX، خاصةً عندما كان BIM حاضرًا أيضًا، على إحداث ثقوب.
قُمع مخفي داخل BAX
لاكتشاف أين وكيف يعمل هذا الليبيد، لجأ الفريق إلى مجموعة من الأدوات البنيوية والفيزيو‑كيميائية. أظهروا أن 2‑ترانس‑هيكساديصينال يرتبط بـBAX دون تكوين روابط كيميائية دائمة، وأن إزالة «مقابض» السيستئين الطبيعية في BAX لا تُقلل من التأثير. كشفت تجارب الرنين المغناطيسي النووي أن الارتباط يسبب تحولات دقيقة في أحماض أمينية محددة مدفونة داخل BAX، لا سيما حول الحلزونات المعروفة باسم α5 وα6 وα8. كشفت النماذج الحاسوبية المبنية على هذه التغييرات عن تجاويف على شكل قمع في قلب BAX، كانت مُهملة سابقًا، مغطاة بهلزة مرنة α8. عندما يلتقي المُفعّل BIM بـBAX، تتحرك α8، يتسع القمع، وتتنبأ محاكاة الترسّخ بأن سلسلة الليبيد في 2‑ترانس‑هيكساديصينال تلائم رقب هذا النفق الهيدروفوبي بارتياح. يسمي المؤلفون هذا الجيب «قُمع تشغيل BAX»، أو BAF.
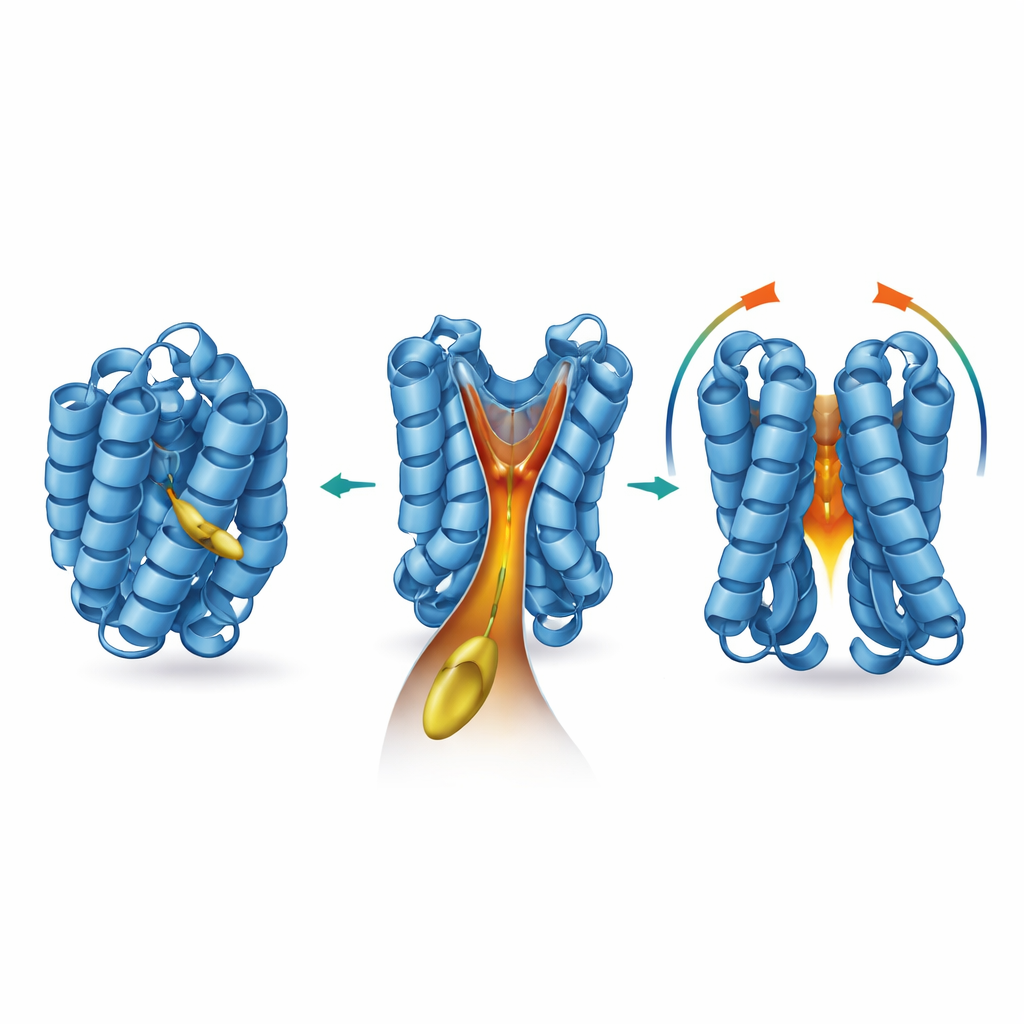
ضبط القمع بالكيمياء والطفرات
ثم تساءل الباحثون عن السمات الجوهرية لليبيد وBAX اللازمة لهذه الشراكة. النسخ الأقصر أو المعدلة كيميائيًا من الليبيد كان بإمكانها أن تلمس سطح BAX لكنها كانت أقل قدرة بكثير على تحفيز تنشيطه أو نشاط تشكيل المسامات. بالمقابل، كانت النسخ الطويلة الأكثر تشابهًا مع 2‑ترانس‑هيكساديصينال الأفضل في تشغيل BAX، مما يشير إلى أن طول السلسلة وبنية مجموعة الرأس يجب أن تتطابق مع شكل القمع. عندما أدخل الفريق طفرات دقيقة تملأ جدران القمع قليلاً أو تشوّهها، استمر BAX في الاستجابة لـBIM لكنه فقد حساسيتَه تجاه 2‑ترانس‑هيكساديصينال. تبين أن البقايا المهمة طبيعيًا، البرولين 168، الذي يجلس في مفصل بين حلزونيْن، يتحكم في القمع عن بُعد. أدى تغيير هذا الحامض الأميني الواحد إلى إعادة تشكيل التجويف، وتثبيت BAX في شكله الراكد، وجعل البروتينات المنقاة والخلايا أقل استجابة بكثير للمعاون الليبيدي.
كيف تتعاون الليبيدات والبروتينات لإنهاء حياة الخلية
مجتمعين، تدعم النتائج رؤية خطوة بخطوة لكيفية تنشيط BAX. أولًا، ترتبط بروتينات المُفعّل مثل BIM بـBAX وتبدأ إعادة ترتيب مبكرة، بما في ذلك إرخاء هلزة «الباب» α8. يكشف هذا الحركة عن قُمع تشغيل BAX، الذي يمكن أن يدخل فيه 2‑ترانس‑هيكساديصينال مثل إسفين. إن احتلال هذا النفق الداخلي يُزعزع تماسك قلب BAX المضغوط، ويُفضل انكشاف سطح تفاعله، ويُعزز تكوين ثنائيات وعناقيد أكبر تثقب الغشاء الميتوكوندري. بدلًا من العمل كمذيب بسيط للغشاء، يظهر هذا الليبيد النشيط حيويًا كشريك جزيئي حقيقي يضبط استعدادية BAX للقتل. من خلال تحديد BAF كموقع تحكم حاسم، يفتح هذا البحث الباب أمام تصميم جزيئات صغيرة إما لتعزيز نشاط BAX — وهو ما قد يكون مفيدًا ضد السرطان — أو لتقليله لحماية الأنسجة السليمة في أمراض التنكس أو الالتهاب.
الاستشهاد: Gelles, J.D., Chen, Y., Luna-Vargas, M.P.A. et al. A gated hydrophobic funnel within BAX binds bioactive lipids to potentiate pro-apoptotic function. Nat Commun 17, 3180 (2026). https://doi.org/10.1038/s41467-026-69836-9
الكلمات المفتاحية: BAX, الاستماتة (الابوبتوز), الليبيذات النشيطة حيوياً, الميتوكوندريا, تفاعل بروتين-ليبيد