Clear Sky Science · ru
Гидрофобный закрываемый «фонтан» внутри BAX связывает биоактивные липиды и усиливает проапоптотическую функцию
Как жиры помогают клеткам решать, когда умереть
Каждый день миллионы наших клеток бесшумно самоуничтожаются, чтобы поддерживать здоровье тканей и удалять повреждённые или опасные клетки. Эта встроенная программа суицида, называемая апоптозом, опирается на белки, способные проделывать дыры в мембранах митохондрий — энергетических центров клетки. В этом исследовании показано, как одна липидоподобная молекула помогает перевести один из таких белков, BAX, из тихого наблюдателя в эффективного палача — раскрывая скрытый «фонтан» в BAX, который в будущем может стать мишенью для новых лекарств.
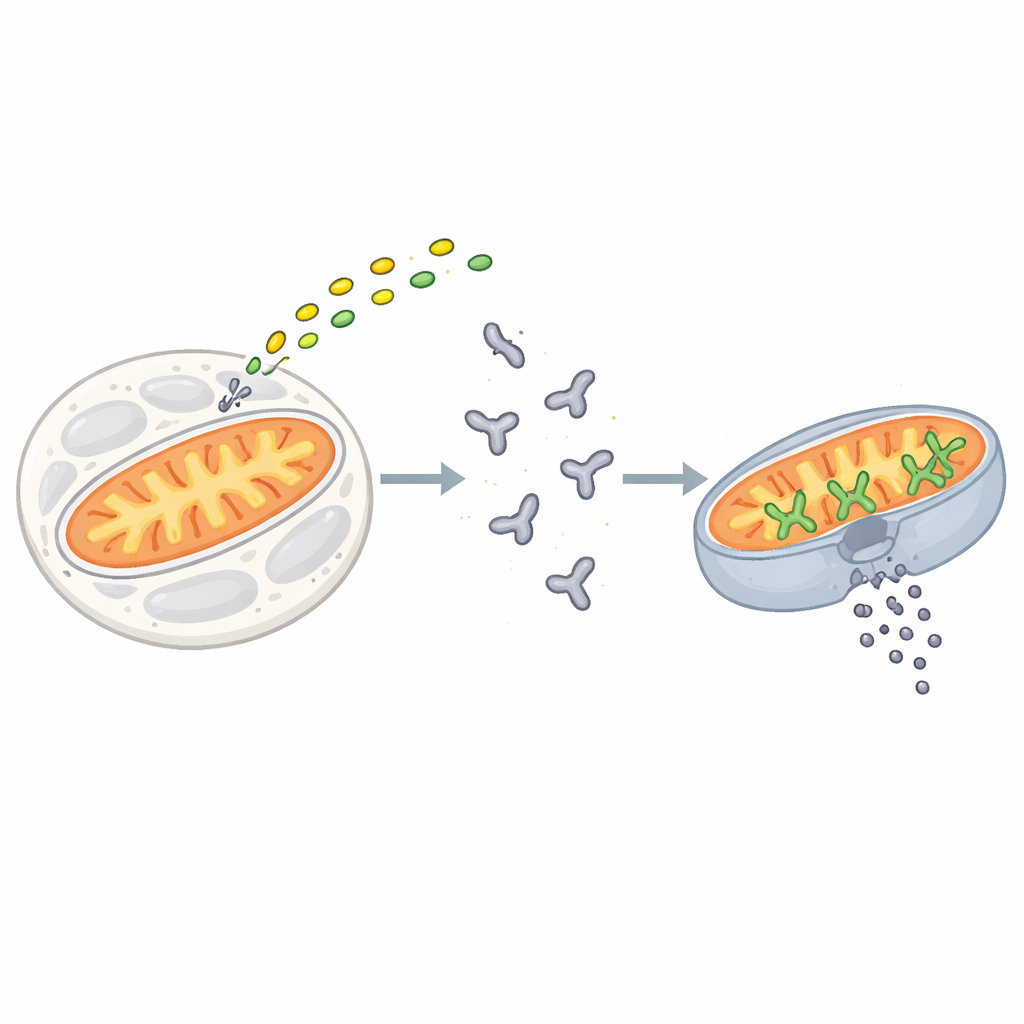
Точка невозврата для клетки
Апоптоз запускается, когда сигналы стресса или повреждения сходятся на семействе белков, известных как белки BCL‑2. BAX — один из ключевых исполнителей в этом семействе. В покоящихся клетках BAX плавает в водной среде как одиночная свернутая единица. Когда приходят сигналы смерти, короткие «активаторы», такие как BIM, прикрепляются к BAX и запускают серию конформационных изменений, переводящих BAX на внешнюю поверхность митохондрий. Там BAX собирается в кластеры, которые формируют большие поры в мембране, позволяя внутреннему содержимому вытекать наружу. Это необратимое событие, называемое проницаемостью внешней митохондриальной мембраны, отмечает точку невозврата для клетки.
На сцену выходит реактивный липидный партнёр
Ранее исследования намекали, что продукт распада сигнальной молекулы сфингозин‑1‑фосфата, называемый 2‑транс‑гексадеценаль, необходим для эффективного образования пор BAX. Но оставалось неясным, изменяет ли эта маслянистая молекула просто свойства митохондриальной мембраны или напрямую взаимодействует с BAX. Авторы сначала протестировали, как добавленный 2‑транс‑гексадеценаль влияет на живые клетки мыши. Отслеживая гибель клеток в реальном времени, они обнаружили, что сам по себе липид вызывает лишь ограниченный апоптоз, но в присутствии препарата, который подавляет антиапоптотические партнёры BAX, гибель клеток резко возрастала — и только при наличии BAX и его близкого родственника BAK. В очищённых системах с искусственными мембранными пузырьками 2‑транс‑гексадеценаль сам по себе не повреждал мембраны, но значительно усиливал способность BAX, особенно в присутствии BIM, проделывать дыры.
Скрытый «фонтан» внутри BAX
Чтобы выяснить, где и как действует этот липид, команда применила набор структурных и биофизических методов. Они показали, что 2‑транс‑гексадеценаль связывается с BAX без образования прочных ковалентных связей, и удаление природных цистеиновых «ручек» BAX не уменьшает эффекта. Эксперименты с ядерно‑магнитным резонансом выявили, что связывание вызывает тонкие сдвиги в отдельных аминокислотах, спрятанных внутри BAX, особенно вокруг спиралей, известных как α5, α6 и α8. Компьютерные модели, основанные на этих изменениях, обнаружили ранее пропущенную в центральной части BAX воронкообразную полость, закрытую гибкой спиралью α8. Когда активатор BIM взаимодействует с BAX, α8 смещается, воронка расширяется, а докинговые расчёты показывают, что липидная цепь 2‑транс‑гексадеценаля плотно помещается в глубокую шейку этого гидрофобного туннеля. Авторы называют этот карман «приводной воронкой BAX», или BAF.
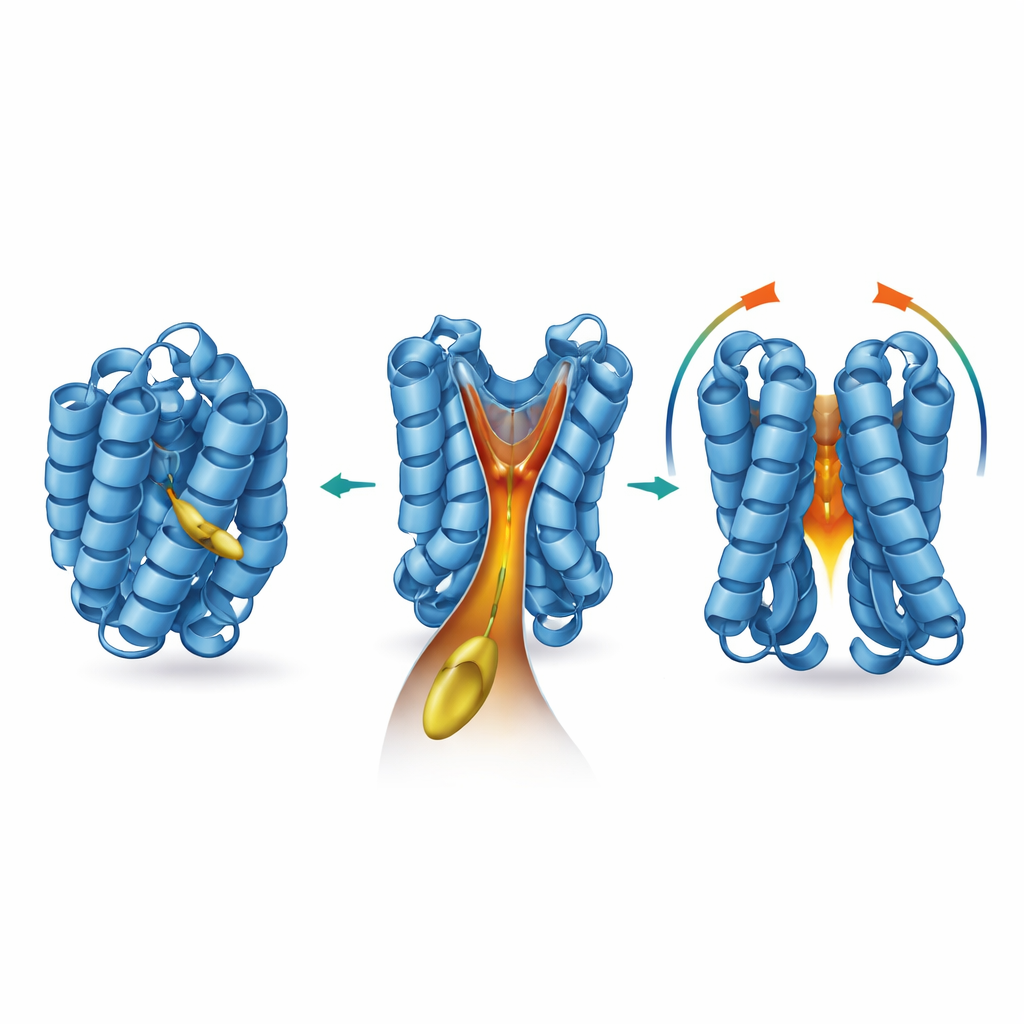
Настройка воронки химией и мутациями
Исследователи затем выясняли, какие особенности липида и самого BAX решающи для этого партнёрства. Более короткие или химически модифицированные версии липида всё ещё могли взаимодействовать с BAX, но были значительно менее способны вызывать его активацию или образование пор. Напротив, длинноцепочечные варианты, наиболее похожие на 2‑транс‑гексадеценаль, лучше всего включали BAX, указывая на то, что длина цепи и структура головной группы должны соответствовать форме воронки. Когда команда вводила точечные мутации, частично заполняющие или искажающие стенки воронки, BAX по‑прежнему реагировал на BIM, но терял чувствительность к 2‑транс‑гексадеценалю. Важная природная остаточная аминокислота, пролин 168, расположенный в шарнире между двумя спиралями, оказался способна управлять воронкой на расстоянии. Замена этой одной аминокислоты изменила форму полости, стабилизировала BAX в покоящейся форме и сделала как очищенные белки, так и клетки значительно менее чувствительными к липидному кофактору.
Как липиды и белки объединяются, чтобы убить клетку
В совокупности работа поддерживает поэтапную модель активации BAX. Сначала активаторы вроде BIM связываются с BAX и запускают ранние перестройки, включая ослабление «запорной» спирали α8. Это движение открывает приводную воронку BAX, в которую 2‑транс‑гексадеценаль может вставиться как клин. Заполнение внутреннего туннеля дестабилизирует плотно упакованный сердечник BAX, способствует обнажению взаимодействующих поверхностей и продвигает образование димеров и более крупных кластеров, перфорирующих митохондриальную мембрану. Вместо того чтобы действовать как простой растворитель мембраны, этот биоактивный липид выступает настоящим молекулярным партнёром, который настраивает готовность BAX к убийству. Определив BAF как критическую точку контроля, исследование открывает путь к созданию малых молекул, которые либо усиливают активность BAX — потенциально полезно против рака, — либо подавляют её для защиты здоровых тканей при дегенеративных или воспалительных заболеваниях.
Цитирование: Gelles, J.D., Chen, Y., Luna-Vargas, M.P.A. et al. A gated hydrophobic funnel within BAX binds bioactive lipids to potentiate pro-apoptotic function. Nat Commun 17, 3180 (2026). https://doi.org/10.1038/s41467-026-69836-9
Ключевые слова: BAX, апоптоз, биоактивные липиды, митохондрии, взаимодействие белок‑липид