Clear Sky Science · it
Un condotto idrofobico con sportello dentro BAX lega lipidi bioattivi per potenziare la funzione pro‑apoptotica
Come i grassi aiutano le cellule a decidere quando morire
Ogni giorno, milioni delle nostre cellule si autodistruggono silenziosamente per mantenere i tessuti sani ed eliminare cellule danneggiate o pericolose. Questo programma suicida incorporato, chiamato apoptosi, dipende da proteine in grado di praticare fori nelle membrane dei mitocondri, le centrali energetiche della cellula. Questo studio svela come una particolare molecola di tipo lipidico aiuti a trasformare una di queste proteine, BAX, da spettatrice silenziosa a esecutrice efficiente—rivelando un "condotto" nascosto in BAX che un giorno potrebbe essere preso di mira da nuovi farmaci.
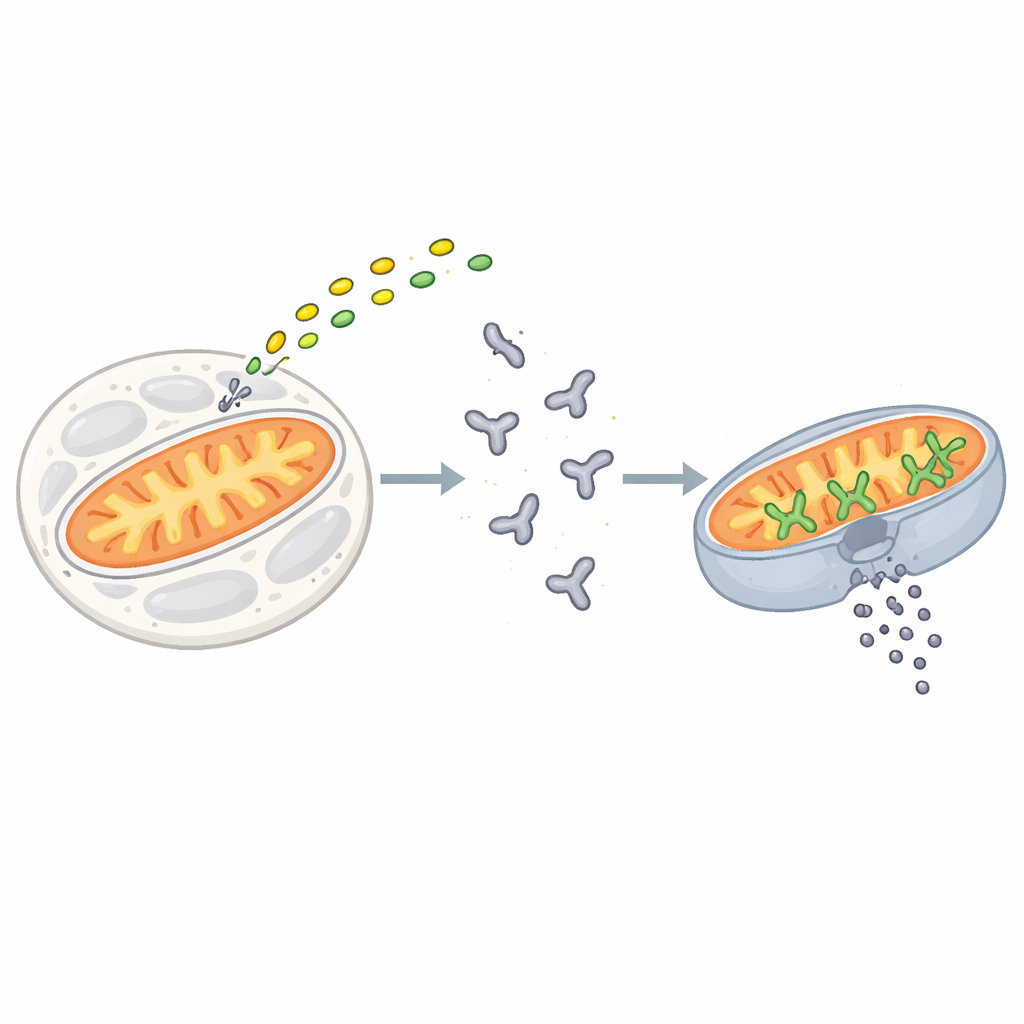
Il punto di non ritorno per una cellula
L'apoptosi viene innescata quando segnali di stress o di danno convergono su una famiglia di proteine note come proteine BCL‑2. BAX è uno dei principali esecutori di questa famiglia. Nelle cellule a riposo, BAX galleggia nel citosol come un'unità monomerica e ripiegata. Quando arrivano segnali di morte, brevi proteine "attivatrici" come BIM si agganciano a BAX e innescano una serie di cambiamenti conformazionali che trasferiscono BAX sulla superficie esterna dei mitocondri. Lì, BAX si organizza in ammassi che aprono grandi pori nella membrana, permettendo la fuoriuscita del contenuto interno. Questo evento irreversibile, chiamato permeabilizzazione della membrana esterna mitocondriale, segna il punto di non ritorno per la cellula.
Entra in scena un lipide reattivo
Studi precedenti suggerivano che un prodotto di degradazione della molecola di segnalazione sfingosina‑1‑fosfato, chiamato 2‑trans‑esadecenale, fosse necessario perché BAX formasse pori in modo efficiente. Ma non era chiaro se questa molecola oleosa altersse semplicemente la membrana mitocondriale o se toccasse direttamente BAX. Gli autori hanno prima testato come l'aggiunta di 2‑trans‑esadecenale influenzasse cellule di topo vive. Tracciando la morte cellulare in tempo reale, hanno riscontrato che il lipide da solo causava apoptosi limitata, ma in presenza di un farmaco che disattiva i partner anti‑morte di BAX la morte cellulare aumentava bruscamente—e solo quando BAX e il suo parente stretto BAK erano presenti. In sistemi purificati che usano bolle di membrana artificiali, il 2‑trans‑esadecenale non danneggiava da solo le membrane, ma aumentava fortemente la capacità di BAX, specialmente in presenza di BIM, di praticare fori.
Un condotto nascosto all'interno di BAX
Per capire dove e come agisce questo lipide, il gruppo si è rivolto a una serie di strumenti strutturali e biofisici. Hanno dimostrato che il 2‑trans‑esadecenale si lega a BAX senza formare legami chimici permanenti, e che rimuovere le "maniglie" di cisteina naturali di BAX non attenua l'effetto. Esperimenti di risonanza magnetica nucleare hanno rivelato che il legame provoca sottili spostamenti in specifici aminoacidi sepolti all'interno di BAX, soprattutto attorno alle eliche note come α5, α6 e α8. Modelli al computer basati su questi cambiamenti hanno scoperto una cavità a forma di imbuto precedentemente trascurata al cuore di BAX, chiusa dall'elica flessibile α8. Quando l'attivatore BIM si lega a BAX, α8 si muove, l'imbuto si allarga e simulazioni di docking prevedono che la catena lipidica del 2‑trans‑esadecenale si incastri nel profondo collo di questo tunnel idrofobico. Gli autori battezzano questa tasca "BAX actuating funnel", o BAF.
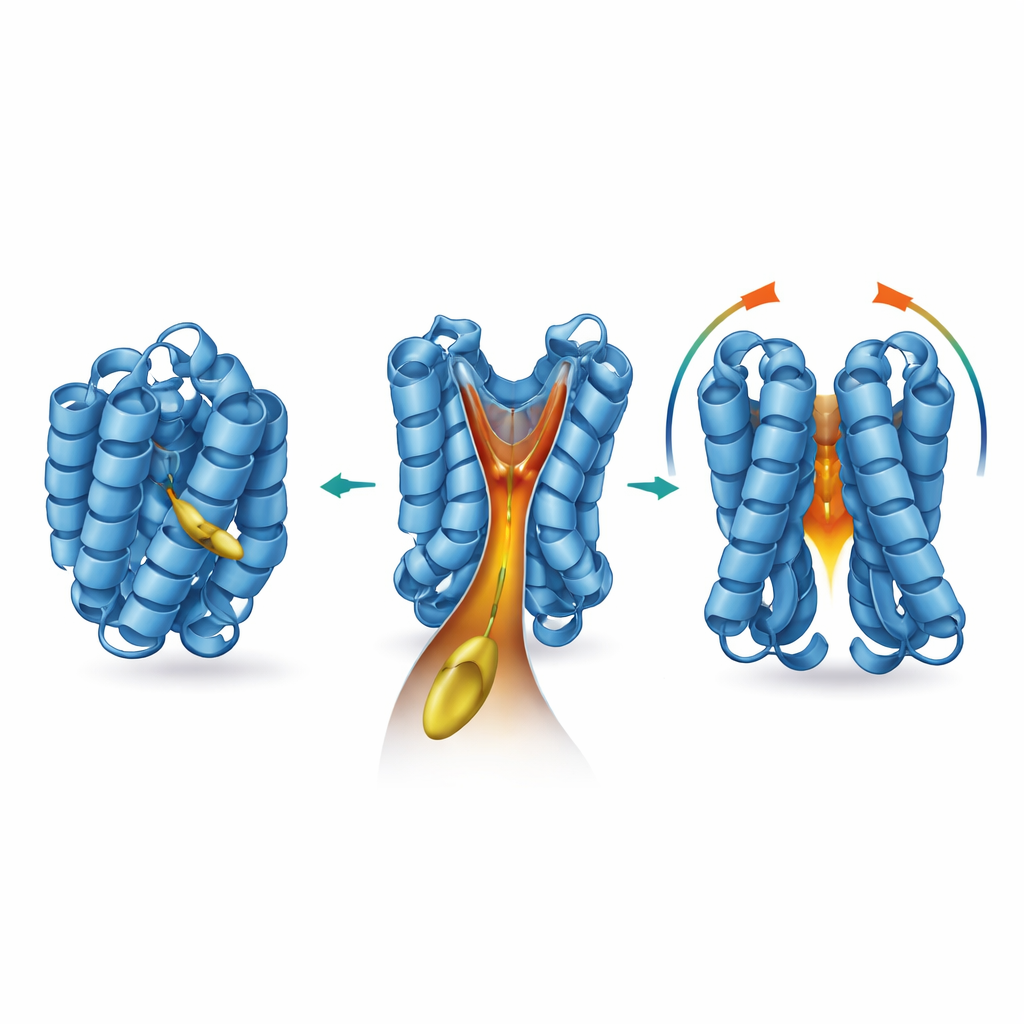
Regolare l'imbuto con chimica e mutazioni
I ricercatori hanno poi chiesto quali caratteristiche del lipide e dello stesso BAX siano cruciali per questa collaborazione. Versioni più corte o chimicamente alterate del lipide potevano ancora sfiorare BAX ma erano molto meno capaci di indurne l'attivazione o l'attività di formazione di pori. Al contrario, le versioni a catena lunga più simili al 2‑trans‑esadecenale erano le migliori nel attivare BAX, indicando che lunghezza della catena e struttura del gruppo terminale devono corrispondere alla forma dell'imbuto. Quando il gruppo ha introdotto mutazioni precise che riempivano leggermente o distorcevano le pareti dell'imbuto, BAX rispondeva ancora a BIM ma perdeva sensibilità al 2‑trans‑esadecenale. Un residuo naturalmente importante, la prolina 168, che si trova in una cerniera tra due eliche, si è rivelato controllare l'imbuto a distanza. Cambiare questo singolo aminoacido ha rimodellato la cavità, stabilizzato BAX nella sua forma a riposo e reso sia le proteine purificate sia le cellule molto meno reattive al co‑fattore lipidico.
Come lipidi e proteine fanno squadra per porre fine a una cellula
Nel complesso, il lavoro supporta una visione passo dopo passo di come BAX viene attivato. Per prima cosa, proteine attivatrici come BIM si legano a BAX e avviano i primi rimaneggiamenti, incluso l'allentamento dell'elica "porta" α8. Questo movimento espone il BAX actuating funnel, nel quale il 2‑trans‑esadecenale può inserirsi come uno cuneo. L'occupazione di questo tunnel interno destabilizza il nucleo strettamente impacchettato di BAX, favorisce l'esposizione della sua superficie di interazione e promuove la formazione di dimeri e ammassi più grandi che perforano la membrana mitocondriale. Piuttosto che agire come un semplice solvente di membrana, questo lipide bioattivo emerge come un vero partner molecolare che regola la prontezza di BAX a uccidere. Definendo il BAF come sito di controllo critico, lo studio apre la strada alla progettazione di piccole molecole che possano aumentare l'attività di BAX—potenzialmente utili contro il cancro—or ridurla per proteggere i tessuti sani in malattie degenerative o infiammatorie.
Citazione: Gelles, J.D., Chen, Y., Luna-Vargas, M.P.A. et al. A gated hydrophobic funnel within BAX binds bioactive lipids to potentiate pro-apoptotic function. Nat Commun 17, 3180 (2026). https://doi.org/10.1038/s41467-026-69836-9
Parole chiave: BAX, apoptosi, lipidi bioattivi, mitocondri, interazione proteina-lipide