Clear Sky Science · fr
Un entonnoir hydrophobe à verrouillage dans BAX lie des lipides bioactifs pour potentialiser la fonction pro‑apoptotique
Comment les graisses aident les cellules à décider de mourir
Chaque jour, des millions de nos cellules s’autodétruisent discrètement pour préserver la santé des tissus et éliminer les cellules endommagées ou dangereuses. Ce programme suicidaire intégré, appelé apoptose, repose sur des protéines capables de percer les membranes des mitochondries, les centrales énergétiques de la cellule. Cette étude révèle comment une molécule de type lipide aide à convertir l’une de ces protéines, BAX, d’un observateur inactif en un exécuteur efficace — dévoilant un « entonnoir » caché dans BAX qui pourrait un jour être ciblé par de nouveaux médicaments.
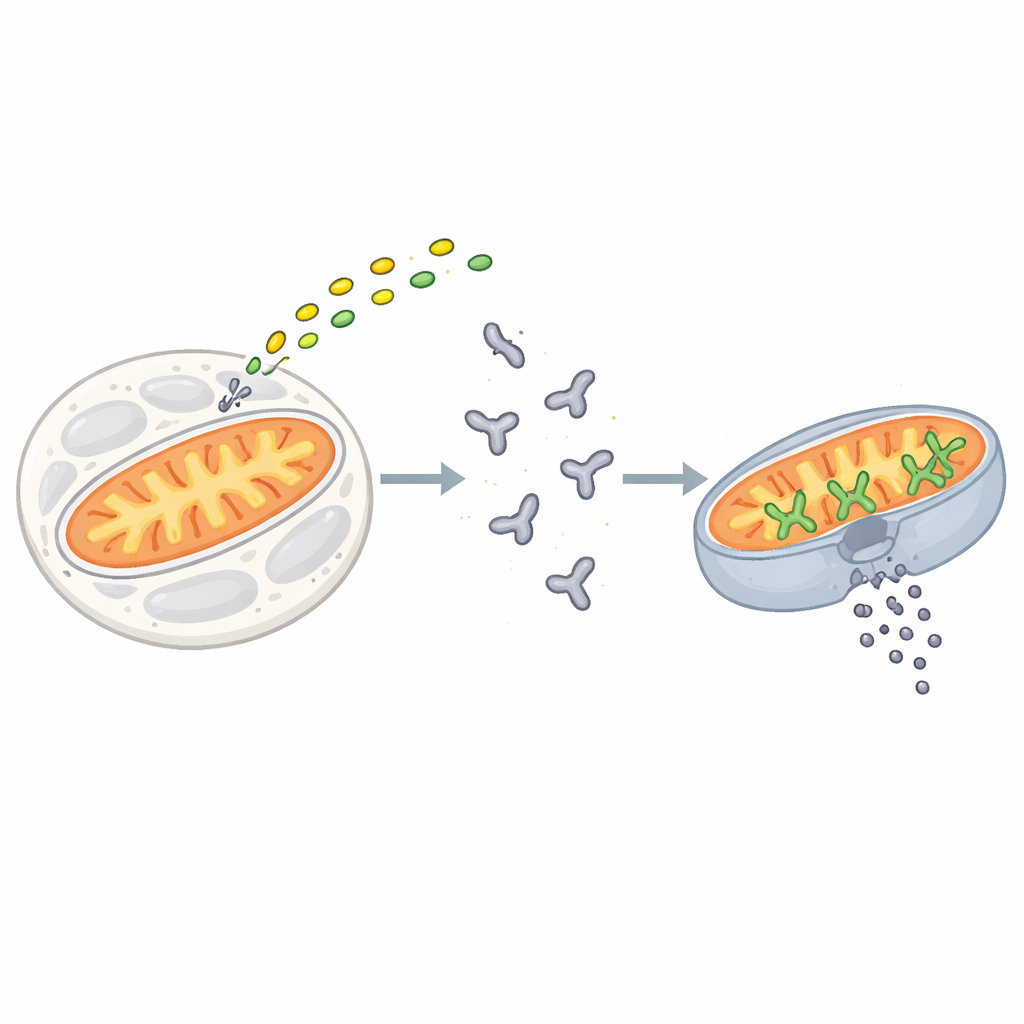
Le point de non‑retour d’une cellule
L’apoptose est déclenchée lorsque des signaux de stress ou de dommage convergent sur une famille de protéines connues sous le nom de protéines BCL‑2. BAX est l’un des principaux acteurs de cette famille. Dans les cellules au repos, BAX circule dans le cytosol sous la forme d’une unité repliée monomérique. Quand les signaux de mort apparaissent, de courtes protéines « activateurs » comme BIM se fixent sur BAX et initient une série de changements de conformation qui déplacent BAX vers la surface externe des mitochondries. Là, BAX s’assemble en amas qui ouvrent de larges pores dans la membrane, permettant au contenu interne de s’échapper. Cet événement irréversible, appelé perméabilisation de la membrane externe mitochondriale, marque le point de non‑retour pour une cellule.
Un lipide réactif entre en scène
Des travaux antérieurs suggéraient qu’un produit de dégradation du messager sphingosine‑1‑phosphate, nommé 2‑trans‑hexadécénal, est nécessaire pour que BAX forme des pores efficacement. Mais il n’était pas clair si cette molécule huileuse modifiait simplement la membrane mitochondriale ou si elle interagissait directement avec BAX. Les auteurs ont d’abord testé l’effet du 2‑trans‑hexadécénal ajouté sur des cellules de souris vivantes. En suivant la mort cellulaire en temps réel, ils ont constaté que le lipide seul provoquait une apoptose limitée, mais qu’en présence d’un médicament qui désactive les partenaires anti‑mort de BAX, la mortalité cellulaire augmentait fortement — et seulement lorsque BAX et son proche parent BAK étaient présents. Dans des systèmes purifiés utilisant des vésicules membranaires artificielles, le 2‑trans‑hexadécénal n’endommageait pas les membranes par lui‑même, mais renforçait nettement la capacité de BAX, surtout en présence de BIM, à percer des trous.
Un entonnoir caché à l’intérieur de BAX
Pour savoir où et comment ce lipide agit, l’équipe a eu recours à une batterie d’outils structuraux et biophysiques. Ils ont montré que le 2‑trans‑hexadécénal se lie à BAX sans former de liaisons chimiques permanentes, et que la suppression des cystéines naturelles de BAX ne diminue pas l’effet. Des expériences de résonance magnétique nucléaire ont révélé que la liaison induit des déplacements subtils d’acides aminés spécifiques enfouis dans BAX, en particulier autour des hélices désignées α5, α6 et α8. Des modèles informatiques basés sur ces changements ont mis au jour une cavité en forme d’entonnoir au cœur de BAX, jusque‑là négligée, fermée par l’hélice flexible α8. Lorsque l’activateur BIM engage BAX, α8 se déplace, l’entonnoir s’élargit, et des simulations de docking prédisent que la chaîne lipidique du 2‑trans‑hexadécénal s’insère parfaitement dans le col profond de ce tunnel hydrophobe. Les auteurs nomment ce site la « BAX actuating funnel », ou BAF.
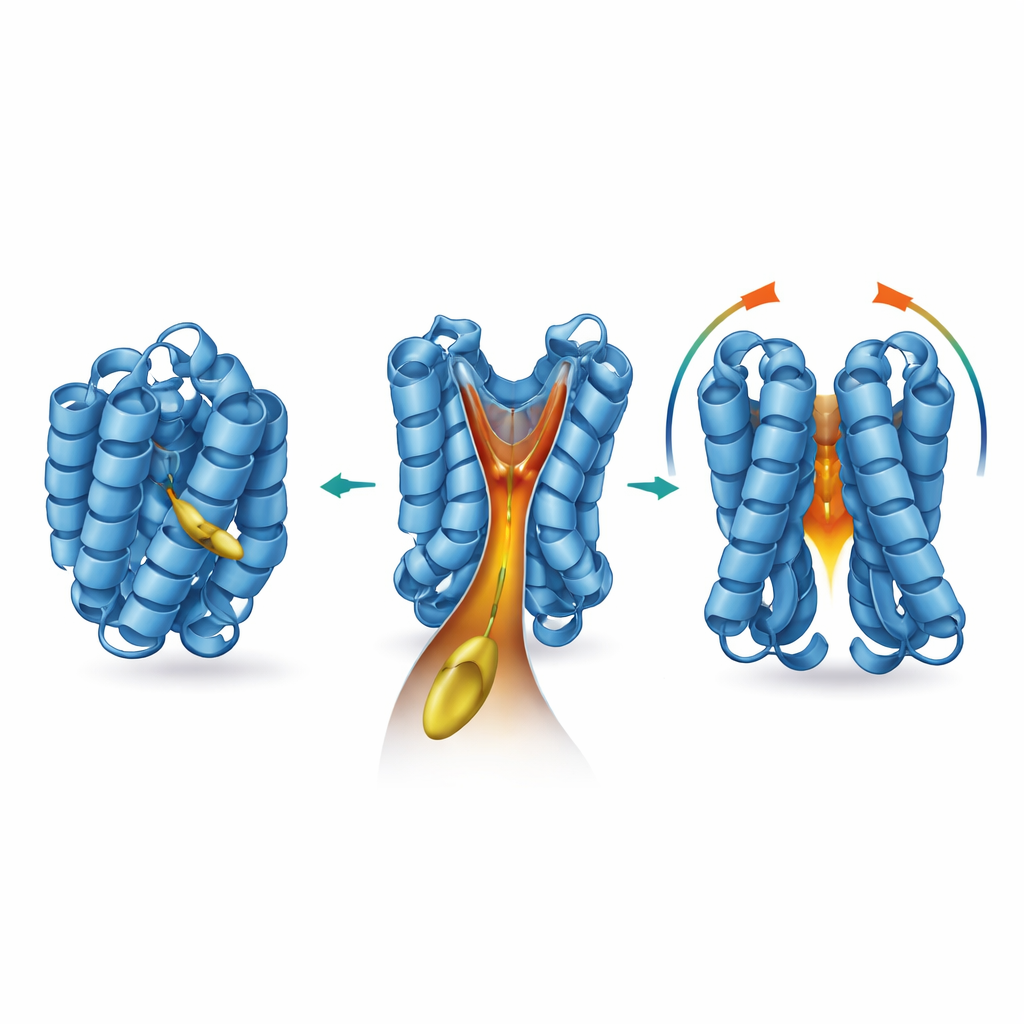
Accorder l’entonnoir par chimie et mutations
Les chercheurs ont ensuite cherché à savoir quelles caractéristiques du lipide et de BAX lui‑même sont cruciales pour ce partenariat. Des versions plus courtes ou chimiquement modifiées du lipide pouvaient encore frôler BAX mais étaient beaucoup moins capables de déclencher son activation ou son activité de formation de pores. En revanche, les versions à chaîne longue les plus proches du 2‑trans‑hexadécénal étaient les plus efficaces pour activer BAX, indiquant que la longueur de la chaîne et la structure du groupe tête doivent correspondre à la forme de l’entonnoir. Lorsque l’équipe introduisit des mutations précises qui remplissaient légèrement ou déformaient les parois de l’entonnoir, BAX répondait toujours à BIM mais perdait sa sensibilité au 2‑trans‑hexadécénal. Un résidu naturellement important, la proline 168, située dans une charnière entre deux hélices, contrôlait à distance l’entonnoir. Le changement de cet acide aminé unique remodelait la cavité, stabilisait BAX dans sa forme au repos, et rendait tant les protéines purifiées que les cellules beaucoup moins réactives au co‑facteur lipidique.
Comment les lipides et les protéines s’unissent pour terminer une cellule
Ensemble, ces résultats soutiennent une vue progressive de l’activation de BAX. D’abord, des protéines activateurs comme BIM se lient à BAX et initient des réarrangements précoces, incluant le relâchement de l’hélice « porte » α8. Ce mouvement expose l’entonnoir activateur de BAX, dans lequel le 2‑trans‑hexadécénal peut s’insérer comme un coin. L’occupation de ce tunnel interne déstabilise le cœur fortement empaqueté de BAX, favorise l’exposition de sa surface d’interaction, et promeut la formation de dimères et d’amas plus larges qui perforent la membrane mitochondriale. Plutôt que d’agir comme un simple solvant membranaire, ce lipide bioactif apparaît comme un véritable partenaire moléculaire qui module la propension de BAX à tuer. En définissant la BAF comme un site de contrôle critique, l’étude ouvre la voie à la conception de petites molécules qui renforcent l’activité de BAX — potentiellement utiles contre le cancer — ou qui l’atténuent pour protéger les tissus sains dans des maladies dégénératives ou inflammatoires.
Citation: Gelles, J.D., Chen, Y., Luna-Vargas, M.P.A. et al. A gated hydrophobic funnel within BAX binds bioactive lipids to potentiate pro-apoptotic function. Nat Commun 17, 3180 (2026). https://doi.org/10.1038/s41467-026-69836-9
Mots-clés: BAX, apoptose, lipides bioactifs, mitochondries, interaction protéine‑lipide