Clear Sky Science · zh
高效 CRISPR 敲入显示 TCF1 无法单独逆转 T 细胞耗竭
为何疲惫的免疫细胞重要
我们的免疫系统依赖杀伤性 T 细胞去追踪被病毒感染或发生癌变的细胞。但当这些威胁持续数月时,T 细胞会变得“耗竭”,丧失大部分战斗力。部分耗竭细胞表现得更像干细胞,能够持续更新反应并有助于现代癌症免疫疗法发挥作用。本研究提出了一个看似简单却对治疗有重大影响的问题:通过启动一个名为 TCF1 的主控基因,能否把衰老的 T 细胞重新推回那种年轻的、干样状态?
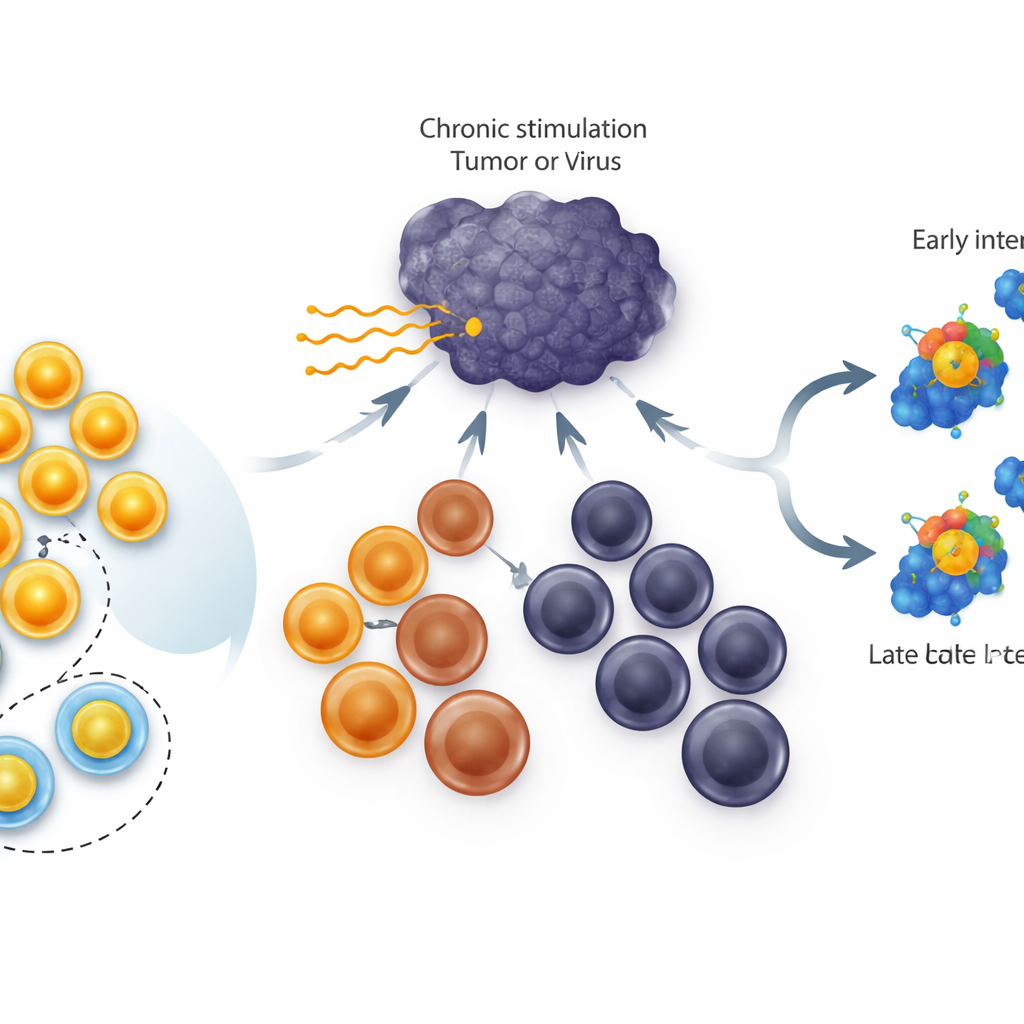
耗竭 T 细胞的不同类型
在慢性感染和肿瘤中,杀伤性 T 细胞并非简单关闭;它们会经过一系列分化阶段。处于顶端的是分裂能力强并能产生新战斗细胞的干样细胞。中间是仍能参与疾病控制的“中间”细胞,底端则是灵活性极低的终末耗竭细胞。基因 TCF1 在干样群体中高度活跃,被认为对其形成和存活至关重要。既往工作显示,在所有耗竭细胞中持续提高 TCF1 水平可以扩大干样细胞的池子。但尚不清楚的是,TCF1 是否真的能把处于更晚期的耗竭细胞逆转回那种干样状态。
在小鼠中建立精确的基因编辑工具
为了解答这一问题,研究者首先需要一种能够在不干扰体内自然行为的前提下,高效向小鼠 T 细胞插入新 DNA 的方法。他们优化了一种基于同源重组修复的 CRISPR 编辑策略,使用 AAV6 病毒作为模板在基因组的精确位置“敲入”新的遗传载荷。通过谨慎激活 T 细胞、递送 CRISPR 组分、在体外短暂休整细胞然后将其转入小鼠体内,他们能够达到 40–80% 的敲入率——这一水平与或优于传统病毒过表达方法。他们还展示了如何在不破坏重要宿主基因的情况下插入基因,以及如何定位特定的基因位点以便新基因仅在特定 T 细胞亚群中被激活。
早期开启 TCF1 与晚期开启的对比
研究的核心比较了两种开启 TCF1 的策略。一种是将 TCF1 插入在所有 T 细胞都活跃的位置,使得在应答开始时 TCF1 就维持高表达。另一种则将 TCF1 插入到 Cx3cr1 基因中,该基因仅在干样细胞向中间耗竭状态成熟时才被激活。第二种设计像一个条件开关,仅在细胞已经沿耗竭路径向下移动后才翻开 TCF1。当这些改造的 T 细胞在一个成熟的慢性病毒感染模型中测试时,持续表达 TCF1 明显扩增了干样细胞池。相比之下,仅在中间细胞中开启 TCF1 并未增加干样细胞的数量,尽管这些中间细胞每个细胞产生的 TCF1 与持续表达组相当或更多。
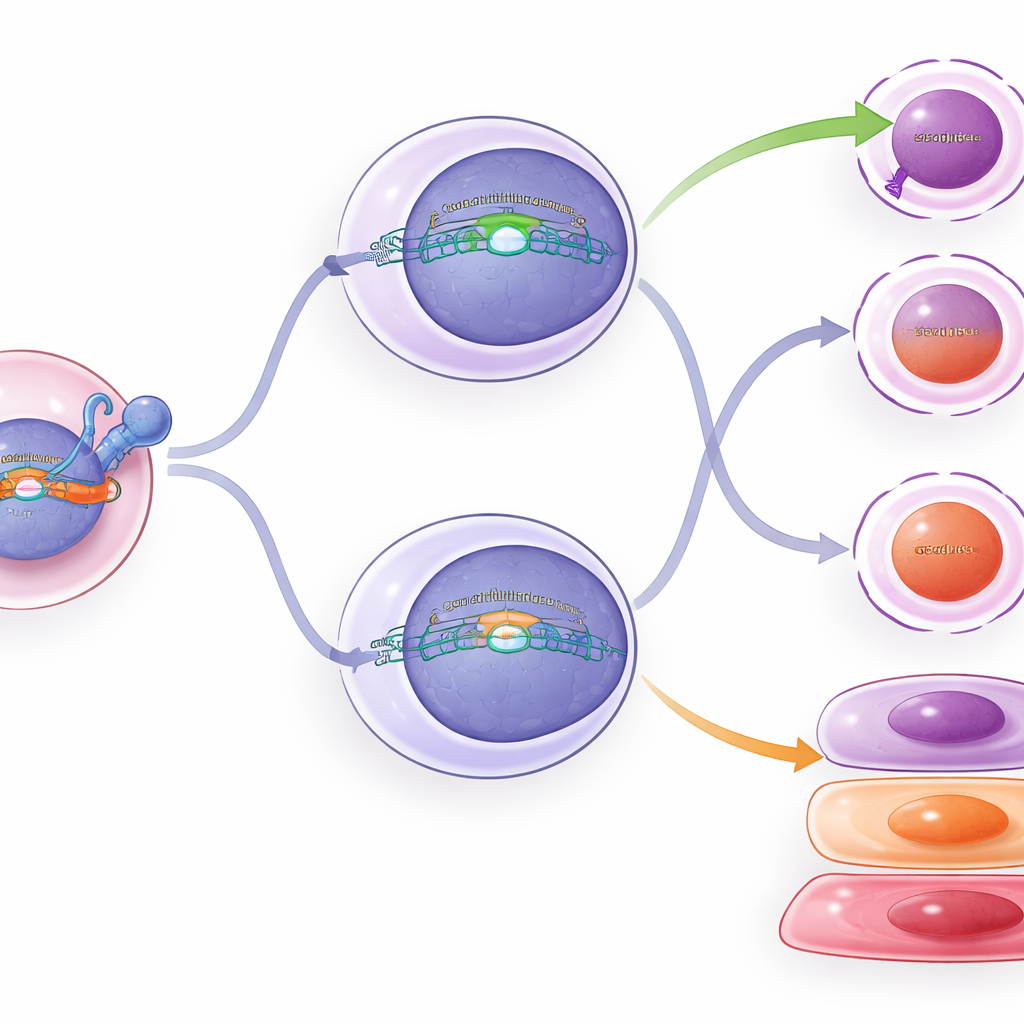
重编程细胞内部发生了什么
为了超越简单的细胞计数,团队对数千个单个 T 细胞的基因表达和染色质(控制哪些基因可被激活的 DNA 包装)进行了分型分析。持续表达 TCF1 的细胞显示出更多的干样簇和早期效应样细胞,这与 TCF1 减缓向深度耗竭推进一致。将 TCF1 有条件地表达在中间细胞中仅引起细微变化:部分基因模式和染色质特征向干样细胞倾斜,耗竭标志略有下降。流式细胞术证实了这些轻微改变——携带额外 TCF1 的中间细胞在某些杀伤和耗竭相关蛋白上略低,而在与干样细胞相关的标志上稍高——但它们并未在身份上完全逆转。
为何单一基因无法把时间倒流
对非专业读者来说,关键结论是:一旦 T 细胞沿耗竭之路走得足够远,单纯重新激活 TCF1 并不足以将它们送回年轻的干样状态。从早期就持续存在的 TCF1 有助于维持干样细胞,实际上起到减缓“衰老”的作用,但事后想要撤销耗竭则无法仅靠它。这对癌症免疫疗法有重要含义:仅靠提升 TCF1 来使高度耗竭的 T 细胞复苏的策略不太可能成功。相反,成功的治疗可能需要组合多种因子,或集中在保护并扩增干样细胞池,趁细胞尚未过度耗竭之前进行干预。
引用: de Menezes, M.N., Chen, A.X.Y., Kulkarni, N. et al. High efficiency CRISPR knock-in demonstrates that TCF1 is insufficient to reverse T cell exhaustion. Nat Commun 17, 2857 (2026). https://doi.org/10.1038/s41467-026-69671-y
关键词: T 细胞耗竭, TCF1, CRISPR 敲入, 癌症免疫疗法, 干样 T 细胞