Clear Sky Science · pl
Wysoka wydajność wprowadzania przez CRISPR pokazuje, że TCF1 nie wystarcza do odwrócenia wyczerpania limfocytów T
Dlaczego zmęczone komórki odpornościowe mają znaczenie
Nasz układ odpornościowy polega na cytotoksycznych limfocytach T, które tropią komórki zainfekowane wirusem i komórki nowotworowe. Gdy zagrożenia utrzymują się miesiącami, limfocyty T mogą ulec „wyczerpaniu”, tracąc dużą część swojej siły. Szczególna podgrupa tych komórek zachowuje się bardziej jak komórki macierzyste, ciągle odnawiając odpowiedź i wspierając działanie nowoczesnych immunoterapii przeciwnowotworowych. W tym badaniu postawiono pozornie proste pytanie o wielkie implikacje terapeutyczne: czy możemy przepchnąć wyczerpane limfocyty T z powrotem w młodszy, macierzysty stan, aktywując pojedynczy gen regulatorowy zwany TCF1?
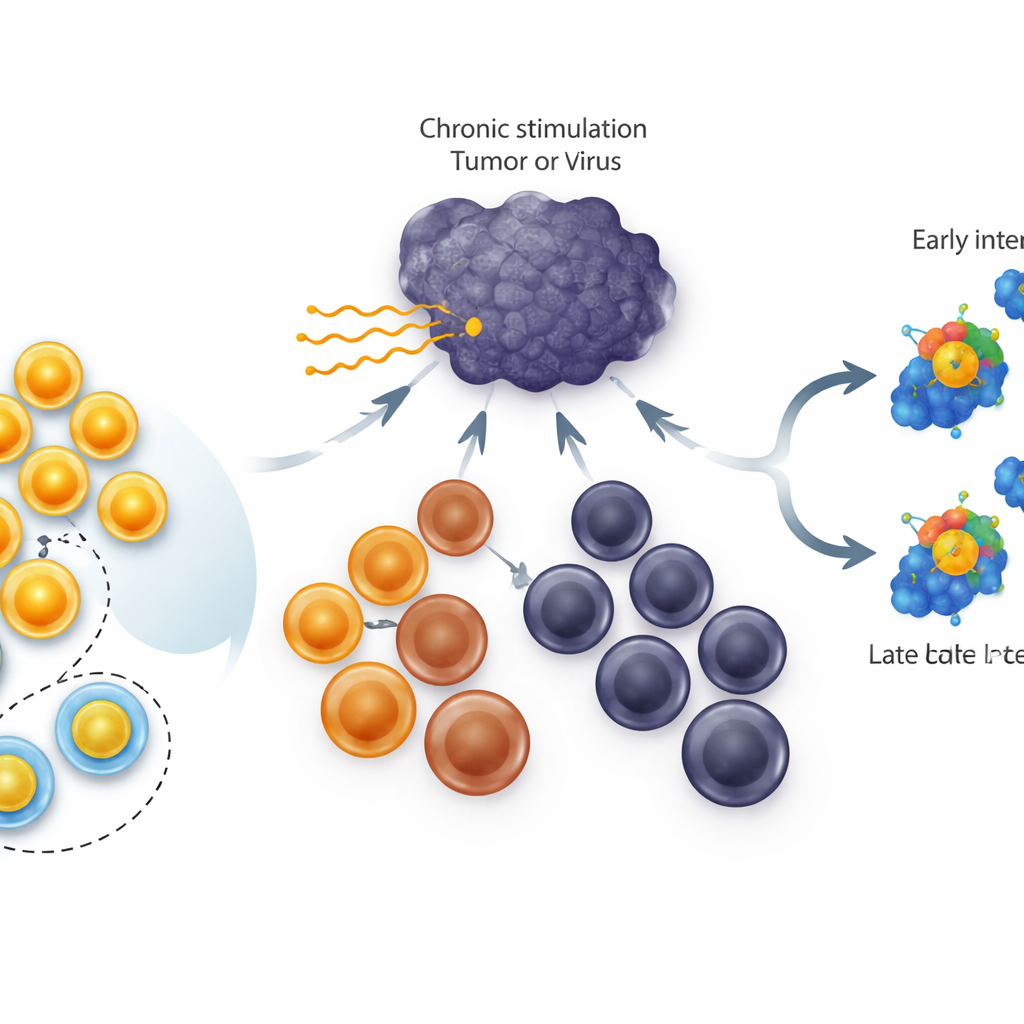
Różne odmiany zmęczonych limfocytów T
W przewlekłych infekcjach i nowotworach cytotoksyczne limfocyty T nie wyłączają się po prostu; przechodzą przez drabinę stanów. Na szczycie znajdują się komórki o cechach macierzystych, które dobrze się dzielą i mogą dawać początek nowym walcznikom. W środku są komórki „pośrednie”, które nadal pomagają kontrolować chorobę, a na dole leżą komórki terminalnie wyczerpane, mające niewielką elastyczność. Gen TCF1 jest silnie aktywny w grupie o cechach macierzystych i wiadomo, że jest niezbędny do ich powstawania i przetrwania. Wcześniejsze prace wykazały, że stałe zwiększanie poziomu TCF1 we wszystkich wyczerpanych komórkach powiększa pulę komórek macierzystych. Nie było jednak jasne, czy TCF1 może faktycznie cofnąć bardziej zaawansowane, wyczerpane komórki z powrotem w górę tej drabiny do stanu macierzystego.
Budowanie precyzyjnego zestawu do edycji genów u myszy
Aby się tym zająć, badacze najpierw potrzebowali bardzo skutecznego sposobu wstawiania nowego DNA do mysich limfocytów T bez zakłócania ich naturalnego zachowania w organizmie. Optymalizowali naprawę homologiczną kierowaną przez CRISPR, która używa wirusowego szablonu AAV6 do „wprowadzania” nowego ładunku genetycznego w precyzyjne miejsca w genomie. Poprzez staranne aktywowanie limfocytów T, dostarczenie składników CRISPR, krótkie odroczenie komórek w laboratorium, a następnie przeszczepienie ich do myszy, osiągnęli wskaźniki wprowadzenia na poziomie 40–80 procent — poziomy porównywalne lub lepsze niż tradycyjne nadekspresje wirusowe. Pokaźnie też udowodnili, jak wstawiać geny bez uszkadzania ważnych genów gospodarza oraz jak celować w konkretne adresy genetyczne, by nowy gen włączał się tylko w określonych podzbiorach limfocytów T.
Włączanie TCF1 wcześnie versus późno
Rdzeniem pracy jest porównanie dwóch strategii włączania TCF1. W jednej zespół wstawił TCF1 w miejsce aktywne we wszystkich limfocytach T, więc TCF1 był wysoki od początku reakcji. W drugiej wstawili TCF1 do genu Cx3cr1, który uaktywnia się dopiero, gdy komórki o cechach macierzystych dojrzewają do stanu pośredniego wyczerpania. Ten drugi projekt działa jak warunkowy przełącznik, włączając TCF1 dopiero po tym, jak komórki zeszły ścieżką wyczerpania. Gdy zmodyfikowane limfocyty T przetestowano w dobrze ustalonym modelu przewlekłej infekcji wirusowej, stała ekspresja TCF1 wyraźnie powiększyła pulę komórek o cechach macierzystych. Natomiast włączanie TCF1 jedynie w komórkach pośrednich nie zwiększyło liczby komórek macierzystych, mimo że te komórki pośrednie produkowały tyle samo lub więcej TCF1 na komórkę niż układ z ciągłą ekspresją.
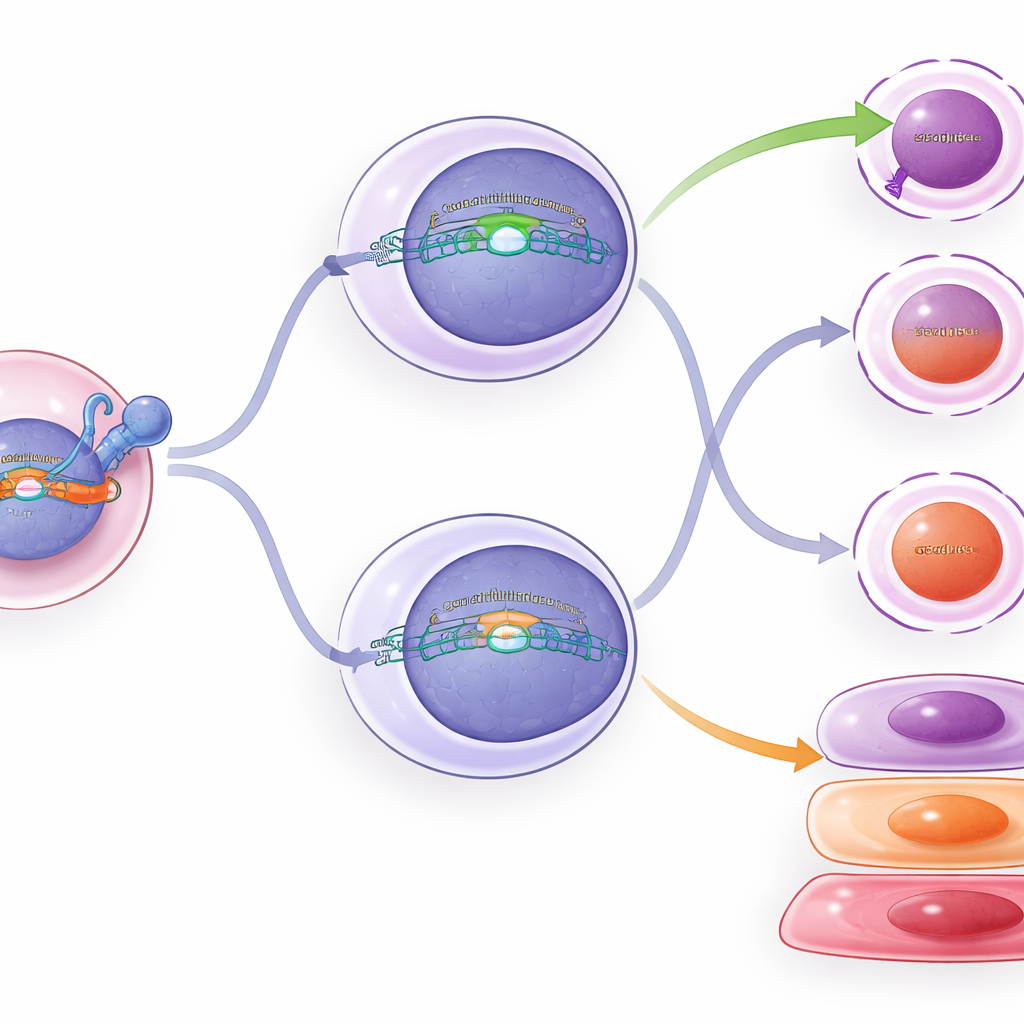
Co dzieje się wewnątrz przestawionych komórek
Aby zajrzeć dalej niż proste liczenie komórek, zespół profilował aktywność genów i chromatynę (pakowanie DNA, które kontroluje, które geny mogą się włączać) w tysiącach pojedynczych limfocytów T. Komórki ze stałą ekspresją TCF1 wykazywały więcej klastrów o cechach macierzystych i wczesnych komórek efektorowych, co zgadza się z rolą TCF1 w spowalnianiu marszu w kierunku głębokiego wyczerpania. Warunkowe TCF1 w komórkach pośrednich powodowało tylko subtelne przesunięcia: niektóre wzory genów i cechy chromatyny przesunęły się w stronę tych obserwowanych w komórkach macierzystych, a markery wyczerpania nieznacznie spadły. Cytometria przepływowa potwierdziła te łagodne zmiany — komórki pośrednie z dodatkowym TCF1 miały nieco mniej niektórych białek związanych z zabijaniem i wyczerpaniem oraz nieco więcej markera związanego z komórkami macierzystymi — ale nie zredukowały swojej tożsamości całkowicie.
Dlaczego jeden gen nie cofa czasu
Dla nietechnicznego odbiorcy kluczowy przekaz jest taki: gdy limfocyty T przejdą wystarczająco daleko ścieżką wyczerpania, samo ponowne uruchomienie TCF1 nie wystarczy, by przywrócić je do młodszego, macierzystego stanu. Stała obecność TCF1 pomaga zachować komórki macierzyste, jeśli występuje od najwcześniejszych etapów, skutecznie spowalniając „starzenie”, ale nie potrafi cofnąć wyczerpania po fakcie. Ma to istotne konsekwencje dla immunoterapii przeciwnowotworowej: strategie próbujące odmłodzić mocno wyczerpane limfocyty T samoistnym zwiększeniem TCF1 prawdopodobnie nie zadziałają. Zamiast tego skuteczne terapie mogą wymagać kombinacji kilku czynników lub skupienia się na ochronie i ekspansji puli komórek macierzystych, zanim komórki staną się zbyt wyczerpane, by je uratować.
Cytowanie: de Menezes, M.N., Chen, A.X.Y., Kulkarni, N. et al. High efficiency CRISPR knock-in demonstrates that TCF1 is insufficient to reverse T cell exhaustion. Nat Commun 17, 2857 (2026). https://doi.org/10.1038/s41467-026-69671-y
Słowa kluczowe: Wyczerpanie limfocytów T, TCF1, wprowadzanie przez CRISPR, immunoterapia przeciwnowotworowa, limfocyty T o cechach macierzystych