Clear Sky Science · it
Un’efficiente integrazione CRISPR ad alta efficienza dimostra che TCF1 non è sufficiente per invertire l’esaurimento delle cellule T
Perché le cellule immunitarie esauste sono importanti
Il nostro sistema immunitario si affida alle cellule T citotossiche per individuare e distruggere cellule infettate da virus e cellule tumorali. Ma quando queste minacce persistono per mesi, le cellule T possono diventare “esauste”, perdendo gran parte della loro efficacia. Un sottogruppo speciale di queste cellule si comporta più come cellule staminali, rinnovando continuamente la risposta e contribuendo all’efficacia delle moderne immunoterapie per il cancro. Questo studio pone una domanda apparentemente semplice ma di grande rilevanza clinica: possiamo riportare le cellule T logore a questo stato giovanile e simile alle staminali riattivando un singolo gene di controllo maestro chiamato TCF1?
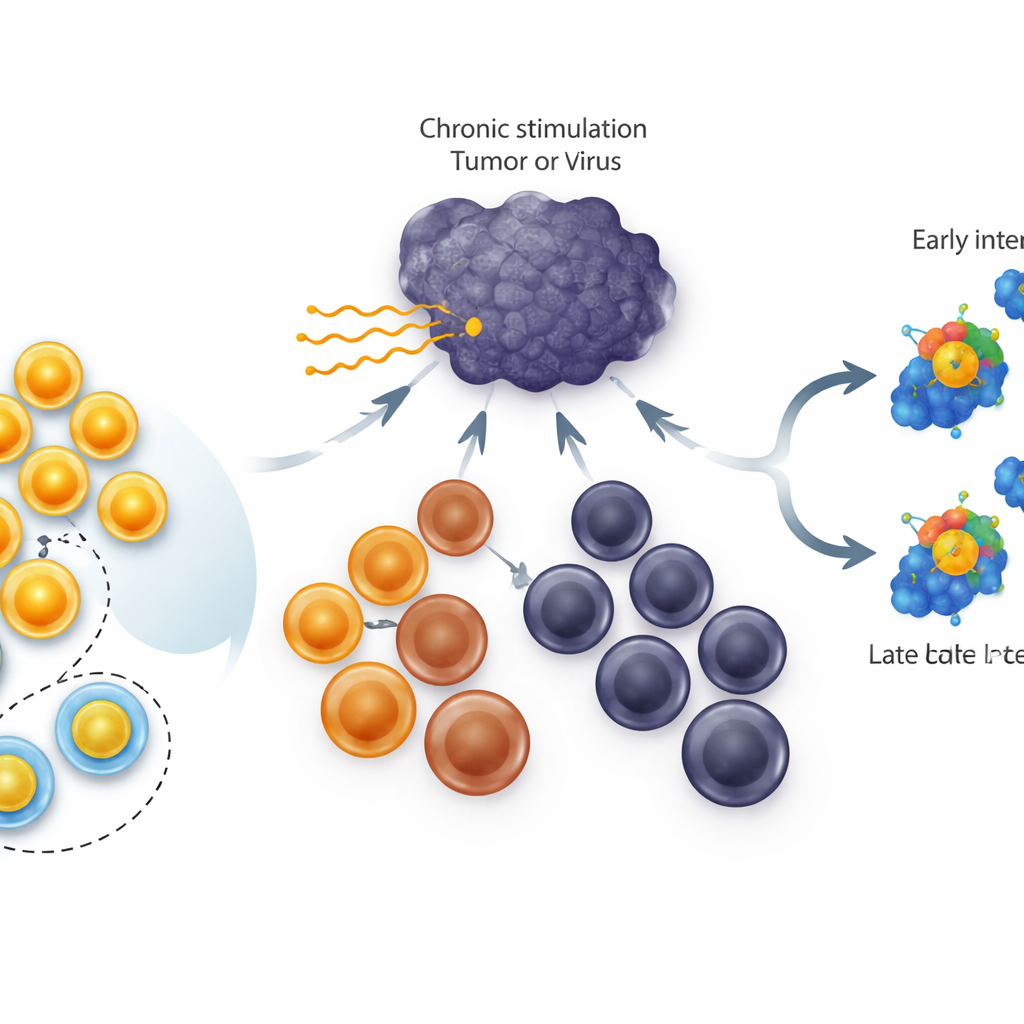
Diverse tipologie di cellule T esauste
Nelle infezioni croniche e nei tumori, le cellule T citotossiche non si spengono semplicemente; attraversano una scala di stati. In cima ci sono le cellule di tipo staminale che si dividono bene e possono generare nuovi effettori. Nel mezzo si trovano le cellule “intermedie” che contribuiscono ancora al controllo della malattia, e in fondo stanno le cellule terminalmente esauste che hanno poca flessibilità residua. Il gene TCF1 è altamente attivo nel gruppo di tipo staminale ed è noto per essere essenziale alla loro formazione e sopravvivenza. Studi precedenti hanno mostrato che aumentare costantemente TCF1 in tutte le cellule esauste aumenta la dimensione del pool di cellule di tipo staminale. Ciò che non era chiaro è se TCF1 possa effettivamente riportare cellule esauste in stadi più avanzati su per la scala fino a quel tipo staminale.
Costruire un kit di editing genico preciso nei topi
Per affrontare la domanda, i ricercatori hanno innanzitutto avuto bisogno di un metodo molto efficiente per inserire nuovo DNA nelle cellule T di topo senza alterare il loro comportamento naturale in vivo. Hanno ottimizzato una forma di riparazione guidata dall’omologia (homology-directed repair) con CRISPR che utilizza un modello virale AAV6 per “knock-in” di nuovo materiale genetico in posizioni precise del genoma. Attivando con cura le cellule T, consegnando i componenti CRISPR, lasciando brevemente le cellule in riposo in laboratorio e poi trasferendole nei topi, hanno ottenuto tassi di knock-in del 40–80%—livelli comparabili o superiori all’overespressione virale tradizionale. Hanno inoltre dimostrato come inserire geni senza interrompere geni ospiti importanti e come mirare indirizzi genetici specifici in modo che un nuovo gene si attivi solo in particolari sottopopolazioni di cellule T.
Attivare TCF1 precocemente versus tardivamente
Il cuore dello studio confronta due strategie per attivare TCF1. In una, il team ha inserito TCF1 in una posizione attiva in tutte le cellule T, così che TCF1 fosse elevato fin dall’inizio della risposta. Nell’altra, hanno inserito TCF1 nel gene Cx3cr1, che diventa attivo solo quando le cellule di tipo staminale maturano nello stato di esaurimento intermedio. Questo secondo disegno funziona come un interruttore condizionale, accendendo TCF1 solo dopo che le cellule hanno già iniziato il percorso verso l’esaurimento. Quando le cellule T modificate sono state testate in un modello ben consolidato di infezione virale cronica, l’espressione costante di TCF1 ha chiaramente ampliato il pool di cellule di tipo staminale. Al contrario, accendere TCF1 solo nelle cellule intermedie non ha aumentato il numero di cellule di tipo staminale, anche se quelle cellule intermedie producevano tanto o più TCF1 per cellula rispetto all’impostazione ad espressione costante.
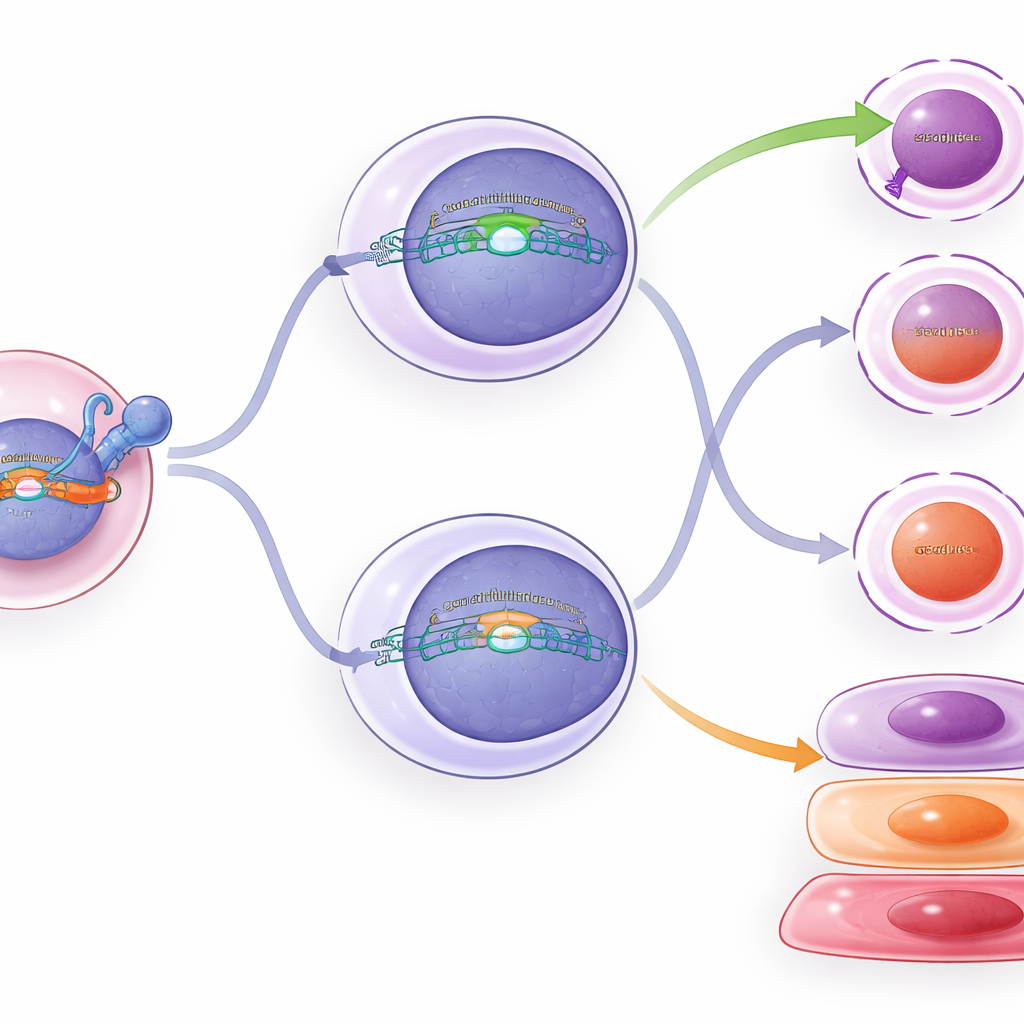
Cosa accade all’interno delle cellule riprogrammate
Per andare oltre il semplice conteggio cellulare, il gruppo ha profilato l’attività genica e la cromatina (il confezionamento del DNA che controlla quali geni possono attivarsi) in migliaia di singole cellule T. Le cellule con TCF1 costante mostravano più cluster di tipo staminale e cellule effettori precoci, coerentemente con l’idea che TCF1 rallenti la progressione verso l’esaurimento profondo. Il TCF1 condizionale nelle cellule intermedie ha causato solo spostamenti sottili: alcuni pattern genici e caratteristiche cromatiniche si sono orientati verso quelli delle cellule di tipo staminale, e i marcatori di esaurimento sono leggermente diminuiti. La citometria a flusso ha confermato questi cambiamenti lievi—le cellule intermedie con TCF1 aggiuntivo avevano un po’ meno di certe proteine associate alla citotossicità e all’esaurimento, e un po’ di più un marcatore associato alle cellule di tipo staminale—ma non sono ritornate completamente alla loro identità giovanile.
Perché un singolo gene non può riportare indietro il tempo
Per un non specialista, il messaggio chiave è che una volta che le cellule T hanno percorso sufficientemente la strada dell’esaurimento, la sola riattivazione di TCF1 non è sufficiente a riportarle a uno stato giovanile e simile alle staminali. TCF1 costante aiuta a preservare le cellule di tipo staminale se è presente fin dall’inizio, agendo efficacemente da rallentatore dell’invecchiamento, ma non può annullare l’esaurimento a posteriori. Questo ha implicazioni importanti per l’immunoterapia del cancro: le strategie che cercano di ringiovanire cellule T fortemente esauste potenziando solo TCF1 probabilmente non avranno successo. Le terapie efficaci potrebbero invece dover combinare più fattori o concentrarsi sulla protezione e l’espansione del pool di cellule di tipo staminale prima che le cellule diventino troppo esauste per essere recuperate.
Citazione: de Menezes, M.N., Chen, A.X.Y., Kulkarni, N. et al. High efficiency CRISPR knock-in demonstrates that TCF1 is insufficient to reverse T cell exhaustion. Nat Commun 17, 2857 (2026). https://doi.org/10.1038/s41467-026-69671-y
Parole chiave: Esaurimento delle cellule T, TCF1, Integrazione CRISPR, Immunoterapia contro il cancro, Cellule T di tipo staminale