Clear Sky Science · nl
Hoogrendement CRISPR knock-in toont aan dat TCF1 onvoldoende is om T-celuitputting te keren
Waarom uitgeputte immuuncellen ertoe doen
Ons immuunsysteem vertrouwt op cytotoxische T-cellen om met virussen geïnfecteerde en kankercellen op te sporen en uit te schakelen. Wanneer deze dreigingen maandenlang aanhouden, kunnen T-cellen echter “uitgeput” raken en veel van hun effectiviteit verliezen. Een speciale subset van deze cellen gedraagt zich meer als stamcellen: ze vernieuwen de respons continu en helpen moderne kankerimmunotherapieën functioneren. Deze studie stelt een schijnbaar eenvoudige maar behandelingskritische vraag: kunnen we uitgeputte T-cellen terugduwen naar die jeugdige, stam-achtige toestand door één mestergene, TCF1, aan te zetten?
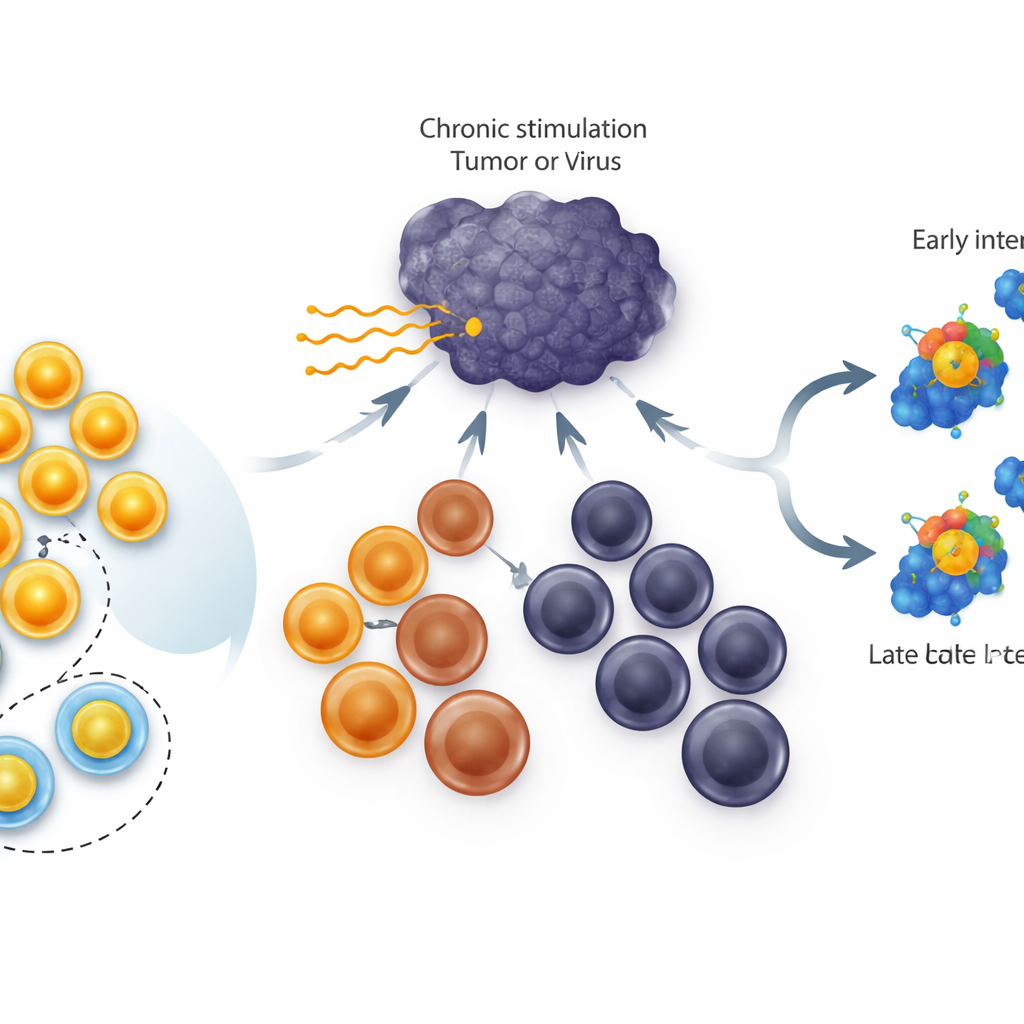
Verschillende typen uitgeputte T-cellen
Bij chronische infecties en tumoren schakelen cytotoxische T-cellen niet simpelweg uit; ze doorlopen een reeks toestanden. Bovenaan bevinden zich stam-achtige cellen die goed delen en nieuwe strijders kunnen voortbrengen. In het midden zitten “intermediaire” cellen die nog bijdragen aan ziektecontrole, en onderaan bevinden zich terminaal uitgeputte cellen met weinig veerkracht meer. Het gen TCF1 is sterk actief in de stam-achtige groep en is essentieel voor hun vorming en overleving. Eerder werk toonde aan dat het constant verhogen van TCF1 in alle uitgeputte cellen de omvang van de stam-achtige pool vergroot. Wat onduidelijk bleef, is of TCF1 gevorderde, meer uitgeputte cellen daadwerkelijk weer omhoog kan rewinden naar die stam-achtige staat.
Het bouwen van een precieze genbewerkingsset in muizen
Om dit aan te pakken, moesten de onderzoekers eerst een zeer efficiënte manier vinden om nieuw DNA in muizent-cellen in te voegen zonder hun natuurlijk gedrag in het lichaam te verstoren. Ze optimaliseerden een homologie-gemedieerde reparatievorm van CRISPR-bewerking die een AAV6-virus als sjabloon gebruikt om nieuwe genetische lading op exacte locaties in het genoom te ‘knock-innen’. Door T-cellen zorgvuldig te activeren, CRISPR-componenten af te leveren, de cellen kort in het lab te laten rusten en ze vervolgens in muizen te transfereren, bereikten ze knock-in-percentages van 40–80 procent — niveaus vergelijkbaar met of beter dan traditionele virale overexpressie. Ze toonden ook aan hoe genen in te voegen zonder belangrijke gastheergenes te breken, en hoe specifieke genetische adressen te targeten zodat een nieuw gen alleen in bepaalde T-celsubsets wordt aangezet.
TCF1 vroeg versus laat aanzetten
Het hart van de studie vergelijkt twee strategieën om TCF1 aan te zetten. In de ene plaatsten de onderzoekers TCF1 op een locatie die in alle T-cellen actief is, zodat TCF1 vanaf het begin van de respons hoog was. In de andere plaatsten ze TCF1 in het Cx3cr1-gen, dat pas actief wordt wanneer stam-achtige cellen rijpen naar de intermediaire uitgeputte toestand. Dit tweede ontwerp werkt als een conditionele schakelaar en zet TCF1 alleen aan nadat de cellen al verder op het uitputtingspad zijn gekomen. In een goed vastgesteld model van chronische virale infectie vergrootte constante TCF1-expressie duidelijk de stam-achtige pool. Daarentegen leidde TCF1-aanzetting alleen in intermediaire cellen niet tot meer stam-achtige cellen, ook al produceerden die intermediaire cellen evenveel of meer TCF1 per cel dan in het constante-expressie ontwerp.
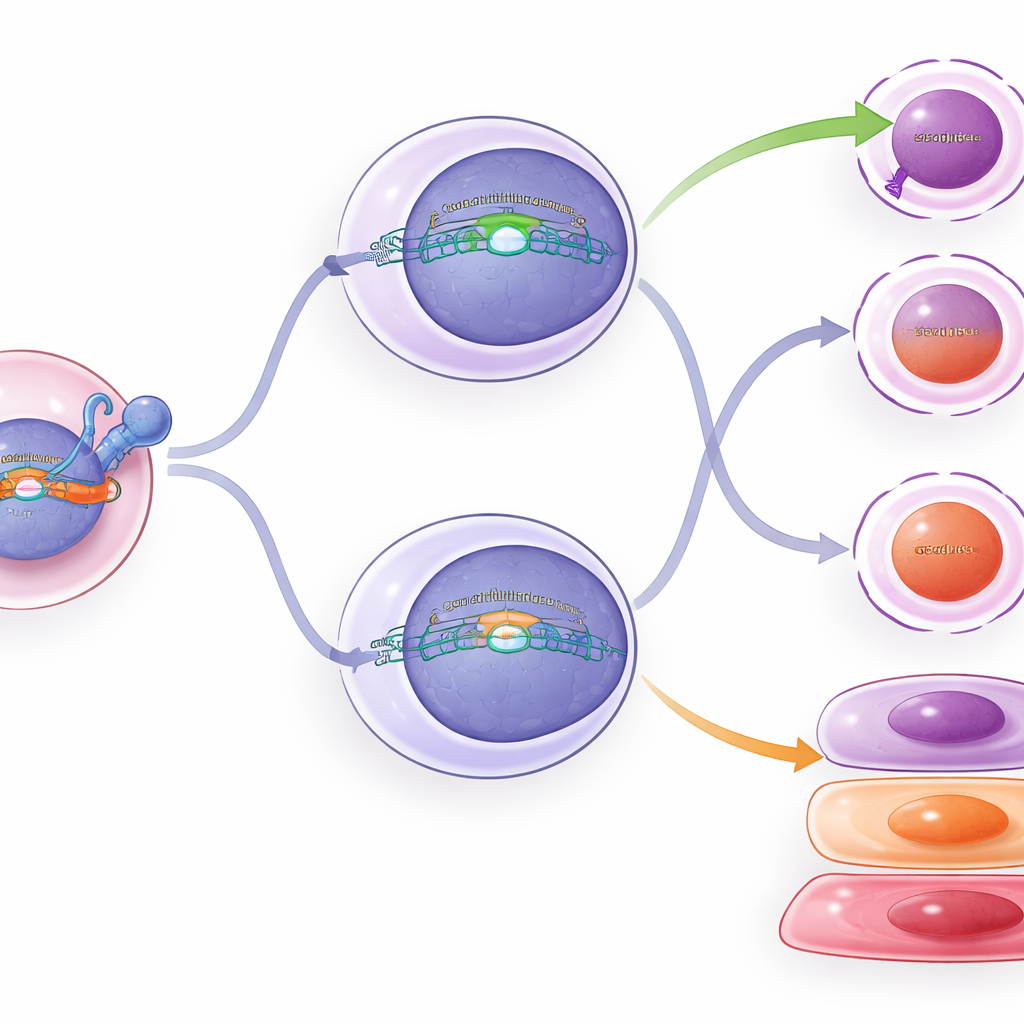
Wat er binnen in de herbedrade cellen gebeurt
Om verder te kijken dan eenvoudige celcounts profyleerden de onderzoekers genactiviteit en chromatine (de DNA-verpakking die bepaalt welke genen aan kunnen) in duizenden individuele T-cellen. Cellen met constante TCF1 toonden meer stam-achtige clusters en vroege effector-achtige cellen, wat consistent is met het idee dat TCF1 het voortschrijden naar diepe uitputting vertraagt. Conditionele TCF1 in intermediaire cellen veroorzaakte slechts subtiele verschuivingen: sommige genpatronen en chromatinekenmerken bewogen enigszins richting die van stam-achtige cellen, en merkers van uitputting daalden iets. Flowcytometrie bevestigde deze milde veranderingen — intermediaire cellen met extra TCF1 hadden iets minder van bepaalde cytotoxische en uitputtingsproteïnen, en iets meer van een merker geassocieerd met stam-achtige cellen — maar ze keerden niet volledig in identiteit terug.
Waarom één gen de klok niet terug kan draaien
Voor niet-specialisten is de kernboodschap dat zodra T-cellen ver genoeg op het uitputtingspad zijn geraakt, het eenvoudig reactiveren van TCF1 niet genoeg is om ze terug te sturen naar een jeugdige, stam-achtige staat. Constante TCF1 helpt stam-achtige cellen te behouden als het van meet af aan aanwezig is en vertraagt als het ware veroudering, maar het kan uitputting achteraf niet ongedaan maken. Dit heeft belangrijke implicaties voor kankerimmunotherapie: strategieën die proberen zwaar uitgeputte T-cellen te verjongen door alleen TCF1 te verhogen zijn waarschijnlijk niet effectief. Succesvolle therapieën zullen waarschijnlijk meerdere factoren moeten combineren of zich richten op het beschermen en uitbreiden van de stam-achtige pool voordat cellen te uitgeput raken om gered te worden.
Bronvermelding: de Menezes, M.N., Chen, A.X.Y., Kulkarni, N. et al. High efficiency CRISPR knock-in demonstrates that TCF1 is insufficient to reverse T cell exhaustion. Nat Commun 17, 2857 (2026). https://doi.org/10.1038/s41467-026-69671-y
Trefwoorden: T-celuitputting, TCF1, CRISPR knock-in, kankerimmunotherapie, stam-achtige T-cellen