Clear Sky Science · ar
كفاءة عالية في إدخال CRISPR توضح أن TCF1 غير كافٍ لعكس استنزاف الخلايا التائية
لماذا تهم الخلايا المناعية المتعبة
يعتمد جهازنا المناعي على الخلايا التائية القاتلة لمطاردة الخلايا المصابة بالفيروسات والخلايا السرطانية. لكن عندما تستمر هذه التهديدات لشهور، قد تدخل الخلايا التائية في حالة «استنزاف» تفقد فيها الكثير من فعاليتها. شريحة خاصة من هذه الخلايا تتصرف أشبه بالخلايا الجذعية، فتعيد تجديد الاستجابة باستمرار وتساعد العلاجات المناعية الحديثة للسرطان على العمل. تطرح هذه الدراسة سؤالاً يبدو بسيطاً لكنه ذو عواقب علاجية كبيرة: هل يمكننا دفع الخلايا التائية المتعبة للعودة إلى هذه الحالة الشبابية الشبيهة بالجذور عن طريق تشغيل جين تحكم رئيسي واحد يُدعى TCF1؟
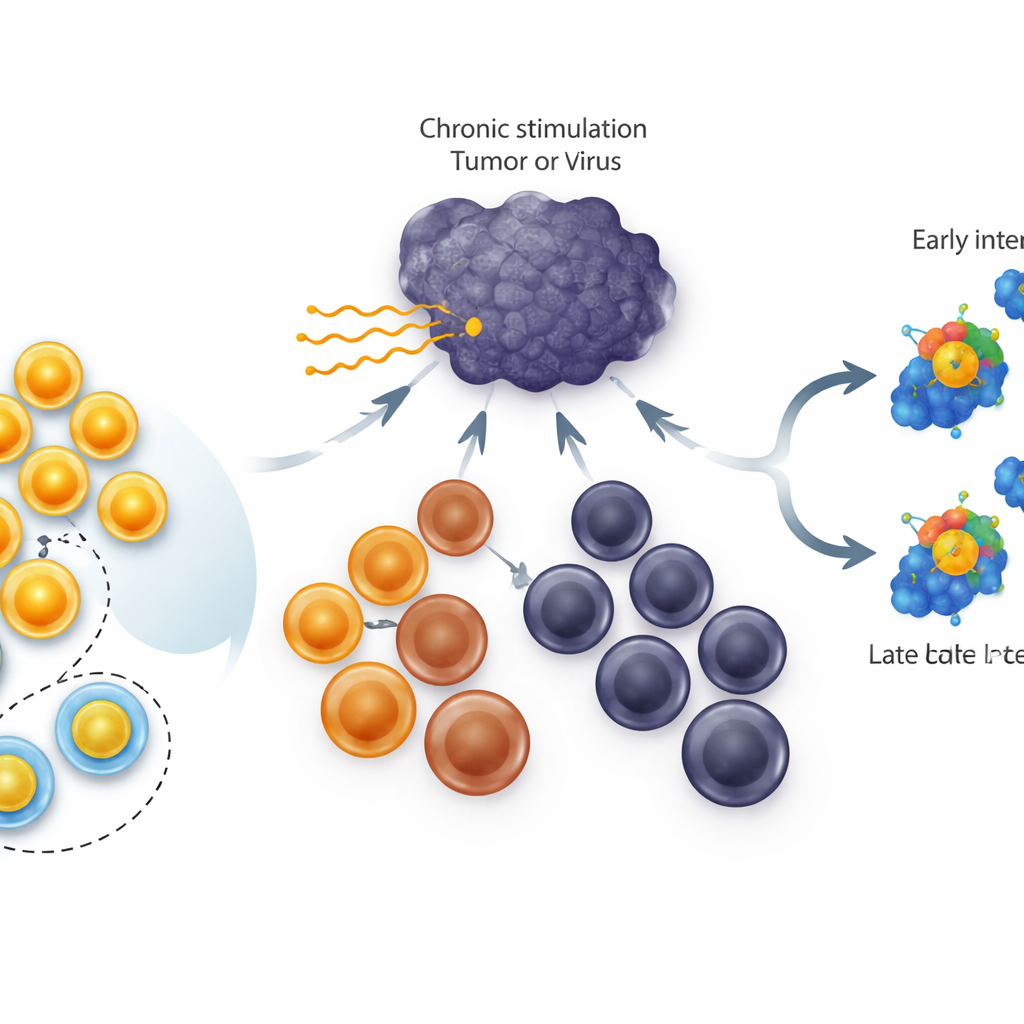
أشكال مختلفة من الخلايا التائية المتعبة
في العدوى المزمنة والأورام، لا تنطفئ الخلايا التائية القاتلة ببساطة؛ بل تمر بسلم من الحالات. في القمة توجد الخلايا الشبيهة بالجذور التي تنقسم جيداً ويمكنها إنتاج مقاتلين جدد. في الوسط توجد خلايا «متوسطة» لا تزال تساهم في السيطرة على المرض، وفي الأسفل توجد الخلايا المستنزفة نهائياً التي فقدت الكثير من المرونة. يكون جين TCF1 نشطاً بشدة في مجموعة الخلايا الشبيهة بالجذور وهو ضروري لتشكلها وبقائها. أظهرت أعمال سابقة أن تعزيز TCF1 باستمرار في جميع الخلايا المستنزفة يزيد حجم تجمع الخلايا الشبيهة بالجذور. وما لم يكن معروفاً هو ما إذا كان TCF1 قادرًا فعلاً على إعادة الخلايا الأكثر تقدماً في الاستنزاف إلى أعلى السلم لتصبح شبيهة بالجذور مرة أخرى.
بناء مجموعة أدوات تحرير جيني دقيقة في الفئران
لمعالجة هذا السؤال، احتاج الباحثون أولاً إلى طريقة فعالة للغاية لإدخال DNA جديد في خلايا تائية للفئران دون إزعاج سلوكها الطبيعي داخل الجسم. قاموا بتحسين شكل من أشكال إصلاح الحمض النووي المعتمد على التشابه (homology-directed repair) باستخدام CRISPR مع قالب فيروسي AAV6 لـ «إدخال» حمولة جينية جديدة في مواقع محددة في الجينوم. من خلال تنشيط الخلايا التائية بعناية، وتسليم مكونات CRISPR، وإراحة الخلايا لفترة وجيزة في المختبر، ثم نقلها إلى الفئران، تمكنوا من الوصول إلى معدلات إدخال تتراوح بين 40–80 بالمئة — مستويات مماثلة أو أفضل من التعبير الفيروسي التقليدي. كما أظهروا كيفية إدخال جينات دون كسر جينات مضيفة مهمة، وكيفية استهداف عناوين جينية محددة بحيث يتم تشغيل الجين الجديد فقط في مجموعات فرعية معينة من الخلايا التائية.
تشغيل TCF1 مبكراً مقابل متأخراً
يركز جوهر الدراسة على مقارنة استراتيجيتين لتشغيل TCF1. في الأولى، أدخل الفريق TCF1 في موقع نشط في جميع الخلايا التائية، بحيث كان مستوى TCF1 عالياً منذ بداية الاستجابة. في الثانية، أدخلوا TCF1 في جين Cx3cr1، الذي ينشط فقط عندما تنضج الخلايا الشبيهة بالجذور إلى حالة الاستنزاف الوسيط. يعمل التصميم الثاني كمفتاح شرطي، يشغّل TCF1 فقط بعد أن تكون الخلايا قد تقدمت في مسار الاستنزاف. عند اختبار الخلايا التائية المعدلة في نموذج عدوى فيروسية مزمنة راسخة، وسّع التعبير المستمر عن TCF1 بوضوح تجمع الخلايا الشبيهة بالجذور. بالمقابل، لم يزد تشغيل TCF1 فقط في الخلايا الوسيطة عدد الخلايا الشبيهة بالجذور، على الرغم من أن تلك الخلايا الوسيطة أنتجت قدراً من TCF1 لكل خلية يعادل أو يفوق ما كان في إعداد التعبير المستمر.
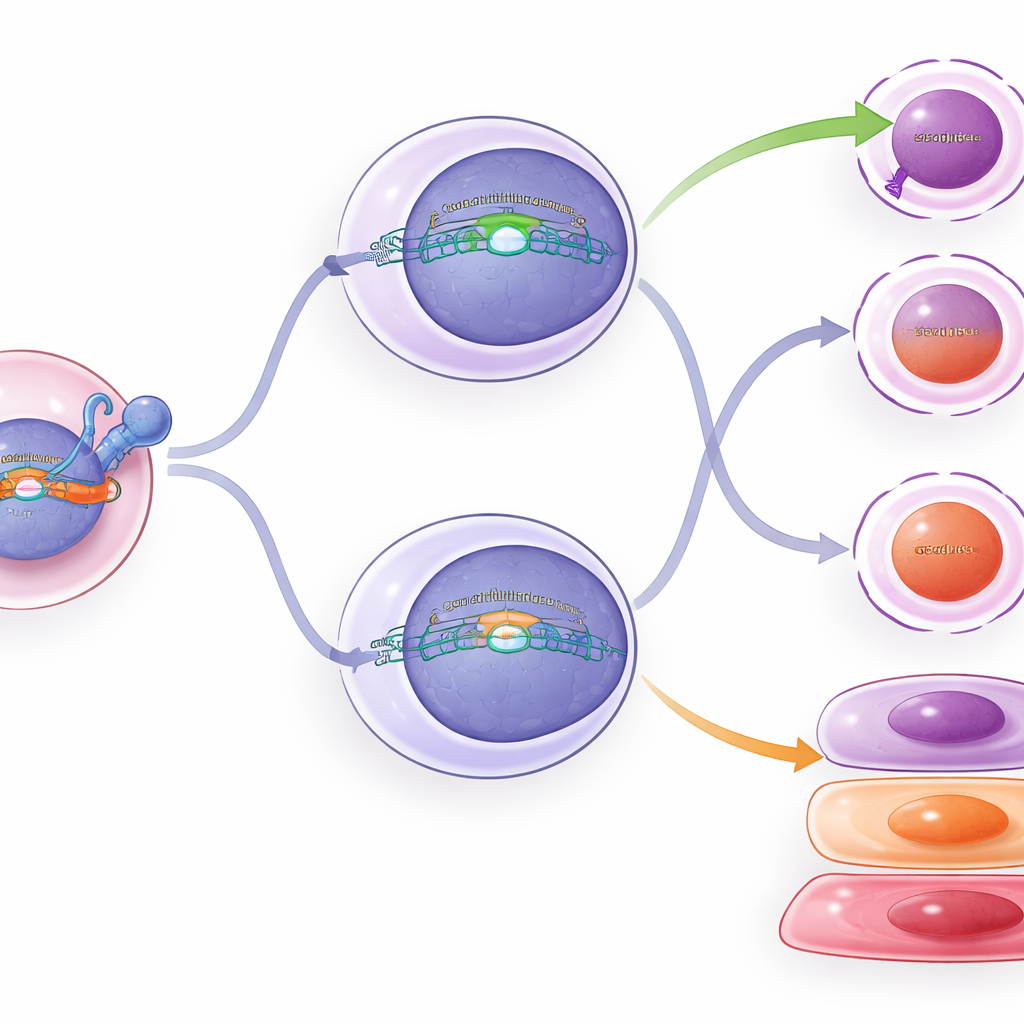
ماذا يحدث داخل الخلايا المعاد توصيلها
للنظر أبعد من عد الخلايا البسيط، قام الفريق بملف نشاط الجينات والكروماتين (تغليف الحمض النووي الذي يتحكم في أي الجينات يمكن أن تُشغّل) في آلاف الخلايا التائية المفردة. أظهرت الخلايا ذات التعبير المستمر لـ TCF1 تجمعات أكثر شبيهة بالجذور وخلايا تأثير مبكرة أكثر، بما يتوافق مع تباطؤ TCF1 في المسار نحو الاستنزاف العميق. أما TCF1 الشرطي في الخلايا الوسيطة فسبب تغيّرات طفيفة فقط: بعض أنماط الجينات وملامح الكروماتين انحرفت قليلاً باتجاه تلك الخاصة بالخلايا الشبيهة بالجذور، وانخفضت بعض علامات الاستنزاف بشكل طفيف. أكدت قياسات التدفق الخلوي هذه التغيّرات المعتدلة — فالخلايا الوسيطة التي أضيف إليها TCF1 أظهرت انخفاضاً طفيفاً في بعض بروتينات القتل والاستنزاف، وزيادة طفيفة في علامة مرتبطة بالخلايا الشبيهة بالجذور — لكنها لم تعد هويتها بالكامل.
لماذا لا يمكن لجين واحد أن يعيد عقارب الساعة للخلف
للغير مختصين، الرسالة الأساسية هي أنه بمجرد أن تسير الخلايا التائية بعيداً في طريق الاستنزاف، فإن مجرد إعادة تنشيط TCF1 ليس كافياً لإعادتها إلى حالة شبابية شبيهة بالجذور. يساعد وجود TCF1 المستمر في الحفاظ على الخلايا الشبيهة بالجذور إذا كان موجوداً منذ المراحل المبكرة، أي إنه يبطئ «الشيخوخة»، لكنه لا يستطيع إلغاء الاستنزاف بعد حدوثه. لهذا فلتأثيرات مهمة على العلاج المناعي للسرطان: الاستراتيجيات التي تحاول تجديد الخلايا التائية المستنزفة بشدة عن طريق تعزيز TCF1 وحده من غير المرجح أن تنجح. بدلاً من ذلك، قد تحتاج العلاجات الفعّالة إلى الجمع بين عدة عوامل أو التركيز على حماية وتوسيع تجمع الخلايا الشبيهة بالجذور قبل أن تصبح الخلايا مفرطة الاستنزاف بحيث لا يمكن إنقاذها.
الاستشهاد: de Menezes, M.N., Chen, A.X.Y., Kulkarni, N. et al. High efficiency CRISPR knock-in demonstrates that TCF1 is insufficient to reverse T cell exhaustion. Nat Commun 17, 2857 (2026). https://doi.org/10.1038/s41467-026-69671-y
الكلمات المفتاحية: استنزاف الخلايا التائية, TCF1, إدخال CRISPR, العلاج المناعي للسرطان, الخلايا التائية شبيهة بالجذور