Clear Sky Science · es
Eficiencia alta de knock-in por CRISPR demuestra que TCF1 es insuficiente para revertir la agotamiento de células T
Por qué importan las células inmunitarias cansadas
Nuestro sistema inmunitario depende de las células T citotóxicas para localizar y eliminar células infectadas por virus y células cancerosas. Pero cuando estas amenazas persisten durante meses, las células T pueden volverse “agotadas”, perdiendo gran parte de su capacidad de acción. Un subtipo especial de estas células se comporta más como células madre, renovando continuamente la respuesta y ayudando al funcionamiento de las inmunoterapias modernas contra el cáncer. Este estudio plantea una pregunta aparentemente simple con grandes implicaciones terapéuticas: ¿podemos empujar a las células T desgastadas de nuevo hacia este estado juvenil y con carácter de célula madre activando un único gen maestro llamado TCF1?
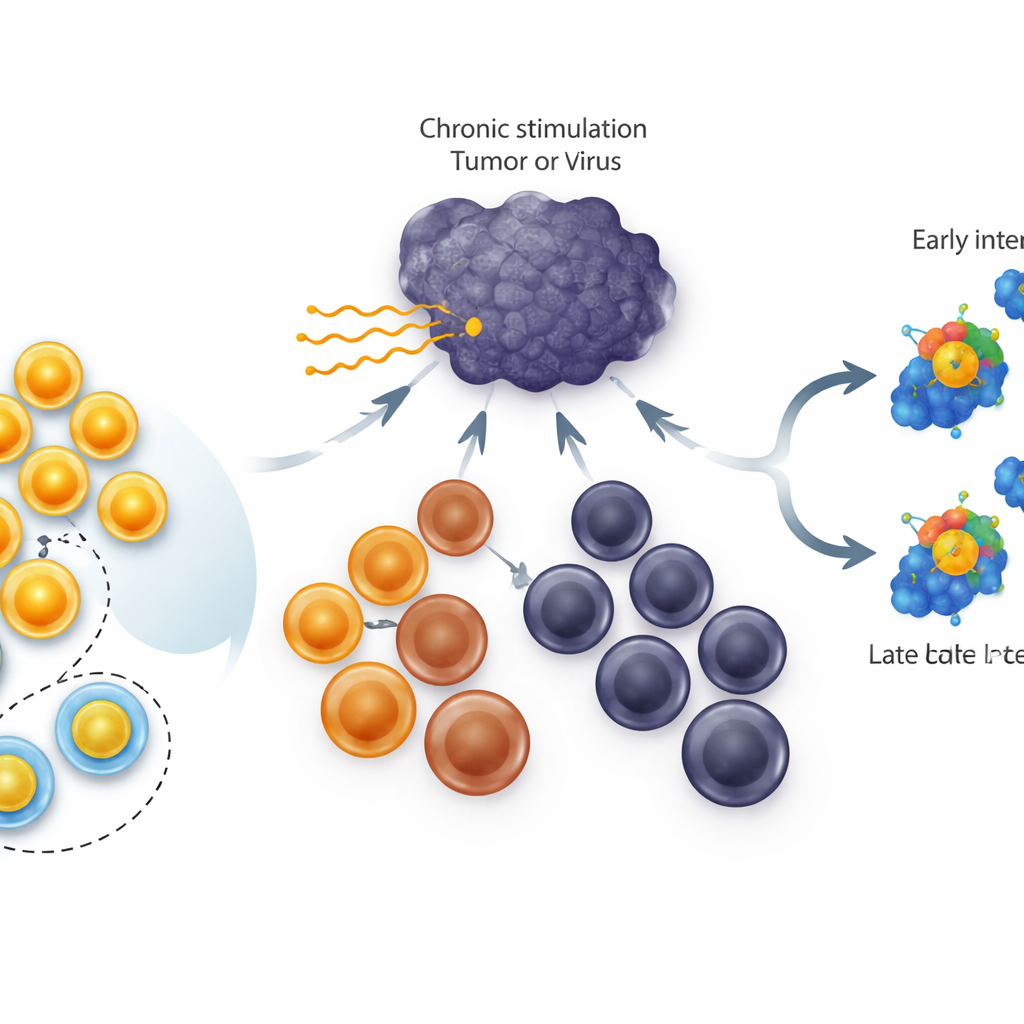
Diferentes versiones de células T agotadas
En infecciones crónicas y tumores, las células T citotóxicas no se apagan de golpe; atraviesan una escalera de estados. En la cima están las células con carácter de célula madre que se dividen bien y pueden generar nuevos combatientes. En el medio están las células “intermedias” que aún contribuyen al control de la enfermedad, y en la base están las células terminalmente agotadas que tienen poca flexibilidad restante. El gen TCF1 está muy activo en el grupo con carácter de célula madre y es conocido por ser esencial para su formación y supervivencia. Trabajos previos mostraron que impulsar constantemente TCF1 en todas las células agotadas aumenta el tamaño de la reserva con carácter de célula madre. Lo que se desconocía era si TCF1 puede realmente retroceder a células agotadas más avanzadas hacia ese estado con carácter de célula madre.
Construir un kit de edición génica preciso en ratones
Para abordar esto, los investigadores primero necesitaron una forma altamente eficiente de insertar nuevo ADN en células T de ratón sin alterar su comportamiento natural dentro del organismo. Optimizaron una edición CRISPR basada en reparación dirigida por homología que usa una plantilla viral AAV6 para “knock-in” de nuevo material genético en lugares precisos del genoma. Activando cuidadosamente las células T, entregando los componentes de CRISPR, dejando las células en reposo brevemente en el laboratorio y luego transfiriéndolas a ratones, pudieron alcanzar tasas de knock-in del 40–80 por ciento —niveles comparables o superiores a la sobreexpresión viral tradicional. También demostraron cómo insertar genes sin romper genes huésped importantes y cómo dirigir direcciones genéticas específicas para que un gen nuevo se active solo en subconjuntos determinados de células T.
Encender TCF1 temprano frente a tarde
El núcleo del estudio compara dos estrategias para activar TCF1. En una, el equipo insertó TCF1 en una ubicación que está activa en todas las células T, por lo que TCF1 era alto desde el inicio de la respuesta. En la otra, insertaron TCF1 en el gen Cx3cr1, que se activa solo cuando las células con carácter de célula madre maduran hacia el estado de agotamiento intermedio. Este segundo diseño actúa como un interruptor condicional, encendiendo TCF1 solo después de que las células ya han avanzado por la vía de agotamiento. Cuando las células T modificadas se probaron en un modelo establecido de infección viral crónica, la expresión constante de TCF1 amplió claramente la reserva con carácter de célula madre. En contraste, activar TCF1 solo en células intermedias no aumentó el número de células con carácter de célula madre, aunque esas células intermedias producían tanto o más TCF1 por célula que en el arreglo de expresión constante.
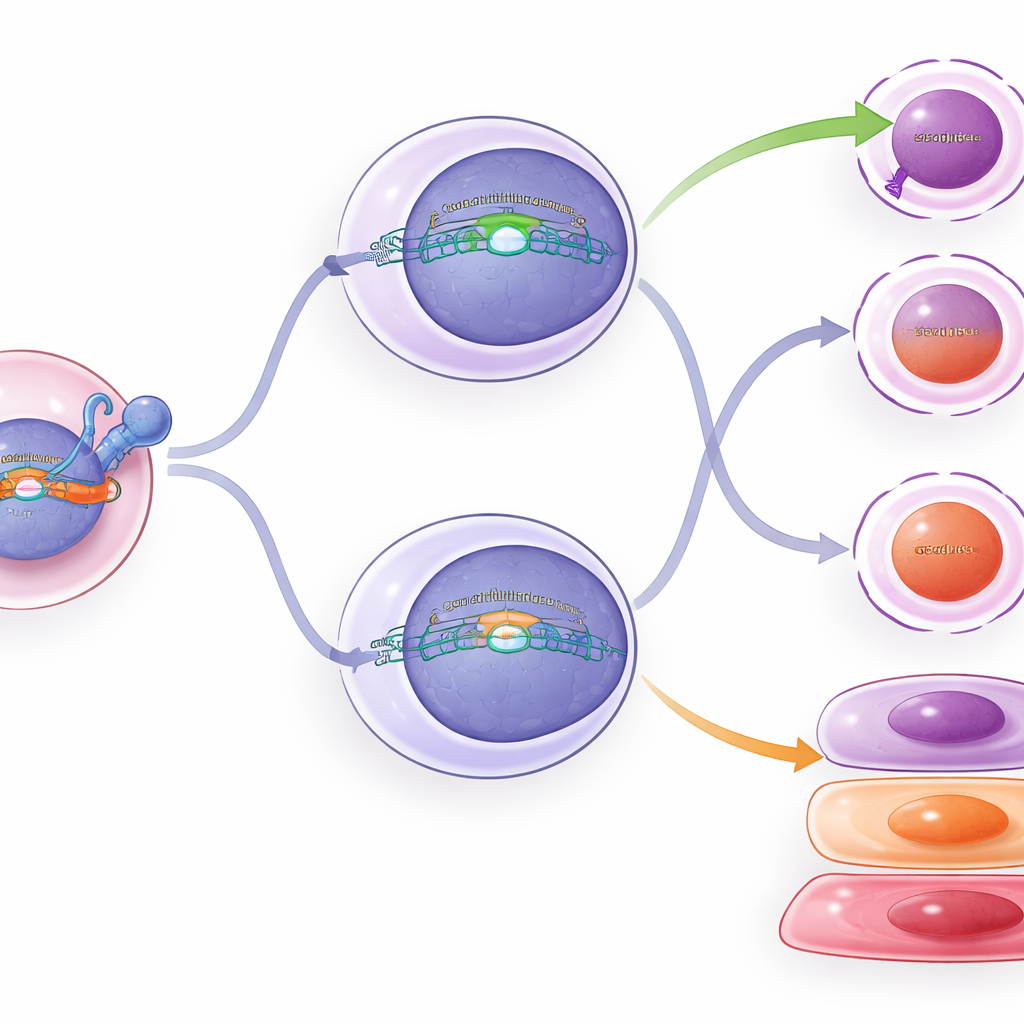
Qué ocurre dentro de las células reconfiguradas
Para ver más allá de los simples recuentos celulares, el equipo perfiló la actividad génica y la cromatina (el empaquetamiento del ADN que controla qué genes pueden activarse) en miles de células T individuales. Las células con TCF1 constante mostraron más agrupaciones con carácter de célula madre y células con rasgos de efector temprano, consistente con que TCF1 ralentiza la progresión hacia el agotamiento profundo. El TCF1 condicional en células intermedias causó solo cambios sutiles: algunos patrones génicos y características de la cromatina se desplazaron ligeramente hacia los de las células con carácter de célula madre, y los marcadores de agotamiento disminuyeron levemente. Citometría de flujo confirmó estos cambios leves: las células intermedias con TCF1 añadido tenían algo menos de ciertas proteínas de citotoxicidad y agotamiento, y algo más de un marcador asociado a las células con carácter de célula madre, pero no recuperaron completamente su identidad.
Por qué un solo gen no puede retroceder el reloj
Para un lector no especialista, el mensaje clave es que una vez que las células T han avanzado lo suficiente por la senda del agotamiento, simplemente reactivar TCF1 no basta para devolverlas a un estado juvenil y con carácter de célula madre. TCF1 constante ayuda a preservar las células con carácter de célula madre si está presente desde etapas tempranas, ralentizando efectivamente el envejecimiento, pero no puede deshacer el agotamiento una vez establecido. Esto tiene implicaciones importantes para la inmunoterapia contra el cáncer: las estrategias que intenten rejuvenecer células T fuertemente agotadas mediante el aumento solo de TCF1 probablemente no funcionarán. En su lugar, las terapias eficaces podrían necesitar combinar varios factores o centrarse en proteger y expandir la reserva con carácter de célula madre antes de que las células se agoten demasiado para ser rescatadas.
Cita: de Menezes, M.N., Chen, A.X.Y., Kulkarni, N. et al. High efficiency CRISPR knock-in demonstrates that TCF1 is insufficient to reverse T cell exhaustion. Nat Commun 17, 2857 (2026). https://doi.org/10.1038/s41467-026-69671-y
Palabras clave: Agotamiento de células T, TCF1, Knock-in por CRISPR, Inmunoterapia contra el cáncer, Células T con carácter de célula madre