Clear Sky Science · tr
Yüksek verimli CRISPR knok‑in, TCF1’in T hücresi yorulmasını geri döndürmek için yeterli olmadığını gösteriyor
Neden Yorgun İmmün Hücreler Önemli?
Bağışıklık sistemimiz, virüs bulaşmış ve kanserli hücreleri avlayan öldürücü T hücrelerine dayanır. Ancak bu tehditler aylarca devam edince, T hücreleri “tükenmiş” hale gelerek etkilerinin büyük kısmını kaybedebilir. Bu hücrelerin özel bir alt grubu kök hücre benzeri davranır; yanıtı sürekli yeniler ve modern kanser immünoterapilerinin etkinliğine katkıda bulunur. Bu çalışma, tedavi açısından büyük çıkarımları olan yanıltıcı derecede basit bir soruyu soruyor: tek bir ana kontrol geni olan TCF1’i açarak yıpranmış T hücrelerini bu genç, kök‑benzeri duruma geri döndürebilir miyiz?
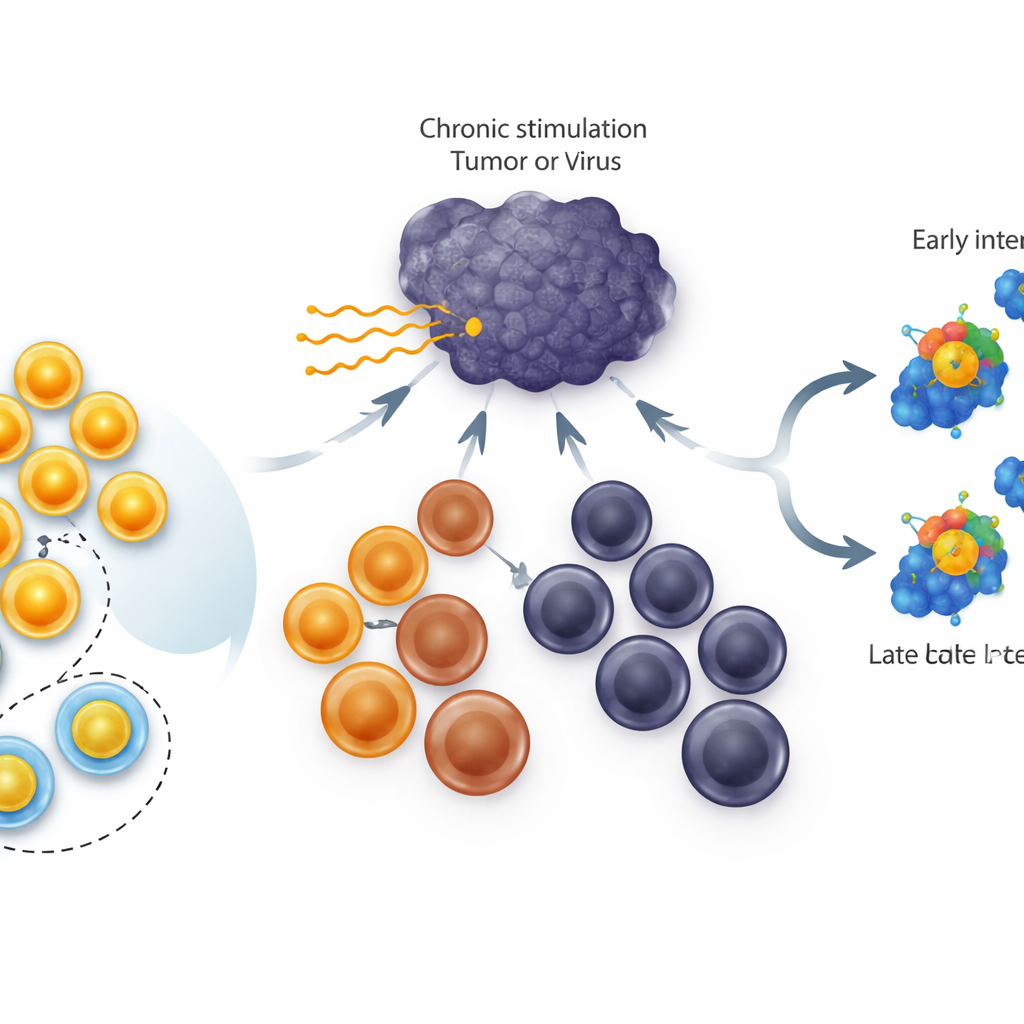
Yorgun T Hücrelerinin Farklı Türleri
Kronik enfeksiyonlar ve tümörlerde öldürücü T hücreleri sadece kapanmaz; bir dizi durumdan geçerler. En üstte iyi bölünen ve yeni savaşçılar üretebilen kök‑benzeri hücreler vardır. Ortada hastalığın kontrolüne hâlâ katkıda bulunan “ara” hücreler bulunur ve en altta esnekliği kalmamış terminal derecede tükenmiş hücreler yer alır. TCF1 geni kök‑benzeri grupta yüksek düzeyde aktiftir ve bu hücrelerin oluşumu ile hayatta kalması için gereklidir. Önceki çalışmalar, tükenmiş tüm hücrelerde TCF1’i sürekli artırmanın kök‑benzeri havuzun büyümesini sağladığını göstermişti. Bilinmeyen ise, TCF1’in daha ileri, tükenmiş hücreleri gerçekten de merdiven yukarı, kök‑benzeri duruma geri çevirebilip çeviremeyeceğiydi.
Mısta Hassas Bir Gen Düzenleme Araç Kiti Kurmak
Bunu ele almak için araştırmacıların önce fare T hücrelerine yeni DNA’yı vücut içindeki doğal davranışlarını bozmayacak şekilde yüksek verimle sokmanın bir yoluna ihtiyaçları vardı. Genomdaki kesin noktalara yeni genetik yükleri “knok‑in” yapmak için AAV6 viral şablonu kullanan bir homolog yeniden onarım (homology‑directed repair) biçiminde CRISPR düzenlemesini optimize ettiler. T hücrelerini dikkatle aktive edip CRISPR bileşenlerini verip hücreleri laboratuvarda kısa süre dinlendirdikten sonra farelere aktarımla, knok‑in oranlarını yüzde 40–80 aralığına çıkarabildiler—bu oranlar geleneksel viral aşırı ifade yöntemleriyle karşılaştırılabilir veya daha iyi düzeyde. Ayrıca önemli konakçı genleri kırmadan gen sokmanın ve yeni bir genin yalnızca belirli T hücresi alt kümelerinde aktif olmasını sağlayacak hedefleme yapmanın yollarını gösterdiler.
TCF1’i Erken mi Yoksa Geç mi Açmak?
Çalışmanın özünü, TCF1’i açmak için iki stratejinin karşılaştırılması oluşturuyor. Birinde ekip, TCF1’i tüm T hücrelerinde aktif olan bir konuma yerleştirdi; böylece TCF1 yanıtın başından itibaren yüksekti. Diğerinde ise TCF1’i yalnızca kök‑benzeri hücreler ara tükenmişliğe ilerlediğinde aktif hale gelen Cx3cr1 genine yerleştirdiler. Bu ikinci tasarım, hücreler tükenme yolunda ilerledikten sonra TCF1’i ancak o zaman açan koşullu bir anahtar gibi davranıyor. Değiştirilmiş T hücreleri iyi kurulmuş bir kronik viral enfeksiyon modeli içinde test edildiğinde, sürekli TCF1 ifadesi kök‑benzeri havuzu belirgin şekilde genişletti. Buna karşılık, yalnızca ara hücrelerde TCF1’i açmak kök‑benzeri hücre sayısını artırmadı; oysa bu ara hücreler hücre başına sürekli ifadeye yakın veya daha fazla TCF1 üretmişlerdi.
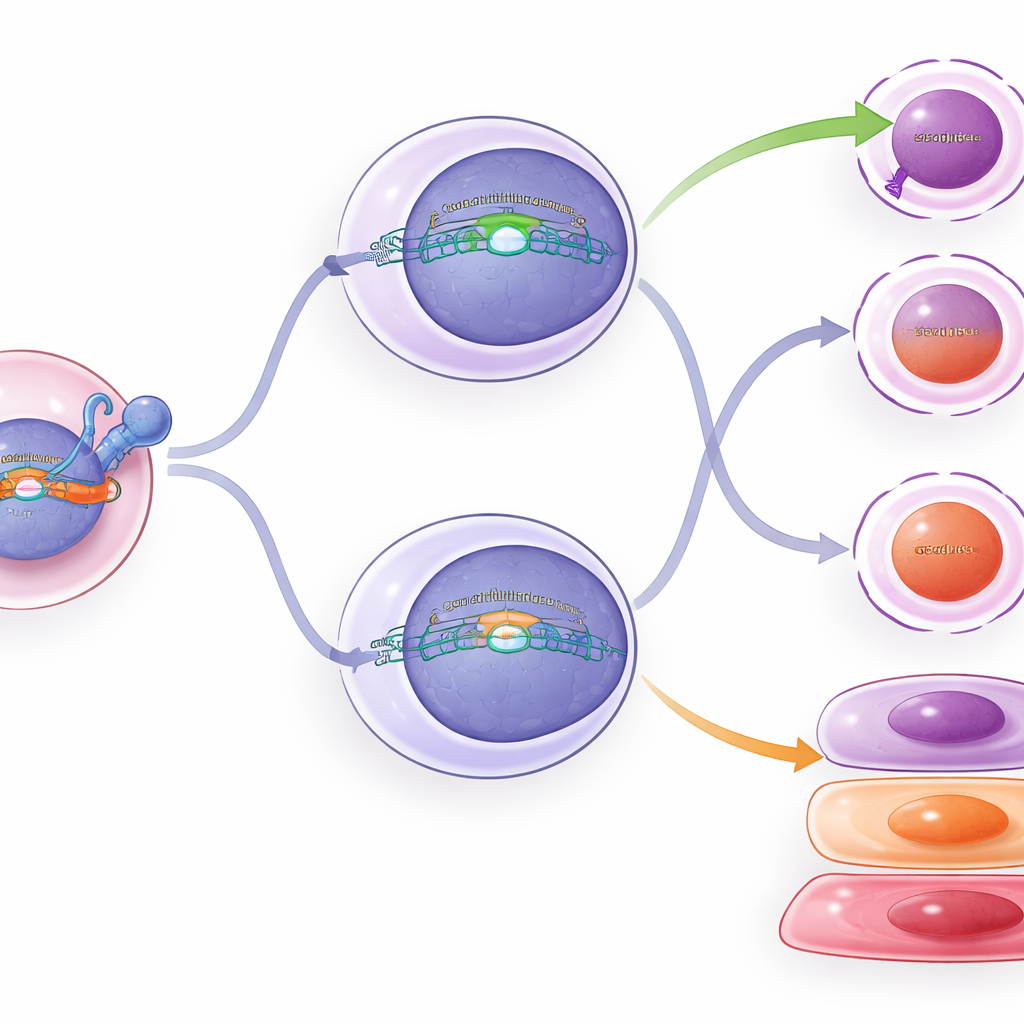
Yeniden Kabartılan Hücrelerin İçinde Neler Oluyor?
Basit hücre sayılarının ötesini görmek için ekip, binlerce tek T hücresinde gen etkinliğini ve kromatini (hangi genlerin açılabileceğini kontrol eden DNA paketlemesi) profillendirdi. Sürekli TCF1 taşıyan hücreler daha fazla kök‑benzeri küme ve erken efektör‑benzeri hücre gösterdi; bu, TCF1’in derin tükenmeye doğru ilerlemeyi yavaşlattığıyla tutarlı. Ara hücrelerde koşullu TCF1 yalnızca ince değişikliklere yol açtı: bazı gen desenleri ve kromatin özellikleri kök‑benzeri hücrelere doğru hafifçe kaydı ve tükenme belirteçleri bir miktar azaldı. Akış sitometrisi bu hafif değişiklikleri doğruladı—ek TCF1’e sahip ara hücrelerde belirli öldürücü ve tükenme proteinlerinin biraz düşük, kök‑benzeri hücrelerle ilişkilendirilen bir belirtecin ise biraz daha yüksek olduğu görüldü—ancak kimlikleri tamamen geri dönmedi.
Neden Tek Bir Gen Saati Geri Alamaz?
Uzman olmayan bir okuyucu için temel mesaj şudur: T hücreleri tükenme yolunda yeterince ilerlediklerinde, yalnızca TCF1’i yeniden etkinleştirmek onları genç, kök‑benzeri duruma geri göndermek için yeterli değildir. Sürekli TCF1, erken dönemde mevcutsa kök‑benzeri hücreleri korumaya yardımcı olur ve etkili bir şekilde yaşlanmayı yavaşlatır, ama olanı sonradan geri alamaz. Bu durum kanser immünoterapisi için önemli çıkarımlar taşır: yalnızca TCF1’i artırarak şiddetle tükenmiş T hücrelerini gençleştirmeye çalışan stratejiler muhtemelen başarısız olacaktır. Bunun yerine başarılı terapiler birkaç faktörü birleştirmeyi ya da hücreler fazla tükenmeden önce kök‑benzeri havuzun korunması ve genişletilmesine odaklanmayı gerektirebilir.
Atıf: de Menezes, M.N., Chen, A.X.Y., Kulkarni, N. et al. High efficiency CRISPR knock-in demonstrates that TCF1 is insufficient to reverse T cell exhaustion. Nat Commun 17, 2857 (2026). https://doi.org/10.1038/s41467-026-69671-y
Anahtar kelimeler: T hücresi yorulması, TCF1, CRISPR knok‑in, kanser immünoterapisi, kök‑benzeri T hücreleri