Clear Sky Science · ru
Высокоэффективный CRISPR-внедрение показывает, что TCF1 недостаточен для обратного восстановления истощённых T‑клеток
Почему истощённые иммунные клетки важны
Наша иммунная система опирается на киллерные T‑клетки, которые ищут и уничтожают инфицированные вирусами и раковые клетки. Но если угроза сохраняется месяцами, T‑клетки могут «истощаться», теряя большую часть своей эффективности. Особая подгруппа таких клеток ведёт себя больше как стволовые клетки: постоянно обновляет ответ и помогает современным методам иммунотерапии рака работать. В этом исследовании задаётся на первый взгляд простой, но важный для лечения вопрос: можно ли вернуть вымотанные T‑клетки в молодое, стволоподобное состояние, включив одиночный главный ген‑регулятор TCF1?
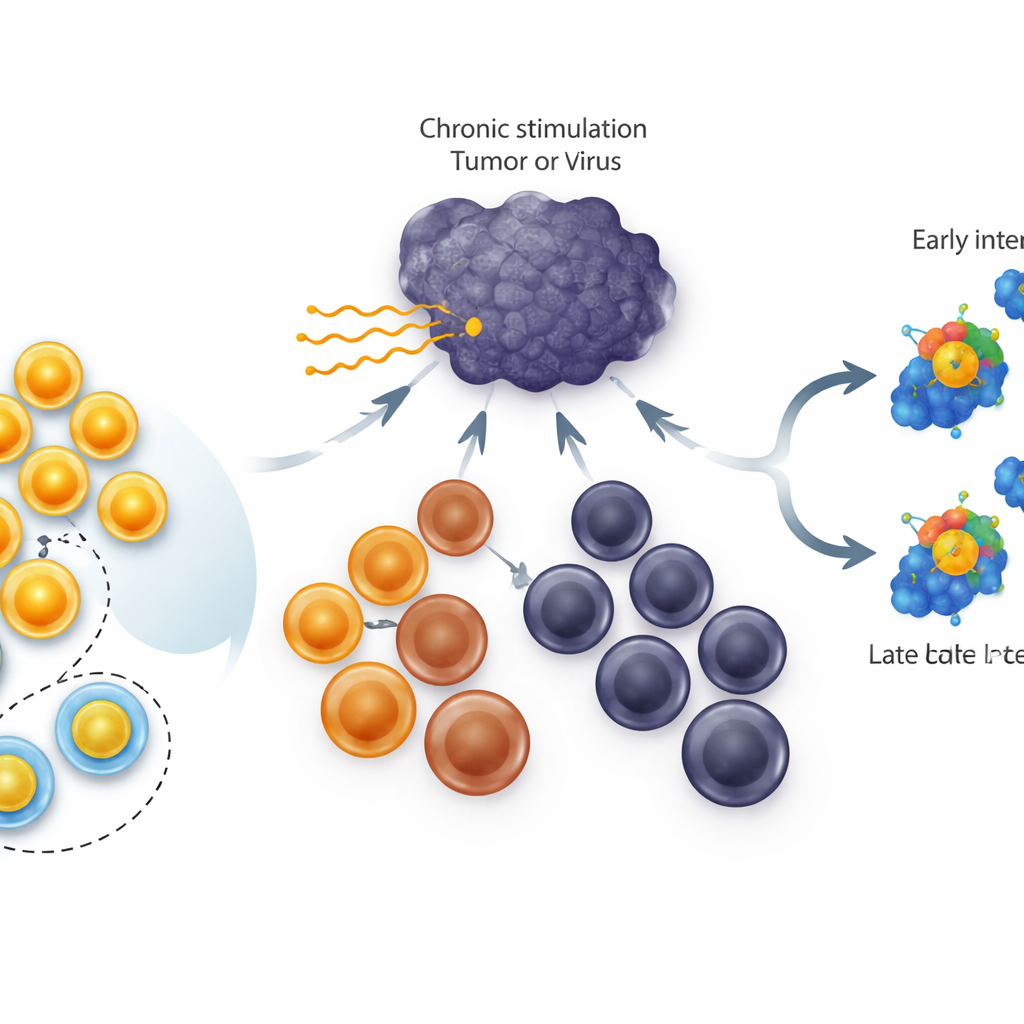
Разные варианты истощённых T‑клеток
При хронических инфекциях и опухолях киллерные T‑клетки не просто выключаются — они проходят через ступени состояний. На вершине находятся стволоподобные клетки, которые хорошо делятся и могут порождать новых бойцов. Посередине — «промежуточные» клетки, которые ещё вносят вклад в контроль заболевания, а внизу — терминально истощённые клетки, потерявшие гибкость. Ген TCF1 сильно активен в стволоподобной группе и необходим для их формирования и выживания. Предыдущие работы показали, что постоянное повышение TCF1 во всех истощённых клетках увеличивает размер пула стволоподобных клеток. Оставался вопрос: может ли TCF1 на самом деле вернуть более продвинутые, глубоко истощённые клетки обратно вверх по этой лестнице в стволоподобное состояние?
Создание точного инструмента генного редактирования в мышах
Чтобы ответить на этот вопрос, исследователям сначала потребовался высокоэффективный способ вставки новой ДНК в T‑клетки мыши, не нарушая их естественного поведения в организме. Они оптимизировали генно‑редактирование с репарацией по гомологии (homology‑directed repair), использующее AAV6‑вирион‑шаблон для «внедрения» нового генетического груза в точные места генома. Тщательно активируя T‑клетки, доставляя компоненты CRISPR, давая короткий отдых клеткам в лаборатории и затем пересаживая их в мышей, они достигли уровней внедрения 40–80% — сопоставимых с традиционным вирусным сверхэкспрессированием или превосходящих его. Они также показали, как вставлять гены, не нарушая важных генов хозяина, и как нацеливать конкретные генетические адреса, чтобы новый ген включался только в определённых подгруппах T‑клеток.
Включение TCF1 рано и поздно
Ядро исследования сравнивает две стратегии включения TCF1. В одной команде вставляли TCF1 в участок, активный во всех T‑клетках, так что TCF1 был высоким с самого начала ответа. В другой — вставляли TCF1 в ген Cx3cr1, который активируется только когда стволоподобные клетки переходят в промежуточное истощённое состояние. Этот второй дизайн действует как условный переключатель, включающий TCF1 только после того, как клетки уже продвинулись по пути истощения. В модели хорошо изученной хронической вирусной инфекции постоянная экспрессия TCF1 явно расширяла пул стволоподобных клеток. Напротив, включение TCF1 только в промежуточных клетках не увеличивало число стволоподобных клеток, хотя сами промежуточные клетки выражали не меньше, а иногда и больше TCF1 на клетку, чем при постоянной экспрессии.
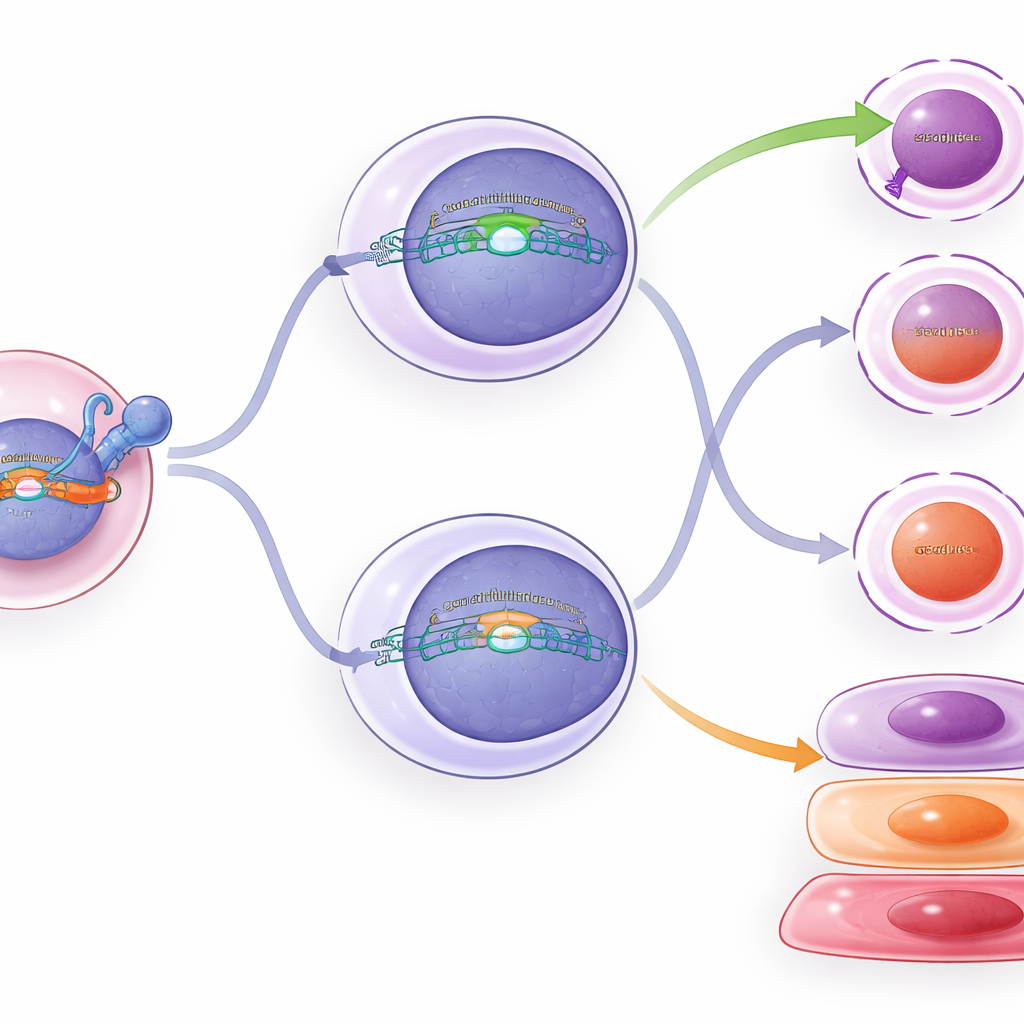
Что происходит внутри перенастроенных клеток
Чтобы заглянуть дальше простого подсчёта клеток, команда профилировала активность генов и состояние хроматина (упаковку ДНК, которая контролирует, какие гены могут включаться) в тысячах отдельных T‑клеток. Клетки с постоянной экспрессией TCF1 образовывали больше кластеров стволоподобных и ранних эффектороподобных клеток, что согласуется с замедлением TCF1 продвижения к глубокой усталости. Условный TCF1 в промежуточных клетках вызывал лишь тонкие сдвиги: некоторые паттерны экспрессии генов и черты хроматина смещались в сторону стволоподобных клеток, а маркеры истощения немного снижались. Проточная цитометрия подтвердила эти мягкие изменения — промежуточные клетки с добавленным TCF1 имели немного меньше некоторых белков, связанных с киллингом и истощением, и немного больше маркера, связанного со стволоподобностью, — но они не полностью вернули свою идентичность.
Почему один ген не может повернуть время вспять
Для неспециалиста главный вывод таков: как только T‑клетки прошли достаточно далеко по дороге истощения, простое реактивирование TCF1 недостаточно, чтобы вернуть их в молодое стволоподобное состояние. Постоянный TCF1 помогает сохранять стволоподобные клетки, если он присутствует с раннего этапа, фактически замедляя «старение», но он не способен обратить истощение вспять после того, как оно наступило. Это имеет важные последствия для иммунотерапии рака: стратегии, которые пытаются омолодить сильно истощённые T‑клетки только за счёт повышения TCF1, вряд ли будут успешными. Вместо этого эффективные терапии, вероятно, должны сочетать несколько факторов или сосредоточиться на защите и расширении пула стволоподобных клеток до того, как клетки станут слишком истощёнными для спасения.
Цитирование: de Menezes, M.N., Chen, A.X.Y., Kulkarni, N. et al. High efficiency CRISPR knock-in demonstrates that TCF1 is insufficient to reverse T cell exhaustion. Nat Commun 17, 2857 (2026). https://doi.org/10.1038/s41467-026-69671-y
Ключевые слова: Истощение T‑клеток, TCF1, CRISPR-внедрение, иммунотерапия рака, стволоподобные T‑клетки