Clear Sky Science · sv
Hög-effektiv CRISPR knock-in visar att TCF1 inte räcker för att vända T-cellsutmattning
Varför utmattade immunceller spelar roll
Vårt immunsystem förlitar sig på mördande T-celler för att spåra upp virusinfekterade och cancerösa celler. Men när dessa hot kvarstår under månader kan T-celler bli ”utmattade” och förlora mycket av sin effektivitet. En särskild undergrupp av dessa celler beter sig mer som stamceller, förnyar kontinuerligt svaret och hjälper moderna cancerimmunoterapier att fungera. Denna studie ställer en bedrägligt enkel fråga med stora behandlingsimplikationer: kan vi pressa utarbetade T-celler tillbaka till detta ungdomliga, stamliknande tillstånd genom att slå på en enda huvudreglerande gen kallad TCF1?
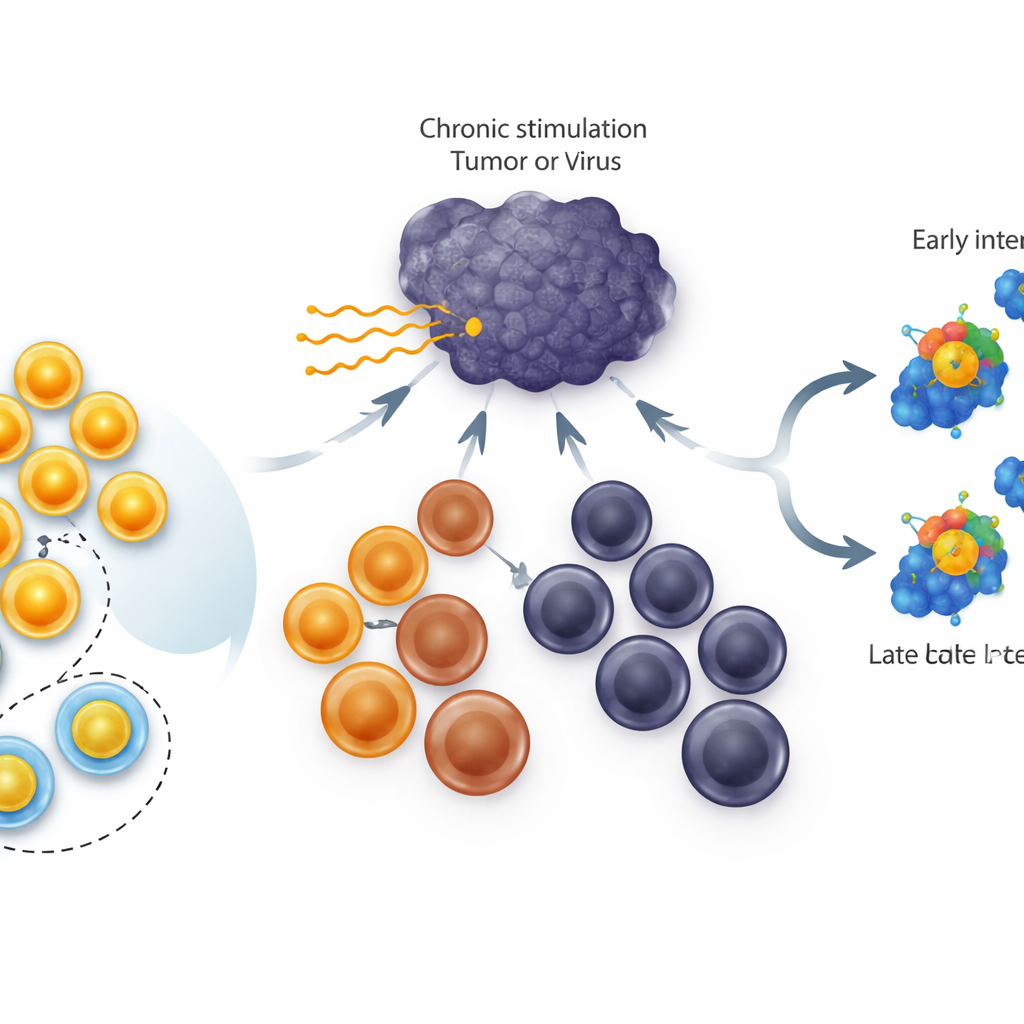
Olika varianter av utmattade T‑celler
Vid kroniska infektioner och tumörer stänger inte mördande T‑celler bara av; de passerar en stege av tillstånd. Längst upp finns stamliknande celler som delar sig väl och kan ge upphov till nya kämpar. I mitten finns ”intermediära” celler som fortfarande bidrar till sjukdomskontroll, och längst ner finns terminalt utmattade celler med liten flexibilitet kvar. Genen TCF1 är mycket aktiv i den stamliknande gruppen och är känd för att vara avgörande för deras bildning och överlevnad. Tidigare arbete visade att konstant förstärkning av TCF1 i alla utmattade celler ökar storleken på den stamliknande poolen. Vad som var okänt var om TCF1 faktiskt kan spola tillbaka mer avancerade, utmattade celler uppför stegen till det stamliknande tillståndet.
Bygga ett precist genredigeringsverktyg i möss
För att ta itu med detta behövde forskarna först ett mycket effektivt sätt att infoga ny DNA i mus‑T‑celler utan att störa deras naturliga beteende i kroppen. De optimerade en homologi‑driven reparationsform av CRISPR‑redigering som använder en AAV6‑viral mall för att ”knocka in” nytt genetiskt material på precisa platser i genomet. Genom att noggrant aktivera T‑celler, leverera CRISPR‑komponenterna, ge cellerna en kort vila i laboratoriet och sedan överföra dem tillbaka till mössen kunde de nå knock‑in‑frekvenser på 40–80 procent — nivåer jämförbara med eller bättre än traditionell viral överexpression. De visade också hur man sätter in gener utan att bryta viktiga värdgener och hur man riktar specifika genetiska adresser så att en ny gen slås på bara i vissa T‑cellsundergrupper.
Slå på TCF1 tidigt kontra sent
Kärnan i studien jämför två strategier för att slå på TCF1. I den ena satte teamet in TCF1 på en plats som är aktiv i alla T‑celler, så TCF1 var hög från början av svaret. I den andra placerade de TCF1 i Cx3cr1‑genen, som blir aktiv först när stamliknande celler mognar till det intermediära utmattade tillståndet. Denna andra design fungerar som en villkorlig strömbrytare som slår på TCF1 först efter att cellerna redan rört sig nedför utmattningsvägen. När de modifierade T‑cellerna testades i en väletablerad modell för kronisk viral infektion expanderade konstant TCF1 tydligt den stamliknande poolen. I kontrast ökade inte att slå på TCF1 endast i intermediära celler antalet stamliknande celler, även om de intermediära cellerna producerade lika mycket eller mer TCF1 per cell jämfört med den konstanta uttrycksdesignen.
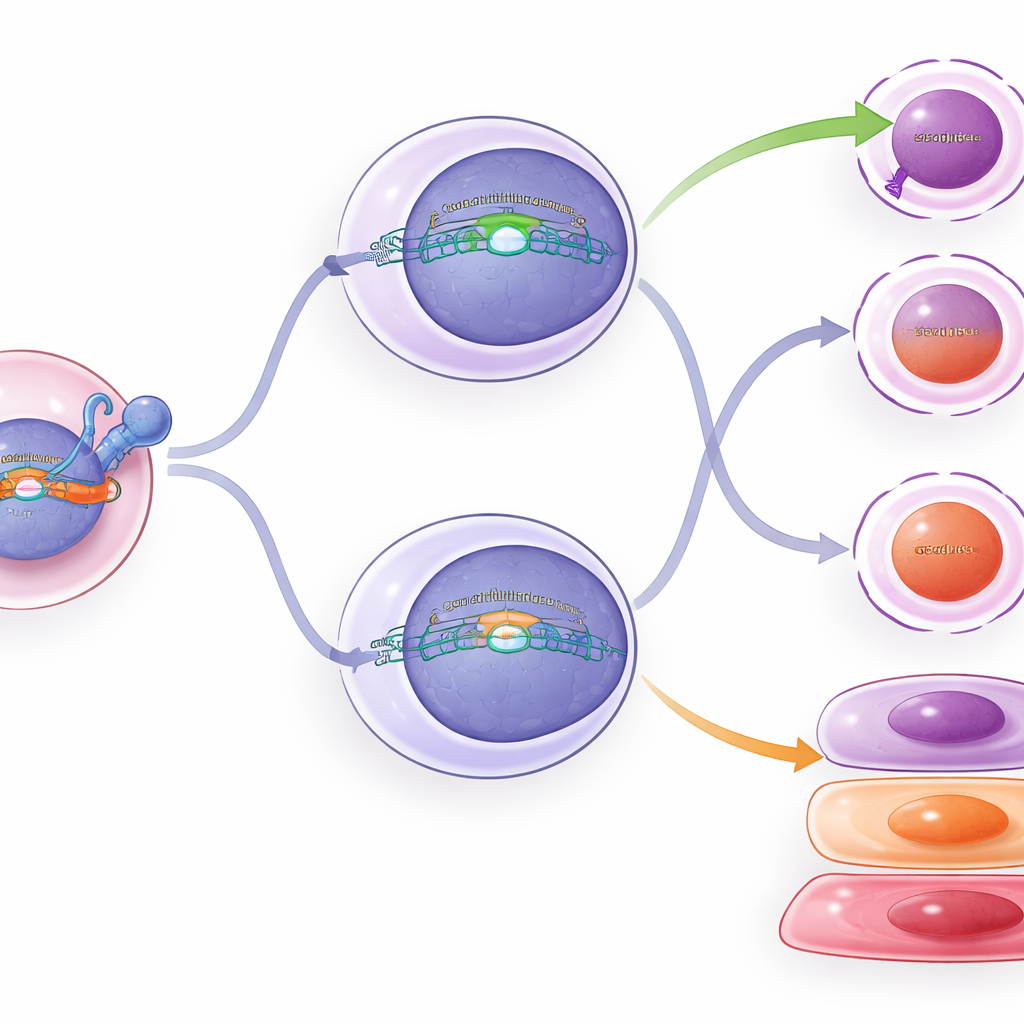
Vad som händer inne i de omkopplade cellerna
För att se bortom enkla cellräkningar profilersade teamet genaktivitet och kromatin (DNA‑paketeringen som styr vilka gener som kan slås på) i tusentals individuella T‑celler. Celler med konstant TCF1 visade fler stamliknande kluster och tidiga effektorlika celler, i linje med att TCF1 bromsar marschen mot djup utmattning. Villkorlig TCF1 i intermediära celler orsakade endast subtila förskjutningar: vissa genmönster och kromatinfunktioner lutade mot de stamliknande cellernas profiler, och markörer för utmattning sjönk något. Flödescytometri bekräftade dessa milda förändringar — intermediära celler med tillsatt TCF1 hade något mindre av vissa dödande och utmattningsassocierade proteiner, och något mer av en markör som förknippas med stamliknande celler — men de återgick inte fullt i identitet.
Varför en gen inte kan vrida tillbaka klockan
För icke‑specialisten är huvudbudskapet att när T‑celler har färdats tillräckligt långt nedför utmattningsvägen räcker det inte att bara återaktivera TCF1 för att skicka dem tillbaka till ett ungdomligt, stamliknande tillstånd. Konstant TCF1 hjälper till att bevara stamliknande celler om den finns närvarande tidigt, och bromsar därigenom åldrandet, men den kan inte ångra utmattning i efterhand. Detta har viktiga implikationer för cancerimmunoterapi: strategier som försöker föryngra starkt utmattade T‑celler genom att enbart öka TCF1 sannolikt inte kommer att fungera. Istället kan framgångsrika terapier behöva kombinera flera faktorer eller fokusera på att skydda och expandera den stamliknande poolen innan cellerna blir för utmattade för att räddas.
Citering: de Menezes, M.N., Chen, A.X.Y., Kulkarni, N. et al. High efficiency CRISPR knock-in demonstrates that TCF1 is insufficient to reverse T cell exhaustion. Nat Commun 17, 2857 (2026). https://doi.org/10.1038/s41467-026-69671-y
Nyckelord: T-cellsutmattning, TCF1, CRISPR knock-in, cancerimmunoterapi, stamliknande T-celler