Clear Sky Science · pt
Alta eficiência em knock-in por CRISPR demonstra que TCF1 é insuficiente para reverter a exaustão de células T
Por que células imunes exaustas importam
Nosso sistema imunológico depende de células T citotóxicas para localizar células infectadas por vírus e células cancerosas. Mas quando essas ameaças persistem por meses, as células T podem tornar-se “exaustas”, perdendo grande parte de sua potência. Um subconjunto especial dessas células comporta-se mais como células-tronco, renovando continuamente a resposta e contribuindo para o sucesso das modernas imunoterapias contra o câncer. Este estudo faz uma pergunta aparentemente simples, com grandes implicações para tratamentos: é possível empurrar células T desgastadas de volta a esse estado juvenil e com caráter de célula-tronco ativando um único gene controlador mestre chamado TCF1?
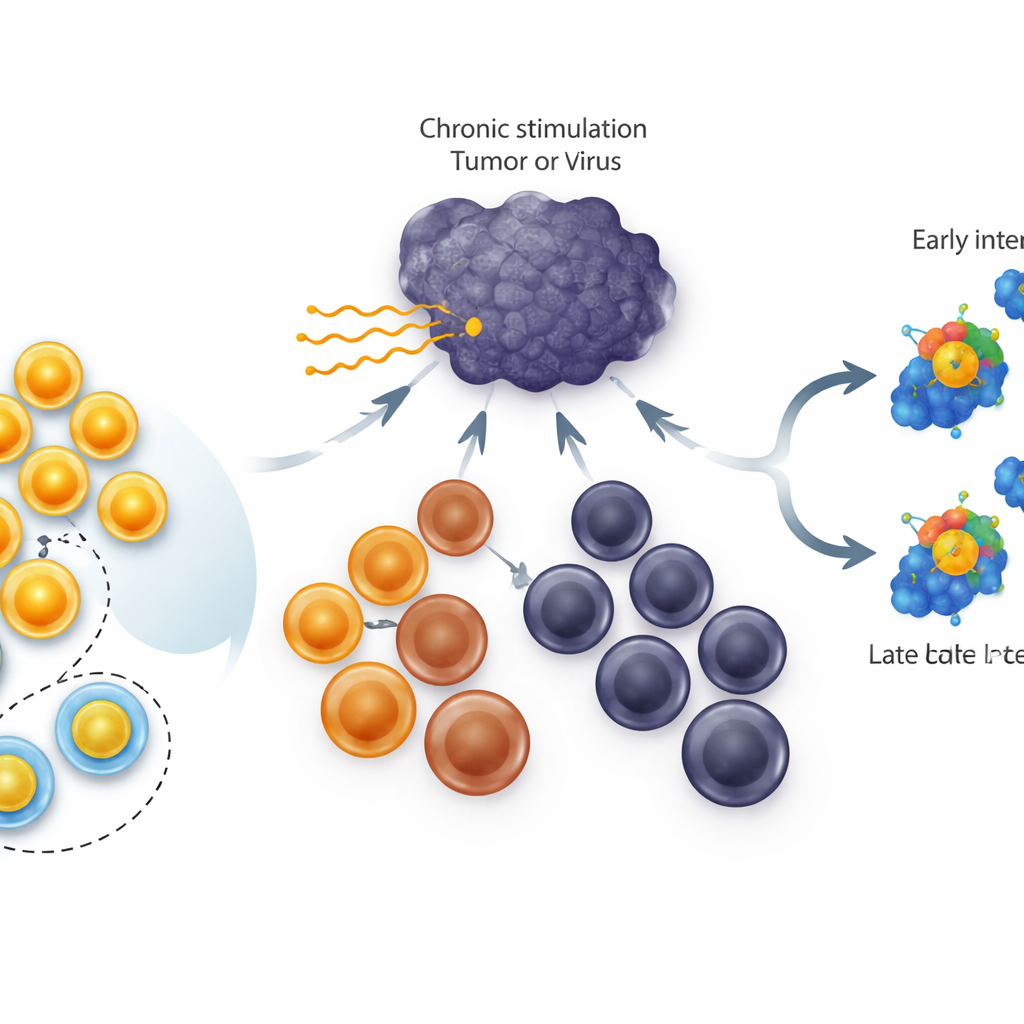
Diversos perfis de células T exaustas
Em infecções crônicas e tumores, as células T citotóxicas não se desligam de uma vez; elas atravessam uma escada de estados. No topo estão as células com caráter de célula-tronco, que se dividem bem e podem gerar novos efetores. No meio estão as células “intermediárias” que ainda contribuem para o controle da doença, e na base estão as células terminalmente exaustas, com pouca flexibilidade restante. O gene TCF1 é altamente ativo no grupo com caráter de célula-tronco e sabe-se que é essencial para sua formação e sobrevivência. Trabalhos anteriores mostraram que aumentar constantemente TCF1 em todas as células exaustas amplia o pool de células com caráter de célula-tronco. O que não se sabia era se TCF1 pode realmente rebobinar células exaustas mais avançadas de volta pela escada até esse estado com características de célula-tronco.
Construindo uma caixa de ferramentas precisa de edição gênica em camundongos
Para abordar isso, os pesquisadores precisaram primeiro de uma maneira altamente eficiente de inserir novo DNA em células T de camundongos sem perturbar seu comportamento natural dentro do organismo. Eles otimizaram uma edição CRISPR por reparo direcionado por homologia que usa um molde viral AAV6 para “knock-in” de novo material genético em pontos precisos do genoma. Ativando cuidadosamente as células T, entregando os componentes CRISPR, deixando as células repousarem brevemente em laboratório e então transferindo-as para os camundongos, eles conseguiram taxas de knock-in de 40–80% — níveis comparáveis ou superiores à superexpressão viral tradicional. Também mostraram como inserir genes sem interromper genes hospedeiros importantes e como mirar endereços genéticos específicos para que um novo gene seja ativado apenas em subconjuntos específicos de células T.
Ativar TCF1 cedo versus tarde
O cerne do estudo compara duas estratégias para ativar TCF1. Em uma, a equipe inseriu TCF1 em um local ativo em todas as células T, de modo que TCF1 ficasse alto desde o início da resposta. Na outra, inseriram TCF1 no gene Cx3cr1, que só se torna ativo quando células com caráter de célula-tronco amadurecem para o estado exausto intermediário. Esse segundo desenho age como um interruptor condicional, ligando TCF1 somente depois que as células já avançaram no caminho da exaustão. Quando as células T modificadas foram testadas em um modelo estabelecido de infecção viral crônica, a expressão constante de TCF1 claramente expandiu o pool de células com caráter de célula-tronco. Em contraste, ativar TCF1 apenas nas células intermediárias não aumentou o número de células com caráter de célula-tronco, mesmo que essas células intermediárias produzissem tanto ou mais TCF1 por célula do que no arranjo de expressão constante.
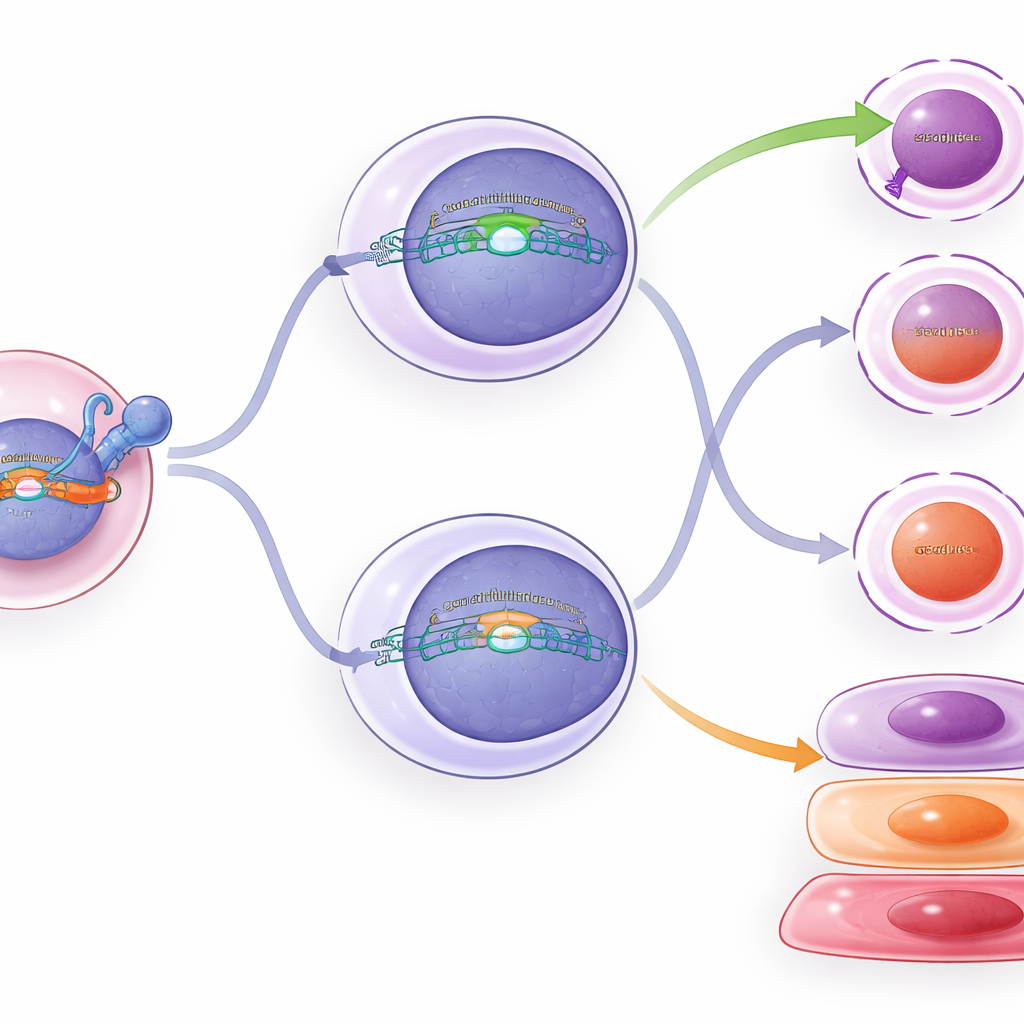
O que acontece dentro das células reprogramadas
Para ir além das contagens simples de células, a equipe perfilou a atividade gênica e a cromatina (o empacotamento do DNA que controla quais genes podem ser ativados) em milhares de células T individuais. Células com TCF1 constante mostraram mais agrupamentos com características de célula-tronco e mais células com perfil inicial de efetor, consistente com TCF1 retardando a marcha rumo à exaustão profunda. TCF1 condicional nas células intermediárias causou apenas mudanças sutis: alguns padrões gênicos e características de cromatina se moveram na direção das células com caráter de célula-tronco, e marcadores de exaustão diminuíram levemente. Citometria de fluxo confirmou essas mudanças modestas — células intermediárias com TCF1 adicional apresentaram um pouco menos de certas proteínas de citotoxicidade e exaustão, e um pouco mais de um marcador associado a células com caráter de célula-tronco — mas não reverteram completamente sua identidade.
Por que um único gene não pode voltar no tempo
Para quem não é especialista, a mensagem principal é que, uma vez que as células T tenham avançado o suficiente pela via da exaustão, simplesmente reativar TCF1 não basta para enviá-las de volta a um estado juvenil com características de célula-tronco. TCF1 constante ajuda a preservar as células com caráter de célula-tronco se estiver presente desde cedo, retardando efetivamente o envelhecimento, mas não consegue desfazer a exaustão depois que ela está estabelecida. Isso tem implicações importantes para a imunoterapia contra o câncer: estratégias que tentem rejuvenescer células T fortemente exaustas apenas aumentando TCF1 provavelmente não serão eficazes. Em vez disso, terapias bem-sucedidas podem precisar combinar vários fatores ou focar em proteger e expandir o pool de células com caráter de célula-tronco antes que as células se tornem excessivamente exaustas para serem resgatadas.
Citação: de Menezes, M.N., Chen, A.X.Y., Kulkarni, N. et al. High efficiency CRISPR knock-in demonstrates that TCF1 is insufficient to reverse T cell exhaustion. Nat Commun 17, 2857 (2026). https://doi.org/10.1038/s41467-026-69671-y
Palavras-chave: exaustão de células T, TCF1, knock-in por CRISPR, imunoterapia contra o câncer, células T com caráter de célula-tronco