Clear Sky Science · de
Hohe Effizienz von CRISPR-Knock‑ins zeigt, dass TCF1 nicht ausreicht, um T‑Zell‑Erschöpfung umzukehren
Warum müde Immunzellen wichtig sind
Unser Immunsystem ist auf Killer‑T‑Zellen angewiesen, um virusinfizierte und entartete Zellen aufzuspüren. Wenn solche Bedrohungen jedoch über Monate andauern, können T‑Zellen „erschöpfen“ und einen Großteil ihrer Schlagkraft verlieren. Eine spezielle Untergruppe dieser Zellen verhält sich eher wie Stammzellen: Sie erneuern die Antwort fortlaufend und tragen zum Erfolg moderner Krebsimmuntherapien bei. Diese Studie stellt eine auf den ersten Blick einfache, aber therapeutisch wichtige Frage: Kann man erschöpfte T‑Zellen wieder in diesen jugendlichen, stammähnlichen Zustand zurückversetzen, indem man ein einzelnes Master‑Steuergen namens TCF1 aktiviert?
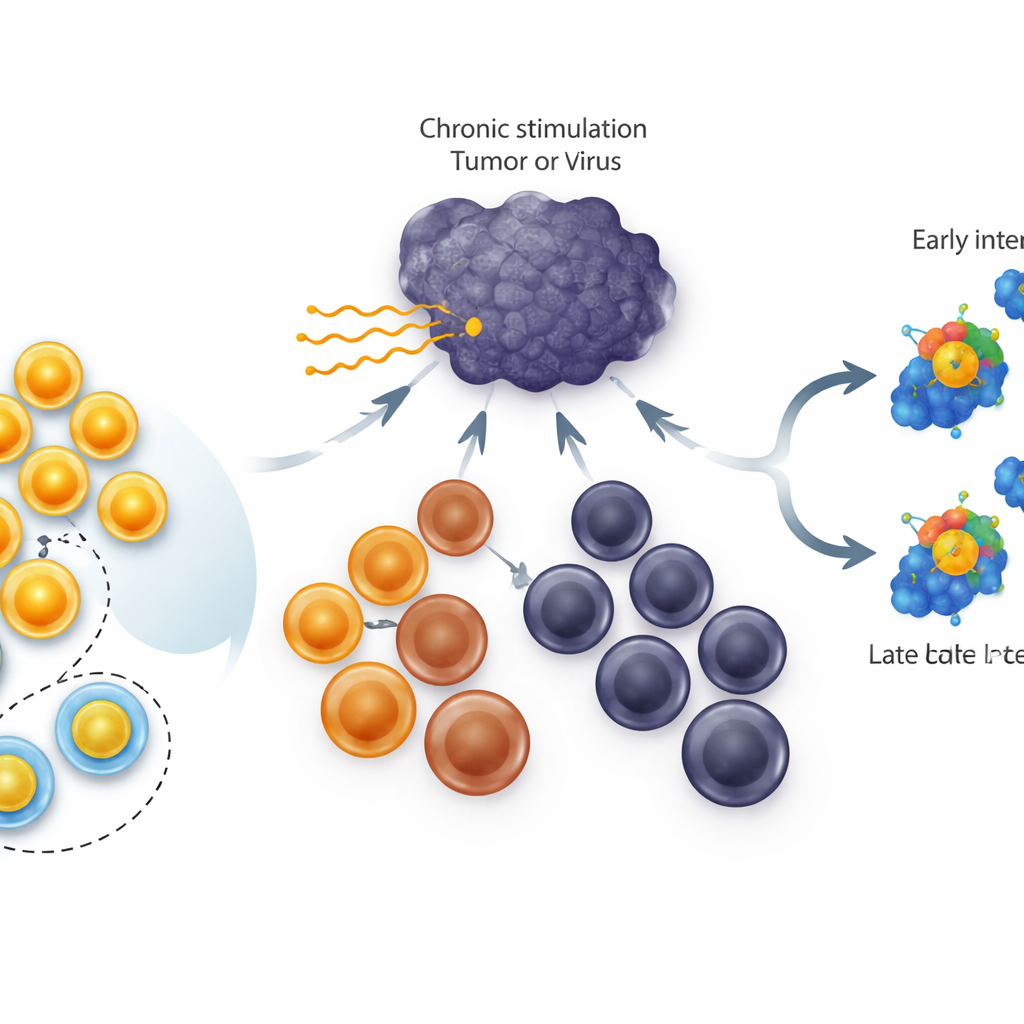
Verschiedene Ausprägungen müder T‑Zellen
Bei chronischen Infektionen und in Tumoren schalten Killer‑T‑Zellen nicht einfach aus; sie durchlaufen eine Abfolge von Zuständen. An der Spitze stehen stammähnliche Zellen, die sich gut teilen und neue Effektorzellen hervorbringen können. In der Mitte finden sich „intermediäre“ Zellen, die noch zur Krankheitskontrolle beitragen, und am Ende stehen terminal erschöpfte Zellen mit wenig verbleibender Flexibilität. Das Gen TCF1 ist in der stammähnlichen Gruppe stark aktiv und für deren Entstehung und Überleben bekannt. Frühere Arbeiten zeigten, dass eine konstante Erhöhung von TCF1 in allen erschöpften Zellen die Größe des stammähnlichen Pools vergrößert. Unklar war jedoch, ob TCF1 fortgeschrittene, stärker erschöpfte Zellen tatsächlich wieder die Leiter hinauf in den stammähnlichen Zustand zurückdrehen kann.
Aufbau eines präzisen Genschneide‑Werkzeugs in Mäusen
Um das zu untersuchen, brauchten die Forschenden zunächst eine sehr effiziente Methode, um neue DNA in Maus‑T‑Zellen einzufügen, ohne ihr natürliches Verhalten im Körper zu stören. Sie optimierten eine Form der CRISPR‑Bearbeitung, die auf homologer Reparatur beruht und eine AAV6‑Virusvorlage nutzt, um neue genetische Fracht an präzisen Stellen im Genom „knock‑in“ zu bringen. Durch gezielte Aktivierung der T‑Zellen, Auslieferung der CRISPR‑Komponenten, eine kurze Ruhephase im Labor und anschließende Übertragung in Mäuse erreichten sie Knock‑in‑Raten von 40–80 Prozent — Werte, die mit oder besser als traditionelle virale Überexpression vergleichbar sind. Sie zeigten außerdem, wie Gene eingefügt werden können, ohne wichtige Wirtsgene zu zerstören, und wie man spezifische Genorte ansteuert, sodass ein neues Gen nur in bestimmten T‑Zell‑Untergruppen aktiv wird.
TCF1 früh versus spät einschalten
Der Kern der Studie vergleicht zwei Strategien, um TCF1 zu aktivieren. In der einen Variante setzten die Forschenden TCF1 an einen Ort ein, der in allen T‑Zellen aktiv ist, sodass TCF1 von Beginn der Antwort an hoch ist. In der anderen Variante platzierten sie TCF1 in das Cx3cr1‑Gen, das erst aktiv wird, wenn stammähnliche Zellen zum intermediären erschöpften Zustand heranreifen. Dieses zweite Design wirkt wie ein bedingter Schalter und schaltet TCF1 erst ein, nachdem die Zellen bereits den Erschöpfungspfad hinabgewandert sind. In einem etablierten Modell chronischer Virusinfektion führte konstante TCF1‑Expression klar zu einer Vergrößerung des stammähnlichen Pools. Im Gegensatz dazu erhöhte das gezielte Einschalten von TCF1 nur in intermediären Zellen nicht die Zahl stammähnlicher Zellen, obwohl diese intermediären Zellen pro Zelle genauso viel oder mehr TCF1 produzierten wie bei der konstanten Expression.
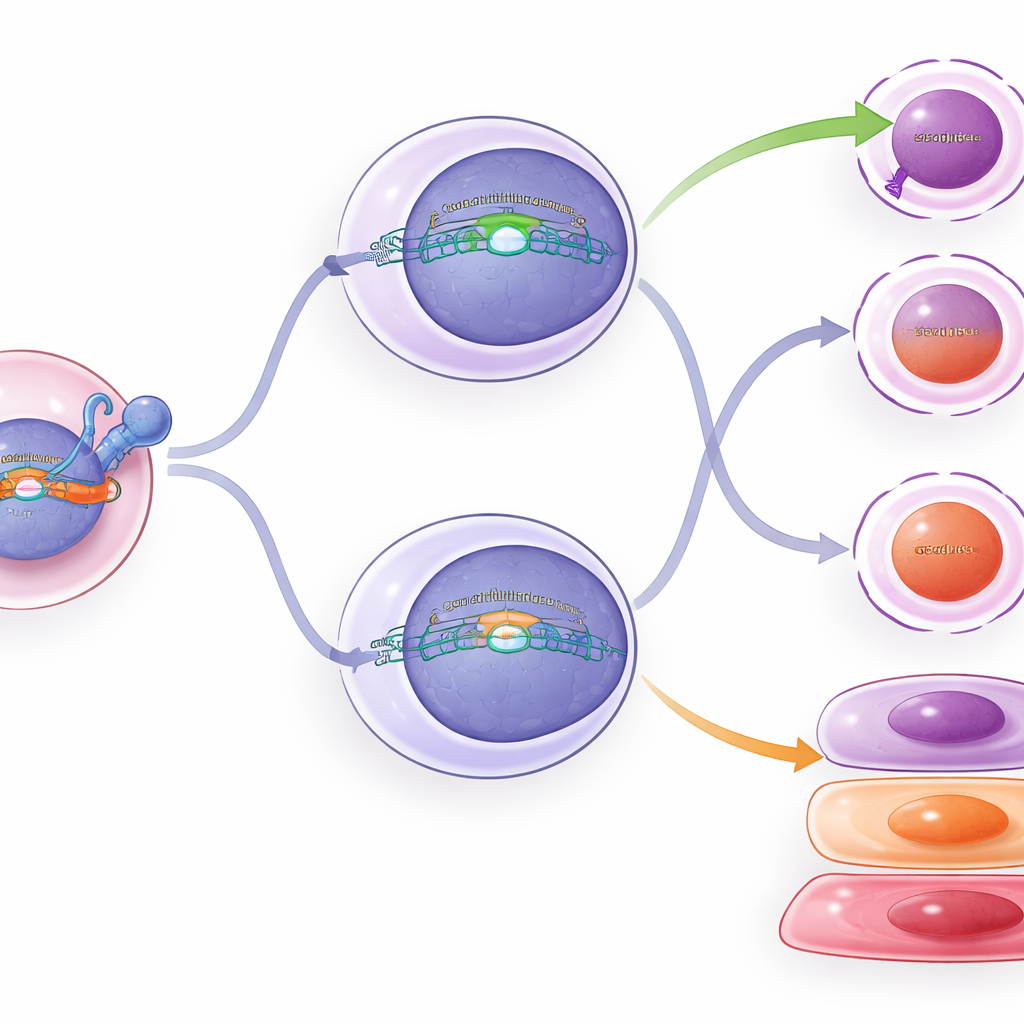
Was in den umprogrammierten Zellen passiert
Um über einfache Zellzählungen hinauszublicken, analysierte das Team Genaktivität und Chromatin (die DNA‑Verpackung, die steuert, welche Gene eingeschaltet werden können) in Tausenden einzelner T‑Zellen. Zellen mit konstanter TCF1‑Expression zeigten mehr stammähnliche Cluster und frühe Effektor‑ähnliche Zellen, was konsistent damit ist, dass TCF1 das Fortschreiten zur tiefen Erschöpfung verlangsamt. Bedingtes TCF1 in intermediären Zellen verursachte nur subtile Verschiebungen: Einige Genmuster und Chromatinmerkmale bewegten sich in Richtung der stammähnlichen Zellen, und Erschöpfungsmarker sanken leicht. Durchflusszytometrie bestätigte diese milden Veränderungen — intermediäre Zellen mit zusätzlichem TCF1 zeigten etwas weniger bestimmter Killer‑ und Erschöpfungsproteine und etwas mehr eines mit stammähnlichen Zellen assoziierten Markers — aber sie revertierten nicht vollständig in ihre Identität.
Warum ein Gen die Uhr nicht zurückdrehen kann
Für Nicht‑Spezialisten lautet die wichtigste Botschaft: Haben T‑Zellen den Erschöpfungsweg weit genug beschritten, reicht das bloße Reaktivieren von TCF1 nicht aus, um sie zurück in einen jugendlichen, stammähnlichen Zustand zu versetzen. Konstantes TCF1 hilft, stammähnliche Zellen zu erhalten, wenn es von Anfang an vorhanden ist und so das „Altern“ verlangsamt, aber es kann Erschöpfung im Nachhinein nicht rückgängig machen. Das hat wichtige Konsequenzen für die Krebsimmuntherapie: Strategien, die versuchen, stark erschöpfte T‑Zellen allein durch Anheben von TCF1 zu verjüngen, werden wahrscheinlich nicht erfolgreich sein. Stattdessen könnten erfolgreiche Therapien mehrere Faktoren kombinieren oder darauf abzielen, den stammähnlichen Pool zu schützen und zu erweitern, bevor die Zellen zu erschöpft sind, um noch gerettet zu werden.
Zitation: de Menezes, M.N., Chen, A.X.Y., Kulkarni, N. et al. High efficiency CRISPR knock-in demonstrates that TCF1 is insufficient to reverse T cell exhaustion. Nat Commun 17, 2857 (2026). https://doi.org/10.1038/s41467-026-69671-y
Schlüsselwörter: T‑Zell‑Erschöpfung, TCF1, CRISPR‑Knock‑in, Krebsimmuntherapie, stammähnliche T‑Zellen