Clear Sky Science · zh
TGFβ活化的PDHB促进线粒体丙酮酸代谢并通过ATP依赖的BRG1促进人内胚层分化
燃料利用如何塑造早期人类发育
我们的人体起始于一小团必须决定自身将成为什么组织的干细胞。该研究提出了一个看似世俗但关键的问题:这些早期细胞如何燃烧糖类,会如何影响它们形成肝、肺和胰腺等器官的抉择?通过并行追踪能量利用与DNA调控,研究者表明一种特定的糖代谢转换不仅是背景变化,而是早期人类发育的积极驱动因子。
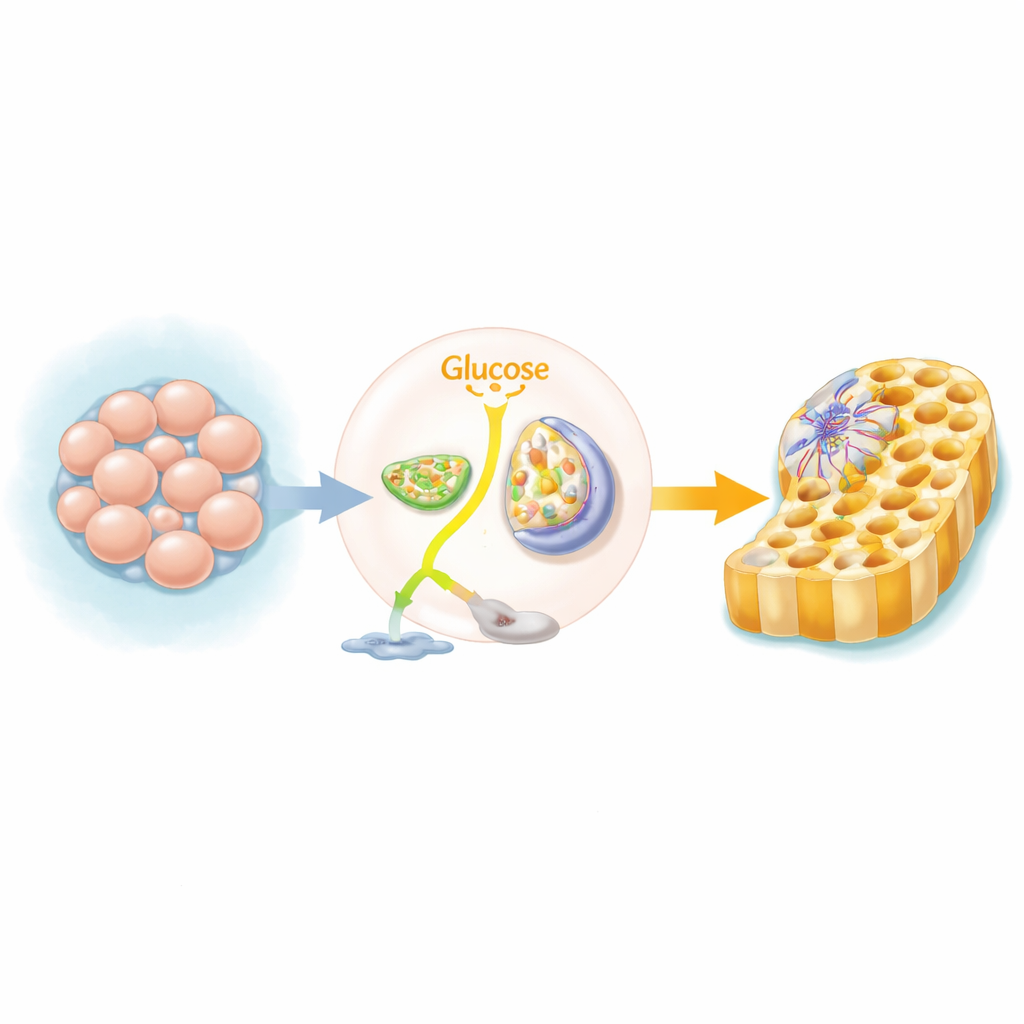
出芽组织中的代谢开关
人多能干细胞可以形成几乎任何组织,通常依赖快速但效率较低的糖代谢途径,即即便在有氧情况下也将葡萄糖分解为乳酸。当这些细胞开始形成“终末内胚层”——即肠道、肝脏和胰腺的前体层时,它们会转换主要的能量通路。细胞不再把糖大量转向乳酸生成,而是将更多糖送入线粒体,运行三羧酸(TCA)循环和氧化磷酸化。研究团队利用全基因组CRISPR筛选和一系列化学抑制剂表明,当该开关被阻断时,成功获得内胚层身份的细胞数量大幅减少。
将糖转化为线粒体能量
这一开关的核心是丙酮酸,它是葡萄糖分解的重要产物。丙酮酸可以被转化为乳酸,或被运入线粒体并转变为乙酰辅酶A,进入TCA循环。研究者发现,将丙酮酸导向线粒体强烈有利于内胚层形成。抑制乳酸生成酶的药物会推动更多丙酮酸进入线粒体并促进分化,而阻止丙酮酸进入线粒体或在线粒体中被处理的化合物则显著降低内胚层标志物。向细胞补充丙酮酸或谷氨酰胺(一种TCA循环的替代燃料)可以在早期糖代谢受阻时帮助恢复这一发育路径。
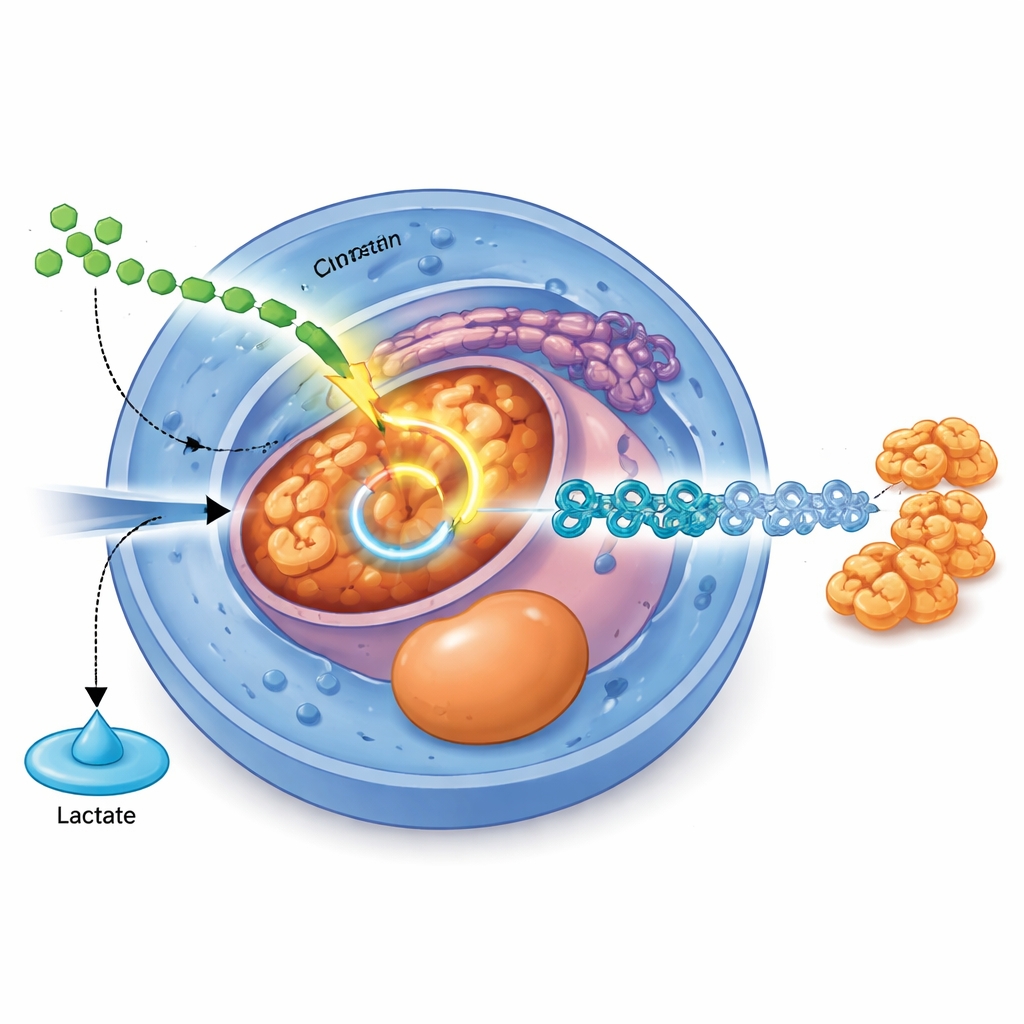
重接代谢的信号通路
该研究鉴定了将外部信号与内部燃料重编程相连的特定分子开关。一个著名的生长信号TGFβ,通过其信使蛋白SMAD2和SMAD3,直接上调PDHB的表达——PDHB是将丙酮酸送入TCA循环的丙酮酸脱氢酶复合体的核心成分。当使用CRISPR下调PDHB时,细胞产生更多乳酸、乙酰辅酶A减少,并难以从干细胞阶段向内胚层及后续胰腺阶段推进。相反,提高PDHB水平可以增强线粒体活性、提高细胞能量,并改善内胚层分化的效率,尤其在TGFβ信号本身较弱时更为明显。
能量水平控制对遗传脚本的访问
为什么这种燃料选择对细胞身份如此重要?作者把影响追溯到ATP——细胞的主要能量货币。阻断葡萄糖分解或线粒体入口会降低ATP水平,而简单地从外部补充额外ATP可以在多种情形下挽救失败的内胚层分化。关键的ATP消耗者是BAF复合体,这是一个以蛋白BRG1为核心的大型“染色质重塑”机器,依赖ATP打开折叠的DNA。当用化学方法抑制BAF或降解/突变BRG1,使其ATP驱动的马达失去功能时,内胚层形成受阻,额外ATP也不再起作用。全基因组染色质可及性绘图显示,当PDHB或线粒体丙酮酸利用降低时,许多靠近内胚层相关基因的区域变得不那么可及,尤其是BRG1通常结合的增强子区域。
这对从细胞构建器官意味着什么
综合来看,这项工作描绘出一条明确的事件链:TGFβ信号上调PDHB,PDHB将丙酮酸引入线粒体,线粒体代谢提升ATP水平,而ATP为BRG1驱动的关键DNA区域开放提供动力,从而使内胚层基因得以启动。简言之,早期人类细胞燃烧糖的方式决定了它们有多少“能量预算”去解锁成为肠道及器官形成组织所需的基因组部分。理解并控制这一燃料开关,可望改进从干细胞培养特定人类组织的方法,用于研究、疾病建模及未来的细胞治疗应用。
引用: Meng, L., Lv, J., Yi, Y. et al. TGFβ-activated PDHB promotes mitochondrial pyruvate metabolism and contributes to human endoderm differentiation via ATP-dependent BRG1. Nat Commun 17, 2846 (2026). https://doi.org/10.1038/s41467-026-69510-0
关键词: 干细胞代谢, 内胚层分化, 线粒体丙酮酸, 染色质重塑, TGFβ信号