Clear Sky Science · nl
TGFβ-geactiveerde PDHB bevordert mitochondriale pyruvaatmetabolisme en draagt bij aan humane endodermdifferentiatie via ATP-afhankelijke BRG1
Hoe brandstofgebruik vroege menselijke ontwikkeling vormt
Onze lichamen beginnen als kleine bolletjes stamcellen die moeten beslissen tot welke weefsels ze zich ontwikkelen. Deze studie stelt een verrassend aards vraagstuk: hoe beïnvloedt de manier waarop deze vroege cellen suiker verbranden hun besluit om organen zoals lever, longen en alvleesklier te vormen? Door energiegebruik en DNA-regulatie tegelijk te volgen, laten de onderzoekers zien dat een specifieke verschuiving in suikermetabolisme niet slechts achtergrond is, maar een actieve motor van vroege menselijke ontwikkeling.
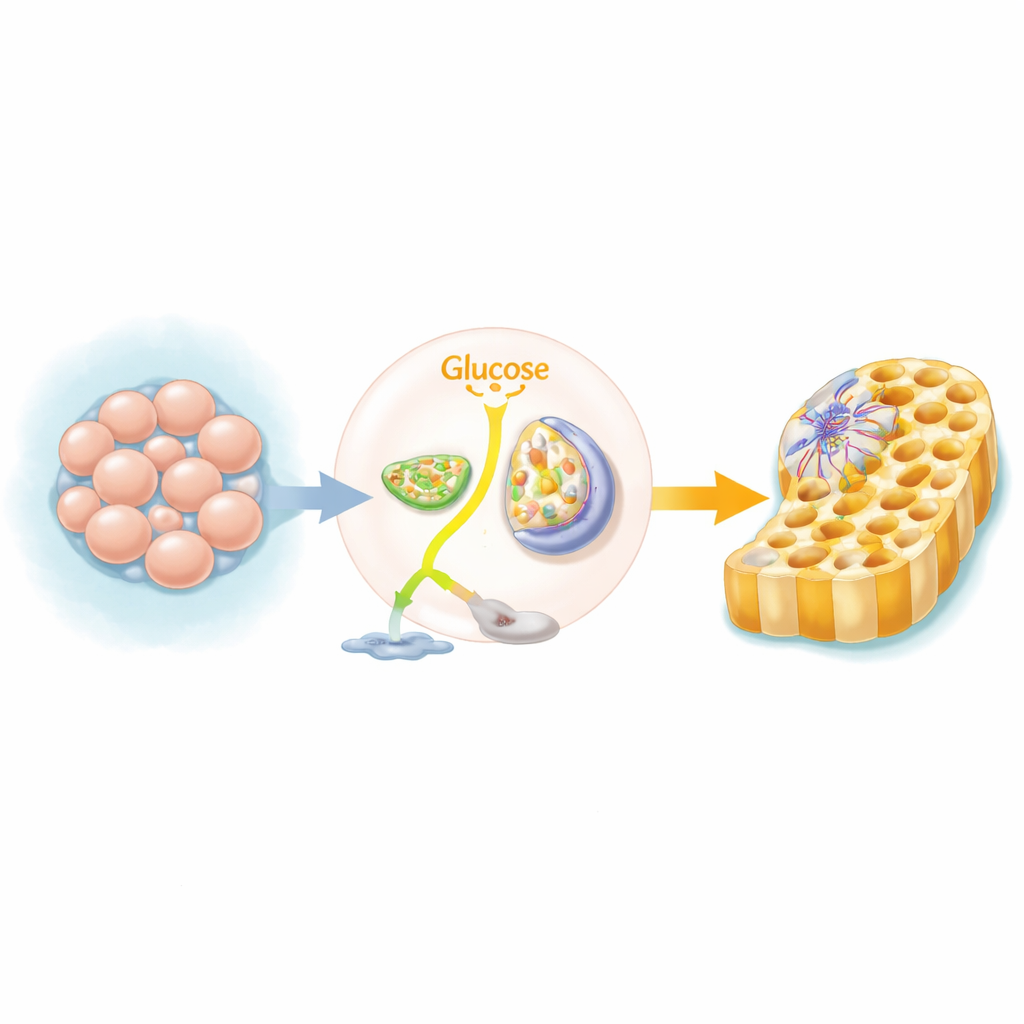
Een metabole schakel in zich vormende weefsels
Humane pluripotente stamcellen, die vrijwel elk weefsel kunnen vormen, vertrouwen normaal gesproken op een snelle maar inefficiënte manier om suiker te gebruiken, waarbij glucose wordt afgebroken tot lactaat zelfs wanneer zuurstof beschikbaar is. Wanneer deze cellen beginnen het “definitieve endoderm” te vormen—de voorloper van darm, lever en alvleesklier— schakelen ze hun belangrijkste brandstofroute om. In plaats van suiker naar lactaat te leiden, sturen ze meer ervan naar de mitochondriën, de energiecentrales van de cel, om de tricarbonzuurcyclus (TCA) en oxidatieve fosforylering aan te drijven. Het team gebruikte genoombrede CRISPR-screens en een reeks chemische blokkades om aan te tonen dat wanneer deze omschakeling wordt geblokkeerd, veel minder cellen met succes een endodermidentiteit aannemen.
Suiker omzetten in mitochondriale energie
In het hart van deze omschakeling ligt pyruvaat, een belangrijk afbraakproduct van glucose. Pyruvaat kan ofwel worden omgezet in lactaat ofwel worden geïmporteerd in mitochondriën en daar omgezet in acetyl-CoA, het toegangsticket tot de TCA-cyclus. De onderzoekers vonden dat het sturen van pyruvaat richting mitochondriën sterk de endodermvorming bevordert. Middelen die de lactaatvormende enzymen remmen dwingen meer pyruvaat naar de mitochondriën en versterken differentiatie, terwijl verbindingen die voorkomen dat pyruvaat de mitochondriën binnengaat of daar verwerkt wordt, de endodermmarkers sterk verminderen. Het aanvullen van cellen met pyruvaat of glutamine, een andere brandstof voor de TCA-cyclus, helpt dit ontwikkelingspad te herstellen wanneer vroege stappen van suikergebruik worden geblokkeerd.
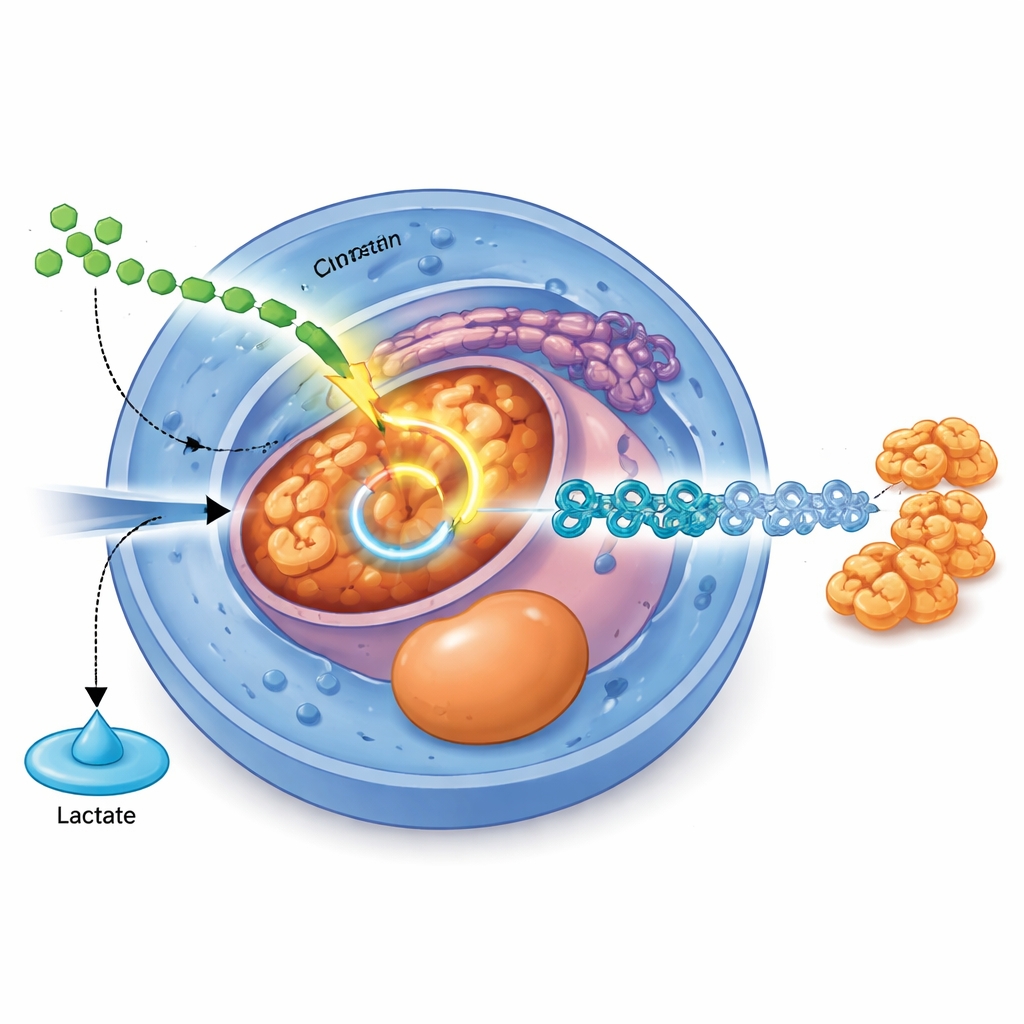
Een signaalpad dat het metabolisme herbedraadt
De studie identificeert een specifieke moleculaire schakel die externe signalen koppelt aan deze interne brandstofomleiding. Een bekend groeisignaal, TGFβ, werkt via zijn boodschapperproteïnen SMAD2 en SMAD3 en verhoogt direct de productie van PDHB, een kerncomponent van het pyruvaatdehydrogenasecomplex dat pyruvaat in de TCA-cyclus voert. Wanneer PDHB-niveaus worden verlaagd met CRISPR-bewerking, produceren cellen meer lactaat, minder acetyl-CoA, en hebben ze moeite om zich van stamcel naar endoderm en later naar pancreatische stadia te ontwikkelen. Omgekeerd versterkt het verhogen van PDHB-niveaus de mitochondriale activiteit, verhoogt het de cellulaire energie en verbetert het de efficiëntie van endodermdifferentiatie, vooral wanneer het TGFβ-signaal zelf zwak is.
Energieniveaus bepalen toegang tot het genetische script
Waarom maakt deze brandstofkeuze zoveel uit voor identiteit? De auteurs brengen het effect terug tot ATP, de belangrijkste energievaluta van de cel. Het blokkeren van glucosedisbalans of mitochondriale toegang verlaagt ATP-niveaus, en het simpelweg aanvoeren van extra ATP van buiten kan mislukte endodermdifferentiatie in verschillende omstandigheden herstellen. De belangrijkste ATP-gebruiker is het BAF-complex, een groot “chromatine-remodellerend” apparaat gecentreerd rond het eiwit BRG1 dat ATP gebruikt om gevouwen DNA open te zetten. Wanneer BAF chemisch wordt geremd of BRG1 wordt afgebroken of gemuteerd zodat de ATP-aangedreven motor niet meer werkt, stokt de endodermvorming en kan extra ATP niet meer helpen. Genoomwijde mapping van chromatine-toegankelijkheid toont aan dat wanneer PDHB of mitochondriaal pyruvaatgebruik verminderd is, veel regio’s nabij endodermgerelateerde genen minder toegankelijk worden, met name enhancerregio’s waar BRG1 normaal bindt.
Wat dit betekent voor het bouwen van organen uit cellen
Samen genomen schetst het werk een duidelijke keten van gebeurtenissen: TGFβ-signalen verhogen PDHB-niveaus, PDHB leidt pyruvaat naar mitochondriën, mitochondriaal metabolisme verhoogt ATP, en ATP levert de energie voor BRG1-gedreven openstelling van belangrijke DNA-regio’s zodat endodermgenen aan kunnen gaan. In eenvoudige woorden: de manier waarop vroege menselijke cellen suiker verbranden bepaalt hoeveel “energiebudget” ze hebben om de delen van het genoom te ontgrendelen die nodig zijn om darm- en organenvormend weefsel te worden. Het begrijpen en controleren van deze brandstofschakel kan methoden verbeteren om specifieke menselijke weefsels uit stamcellen te kweken voor onderzoek, ziekte-modellering en toekomstige celgebaseerde therapieën.
Bronvermelding: Meng, L., Lv, J., Yi, Y. et al. TGFβ-activated PDHB promotes mitochondrial pyruvate metabolism and contributes to human endoderm differentiation via ATP-dependent BRG1. Nat Commun 17, 2846 (2026). https://doi.org/10.1038/s41467-026-69510-0
Trefwoorden: metabolisme van stamcellen, endodermdifferentiatie, mitochondriaal pyruvaat, chromatine-remodellering, TGF beta-signaaltransductie