Clear Sky Science · fr
PDHB activé par le TGFβ favorise le métabolisme mitochondrial du pyruvate et contribue à la différenciation de l’endoderme humain via BRG1 dépendant de l’ATP
Comment l’utilisation du carburant façonne le début du développement humain
Nos corps commencent comme de petites sphères de cellules souches qui doivent décider quels types de tissus elles vont devenir. Cette étude pose une question étonnamment concrète : de quelle façon la manière dont ces premières cellules brûlent le sucre influence-t-elle leur décision de former des organes comme le foie, les poumons et le pancréas ? En suivant simultanément l’usage de l’énergie et la régulation de l’ADN, les chercheurs montrent qu’un changement spécifique du métabolisme du sucre n’est pas seulement un arrière-plan mais un moteur actif du développement humain précoce.
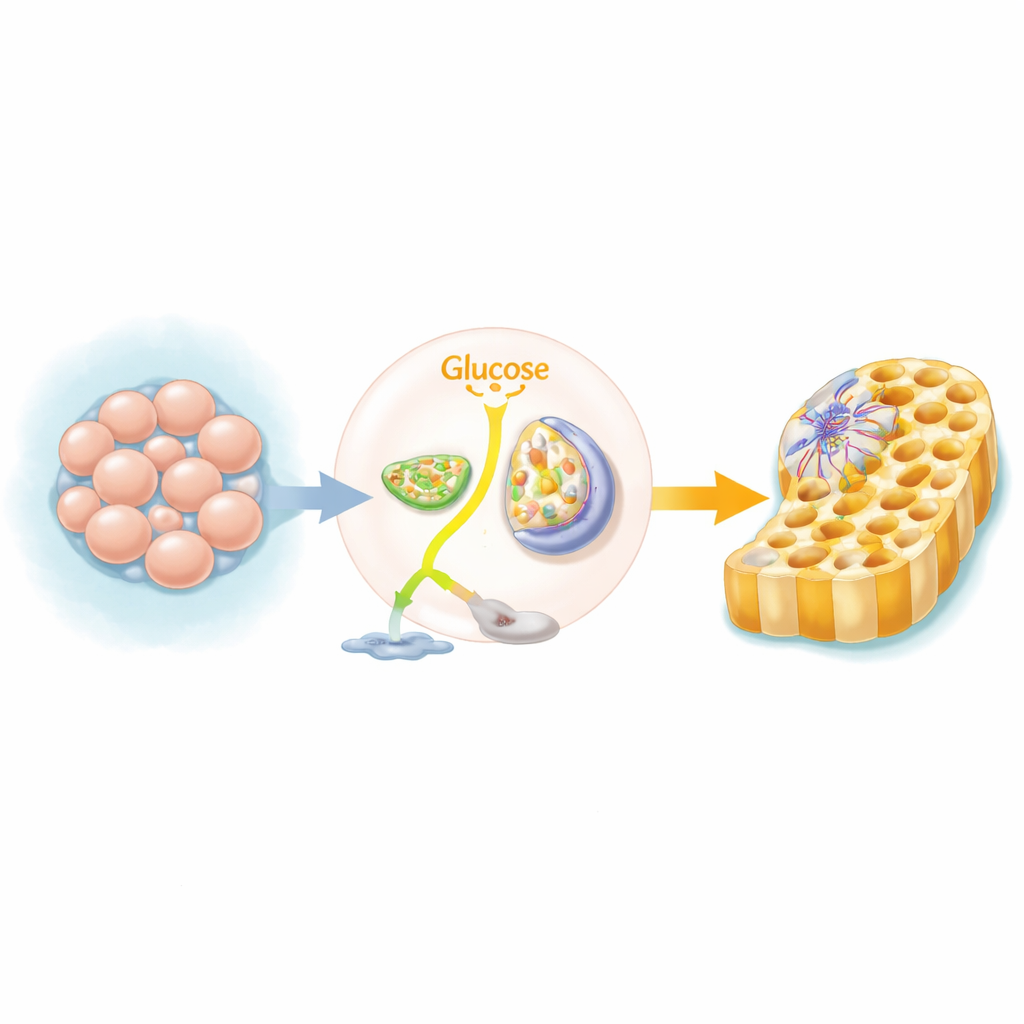
Un basculement métabolique dans les tissus en formation
Les cellules souches pluripotentes humaines, capables de former presque n’importe quel tissu, s’appuient normalement sur une voie rapide mais peu efficace d’utilisation du sucre, dégradant le glucose en lactate même en présence d’oxygène. Lorsque ces cellules commencent à former la couche dite « endoderme définitif » — le précurseur de l’intestin, du foie et du pancréas — elles changent leur route principale d’alimentation. Plutôt que de diriger le sucre vers le lactate, elles envoient davantage de molécules dans les mitochondries, les centrales énergétiques de la cellule, pour faire fonctionner le cycle des acides tricarboxyliques (TCA) et la phosphorylation oxydative. L’équipe a utilisé des cribles CRISPR à l’échelle du génome et une batterie d’inhibiteurs chimiques pour montrer que lorsque ce basculement est bloqué, beaucoup moins de cellules acquièrent l’identité d’endoderme.
Transformer le sucre en énergie mitochondriale
Au cœur de ce basculement se trouve le pyruvate, un produit clé de la dégradation du glucose. Le pyruvate peut être converti en lactate ou importé dans les mitochondries et transformé en acétyl-CoA, le billet d’entrée du cycle TCA. Les chercheurs ont constaté que diriger le pyruvate vers les mitochondries favorise fortement la formation de l’endoderme. Des médicaments qui inhibent les enzymes de production de lactate poussent plus de pyruvate vers les mitochondries et stimulent la différenciation, tandis que des composés qui empêchent le pyruvate d’entrer dans les mitochondries ou d’y être traité réduisent nettement les marqueurs de l’endoderme. Supplémenter les cellules en pyruvate ou en glutamine, un autre carburant du cycle TCA, aide à restaurer cette trajectoire développementale lorsque les premières étapes d’utilisation du sucre sont bloquées.
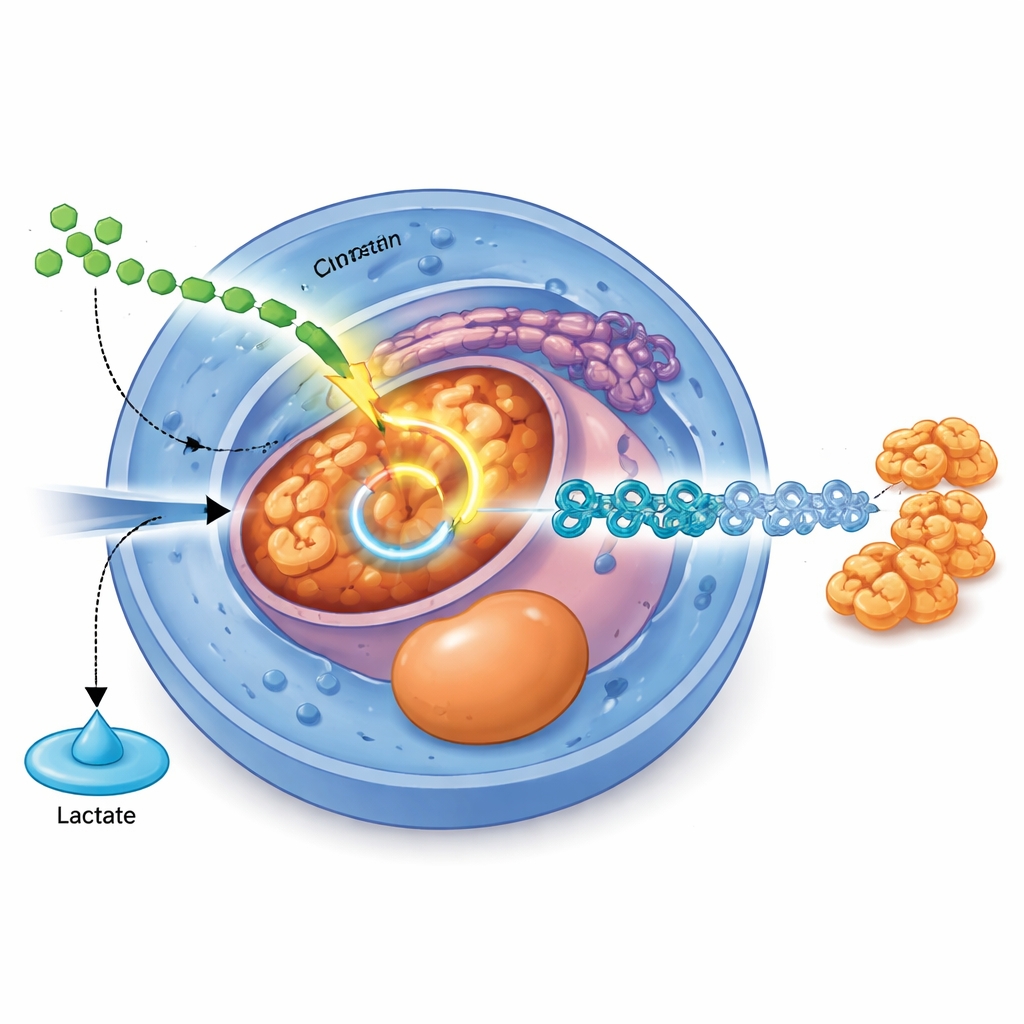
Une voie de signalisation qui reprogramme le métabolisme
L’étude identifie un interrupteur moléculaire spécifique qui relie les signaux externes à ce réacheminement interne du carburant. Un signal de croissance bien connu, le TGFβ, agissant via ses médiateurs SMAD2 et SMAD3, augmente directement la production de PDHB, un composant central du complexe pyruvate déshydrogénase qui alimente le pyruvate dans le cycle TCA. Lorsque les niveaux de PDHB sont réduits par édition CRISPR, les cellules produisent plus de lactate, moins d’acétyl‑CoA, et peinent à progresser des cellules souches vers l’endoderme puis les stades pancréatiques. À l’inverse, augmenter les niveaux de PDHB améliore l’activité mitochondriale, accroît l’énergie cellulaire et augmente l’efficacité de la différenciation en endoderme, en particulier lorsque le signal TGFβ lui‑même est faible.
Le niveau d’énergie contrôle l’accès au script génétique
Pourquoi ce choix de carburant importe‑t‑il tant pour l’identité cellulaire ? Les auteurs relient l’effet à l’ATP, la principale monnaie énergétique de la cellule. Bloquer la dégradation du glucose ou l’entrée mitochondriale abaisse les niveaux d’ATP, et fournir simplement de l’ATP supplémentaire de l’extérieur peut sauver une différenciation en endoderme échouée dans plusieurs contextes. Le consommateur d’ATP clé est le complexe BAF, une grande machine de « remodelage de la chromatine » centrée sur la protéine BRG1 qui utilise l’ATP pour dérouler l’ADN enroulé. Lorsque BAF est inhibé chimiquement ou que BRG1 est dégradé ou muté de façon à rendre son moteur dépendant de l’ATP non fonctionnel, la formation de l’endoderme faiblit et l’ATP supplémentaire ne peut plus aider. Le cartographage à l’échelle du génome de l’accessibilité de la chromatine montre que, lorsque PDHB ou l’utilisation mitochondriale du pyruvate est réduite, de nombreuses régions proches de gènes liés à l’endoderme deviennent moins accessibles, en particulier les régions enhancers où BRG1 se lie normalement.
Ce que cela signifie pour la fabrication d’organes à partir de cellules
Pris ensemble, les travaux décrivent une chaîne d’événements claire : les signaux TGFβ augmentent les niveaux de PDHB, PDHB oriente le pyruvate vers les mitochondries, le métabolisme mitochondrial élève l’ATP, et l’ATP alimente l’ouverture par BRG1 de régions clés de l’ADN afin que les gènes de l’endoderme puissent s’activer. En termes simples, la manière dont les premières cellules humaines brûlent le sucre détermine quel « budget énergétique » elles ont pour débloquer les parties du génome nécessaires à la formation des tissus intestinaux et organiques. Comprendre et contrôler ce commutateur métabolique pourrait améliorer les méthodes de culture de tissus humains spécifiques à partir de cellules souches pour la recherche, la modélisation des maladies et, à terme, des thérapies cellulaires.
Citation: Meng, L., Lv, J., Yi, Y. et al. TGFβ-activated PDHB promotes mitochondrial pyruvate metabolism and contributes to human endoderm differentiation via ATP-dependent BRG1. Nat Commun 17, 2846 (2026). https://doi.org/10.1038/s41467-026-69510-0
Mots-clés: métabolisme des cellules souches, différenciation de l’endoderme, pyruvate mitochondrial, remodelage de la chromatine, signalisation TGF bêta